Haryana State Board HBSE 12th Class Geography Important Questions Chapter 2 विश्व जनसंख्या : वितरण, घनत्व और वृद्धि Important Questions and Answers.
Haryana Board 12th Class Geography Important Questions Chapter 2 विश्व जनसंख्या : वितरण, घनत्व और वृद्धि
वस्तुनिष्ठ प्रश्न
A. नीचे दिए गए चार विकल्पों में से सही उत्तर को चुनिए
1. ईसा के जन्म के समय विश्व की जनसंख्या कितनी थी?
(A) 20 करोड़
(B) 30 करोड़
(C) 40 करोड़
(D) 80 लाख
उत्तर:
(B) 30 करोड़
2. बीसवीं शताब्दी के प्रारंभ में विश्व की जनसंख्या कितनी थी?
(A) 1 अरब
(B) 1.4 अरब
(C) 1.6 अरब
(D) 2 अरब
उत्तर:
(C) 3.
3. इक्कीसवीं शताब्दी के प्रारंभ में विश्व की जनसंख्या कितनी थी?
(A) 5 अरब
(B) 6. अरब
(C) 7 अरब
(D) 5.5 अरब
उत्तर:
(B) 6. अरब

4. बीसवीं शताब्दी के प्रारंभ में इक्कीसवीं शताब्दी के प्रारंभ तक विश्व की जनसंख्या कितने गुना बढ़ी?
(A) दो गुना
(B) तीन गुना
(C) चार गुना
(D) पांच गुना
उत्तर:
(C) चार गुना
5. विश्व के दस सर्वाधिक आबाद देशों में विश्व की कितने प्रतिशत जनसंख्या निवास करती है?
(A) लगभग 20 प्रतिशत
(B) लगभग 50 प्रतिशत
(C) लगभग 60 प्रतिशत
(D) लगभग 90 प्रतिशत
उत्तर:
(C) लगभग 60 प्रतिशत
6. मानव बसाव के लिए अनुपयुक्त स्थान कौन-सा है?
(A) आर्द्र जलवायु प्रदेश
(B) लंबे वर्धनकाल वाले प्रदेश
(C) पर्वतीय तथा ऊबड़-खाबड़ प्रदेश
(D) मैदानी प्रदेश
उत्तर:
(C) पर्वतीय तथा ऊबड़-खाबड़ प्रदेश
7. प्रति वर्ग किलोमीटर क्षेत्र में पाई जाने वाली जनसंख्या को कहा जाता है-
(A) जनसंख्या वितरण
(B) जनगणना
(C) जनसंख्या घनत्व
(D) जनसंख्या विस्फोट
उत्तर:
(C) जनसंख्या घनत्व
8. निम्नलिखित में से उच्च जनसंख्या घनत्व वाला क्षेत्र कौन-सा है?
(A) सहारा मरुस्थल
(B) अमेजन तथा जायरे बेसिन
(C) पूर्व एशिया
(D) पश्चिमी ऑस्ट्रेलिया
उत्तर:
(C) पूर्व एशिया
9. अशोधित जन्म दर से तात्पर्य है-
(A) एक वर्ष में 1000 जनसंख्या के अनुपात में पैदा होने वाले व्यक्तियों की संख्या
(B) एक वर्ष में 1000 जनसंख्या के अनुपात में मरने वालों की संख्या
(C) एक वर्ष में एक स्थान पर आने वाले व्यक्तियों की संख्या
(D) एक वर्ष में बाहर जाने वाले व्यक्तियों की संख्या
उत्तर:
(C) एक वर्ष में एक स्थान पर आने वाले व्यक्तियों की संख्या

10. कुल जनसंख्या और कुल कृषि क्षेत्र के अनुपात को कहा जाता है
(A) अंकगणितीय घनत्व
(B) कायिक घनत्व
(C) जन घनत्व
(D) इनमें से कोई नहीं
उत्तर:
(B) कायिक घनत्व
11. विश्व जनसंख्या वृद्धि की वर्तमान दर क्या है?
(A) 1 प्रतिशत
(B) 1.8 प्रतिशत
(C) 1.2 प्रतिशत
(D) 2.1 प्रतिशत
उत्तर:
(C) 1.2 प्रतिशत
12. विश्व का हर पाँचवां व्यक्ति है
(A) भारतीय
(B) चीनी
(C) रूसी
(D) अमेरिकी
उत्तर:
(B) चीनी
13. विश्व का हर छठा व्यक्ति है
(A) भारतीय
(B) चीनी
(C) रूसी
(D) अमेरिकी
उत्तर:
(A) भारतीय
14. किस महाद्वीप में ऋणात्मक जनसंख्या वृद्धि-दर पाई जाती है?
(A) अफ्रीका
(B) उत्तर अमेरिका
(C) यूरोप
(D) एशिया
उत्तर:
(C) यूरोप
15. निम्न जनसंख्या घनत्व के क्षेत्र हैं-
(A) उष्ण आर्द्र अक्षांश
(B) शुष्क भूमि
(C) ठंडी भूमि
(D) उपर्युक्त सभी
उत्तर:
(C) ठंडी भूमि
16. पहली शताब्दी में विश्व की जनसंख्या कितनी थी?
(A) 20 करोड़
(B) 25 करोड़
(C) 15 करोड़
(D) 40 करोड़
उत्तर:
(B) 25 करोड़
17. विश्व में सबसे कम जनसंख्या वृद्धि-दर किस महाद्वीप में पाई जाती है?
(A) एशिया
(B) यूरोप
(C) उत्तरी अमेरिका
(D) अफ्रीका
उत्तर:
(B) यूरोप
18. विश्व में सबसे अधिक जनसंख्या वृद्धि-दर किस देश में है?
(A) भारत में
(B) चीन में
(C) नाइजीरिया में
(D) बांग्लादेश में
उत्तर:
(C) नाइजीरिया में
19. श्रीलंका की जनसंख्या को दो गुनी होने में कितना समय लगेगा?
(A) 25 वर्ष
(B) 36 वर्ष
(C) 46 वर्ष
(D) 58 वर्ष
उत्तर:
(C) 46 वर्ष
20. भारत में विश्व की कितने प्रतिशत जनसंख्या निवास करती है?
(A) 16.87 प्रतिशत
(B) 18.01 प्रतिशत
(C) 19.20 प्रतिशत
(D) 17.5 प्रतिशत
उत्तर:
(D) 17.5 प्रतिशत
21. नाइजीरिया में विश्व की कितने प्रतिशत जनसंख्या निवास करती है?
(A) 1.84 प्रतिशत
(B) 2.09 प्रतिशत
(C) 2.13 प्रतिशत
(D) 2.43 प्रतिशत
उत्तर:
(D) 2.43 प्रतिशत
22. भारत की जनसंख्या को दो गुनी होने में कितने वर्ष लगेंगे?
(A) 25 वर्ष
(B) 30 वर्ष
(C) 36 वर्ष
(D) 46 वर्ष
उत्तर:
(C) 36 वर्ष
B. निम्नलिखित प्रश्नों के उत्तर एक शब्द में दीजिए
प्रश्न 1.
ईसा के जन्म के समय विश्व की जनसंख्या कितनी थी?
उत्तर:
30 करोड़।
प्रश्न 2.
बीसवीं शताब्दी के प्रारंभ में विश्व की जनसंख्या कितनी थी?
उत्तर:
1.6 अरब।
प्रश्न 3.
इक्कीसवीं शताब्दी के प्रारंभ में विश्व की जनसंख्या कितनी थी?
उत्तर:
लगभग 6 अरब से अधिक।
प्रश्न 4.
बीसवीं शताब्दी के प्रारंभ से इक्कीसवीं शताब्दी के प्रारंभ तक विश्व की जनसंख्या कितने गुना बढ़ी?
उत्तर:
चार गुना।

प्रश्न 5.
मानव बसाव के लिए अनुपयुक्त स्थान कौन-सा है?
उत्तर:
पर्वतीय तथा ऊबड़-खाबड़ प्रदेश।
प्रश्न 6.
प्रति वर्ग किलोमीटर क्षेत्र में पाई जाने वाली जनसंख्या को क्या कहा जाता है?
उत्तर:
जनसंख्या घनत्व।
प्रश्न 7.
कुल जनसंख्या और कुल कृषि क्षेत्र के अनुपात को क्या कहा जाता है?
उत्तर:
कायिक घनत्व।
प्रश्न 8.
विश्व में नगरीय जनसंख्या का प्रतिशत कितना है? (वर्ष, 2001)
उत्तर:
48 प्रतिशत।
प्रश्न 9.
विश्व में उच्चतम जनसंख्या वृद्धि दर (2%+) वाले एक महाद्वीप का नाम लिखिए।
उत्तर:
अफ्रीका।
प्रश्न 10.
विश्व में मध्यम जनसंख्या वृद्धि दर (1.1-1.9%) वाले एक महाद्वीप का नाम लिखिए।
उत्तर:
दक्षिण अमेरिका।
प्रश्न 11.
विश्व में न्यूनतम जनसंख्या वृद्धि दर (0-1%) वाले एक महाद्वीप का नाम लिखिए।
उत्तर:
यूरोप।
प्रश्न 12.
पहली शताब्दी में विश्व की जनसंख्या कितनी थी?
उत्तर:
लगभग 25 करोड़।
प्रश्न 13.
विश्व की जनसंख्या में प्रति वर्ष कितने लोग जुड़ रहे हैं?
उत्तर:
लगभग 8.2 करोड़।
प्रश्न 14.
विश्व में सर्वाधिक जनसंख्या का संकेंद्रण कहाँ पर होता है?
उत्तर:
मैदानी क्षेत्रों पर।
प्रश्न 15.
विश्व में जनसंख्या वितरण का प्रारूप कैसा है?
उत्तर:
असमान।
प्रश्न 16.
किन्हीं दो प्रतिकर्ष कारकों के नाम लिखिए जो लोगों को उनके रहने के मूल स्थान से प्रवास करने के लिए उत्तरदायी होते हैं।
उत्तर:
- प्राकृतिक आपदा
- सामाजिक तनाव।
अति-लघूत्तरात्मक प्रश्न
प्रश्न 1.
जनसंख्या घनत्व क्या है?
उत्तर:
किसी स्थान में प्रति वर्ग कि०मी० में निवास करने वाले व्यक्तियों की संख्या जनसंख्या घनत्व कहलाती है।
प्रश्न 2.
अशोधित जन्म-दर क्या हैं?
उत्तर:
किसी क्षेत्र में प्रति वर्ष हजार व्यक्तियों में जीवित जन्म लेने वाले बच्चों की संख्या को अशोधित जन्म-दर कहा जाता है।
प्रश्न 3.
अशोधित मृत्यु-दर क्या हैं?
उत्तर:
एक वर्ष में प्रति हजार जनसंख्या के अनुपात में मरने वाले व्यक्तियों की संख्या को अशोधित मृत्यु-दर कहा जाता है।

प्रश्न 4.
प्रजननशीलता के चार निर्धारक तत्त्व कौन-से है?
उत्तर:
- जैव कारक
- जनांकिकीय कारक
- सामाजिक-सांस्कृतिक कारक
- आर्थिक कारक।
प्रश्न 5.
उद्गम स्थान किसे कहते हैं?
उत्तर:
जब लोग एक-स्थान से दूसरे स्थान पर जाते हैं तो वह स्थान जहाँ से लोग गमन करते हैं, उद्गम स्थान कहलाता है।
प्रश्न 6.
गंतव्य स्थान किसे कहते हैं?
उत्तर:
जिस स्थान पर लोग आगमन करते हैं वह गंतव्य स्थान कहलाता है।
प्रश्न 7.
विश्व के उच्च जनसंख्या घनत्व वाले दो क्षेत्रों के नाम लिखें।
उत्तर:
- पश्चिमी यूरोप
- संयुक्त राज्य अमेरिका तथा कनाडा के पूर्वी भाग।
प्रश्न 8.
जनसंख्या वृद्धि किसे कहते हैं?
उत्तर:
किसी क्षेत्र विशेष में लोगों की संख्या में, एक निश्चित समय के भीतर होने वाले परिवर्तन वृद्धि को जनसंख्या वृद्धि कहते हैं।
प्रश्न 9.
जनसंख्या के वितरण को प्रभावित करने वाले प्राकृतिक कारक बताएँ।
उत्तर:
धरातलीय स्वरूप, जलवायु, मृदा, प्राकृतिक वनस्पति।
प्रश्न 10.
जनसंख्या में ऋणात्मक वृद्धि कब होती है?
उत्तर:
जब जन्म-दर, मृत्यु-दर से कम हो या लोग विदेशों में जाकर बस जाते हैं तो जनसंख्या में ऋणात्मक वृद्धि होती है।
प्रश्न 11.
अशोधित मृत्यु-दर की गणना किस प्रकार की जाती है?
उत्तर:

प्रश्न 12.
जनसंख्या स्थानान्तरण क्या है?
उत्तर:
जनसंख्या के एक स्थान से दूसरे स्थान पर प्रवसन होने को स्थानान्तरण कहते हैं। जन्म-दर तथा मृत्यु-दर की भाँति स्थानान्तरण भी जनसंख्या परिवर्तनशीलता का मुख्य निर्धारक है। स्थानान्तरण से किसी क्षेत्र की जनसंख्या बढ़ती या कम होती है।
प्रश्न 13.
जनांकिकीय संक्रमण क्या है?
उत्तर:
मनुष्य के साथ जनसंख्या से होने वाले कृत्रिम परिवर्तन को जनांकिकीय संक्रमण कहते हैं। यह जनसंख्या के विकास की अवस्था है। जनसंख्या के इस विकास चक्र में सामान्यतया पाँच अवस्थाएँ होती हैं। इन अवस्थाओं को जनसंख्या चक्र भी कहते हैं।
प्रश्न 14.
मानसून एशिया में सघन जनसंख्या पाए जाने के कारण बताइए।
उत्तर:
मानसून एशिया में नदी-घाटियों, उपजाऊ मैदानों, अनुकूल जलवायु व लम्बे वर्धनकाल के कारण कृषि अधिक होती है; जैसे यहाँ पर चावल की तीन-तीन फसलें उगाई जाती हैं। नगरीकरण तथा औद्योगिकीकरण से यहाँ पर सघन जनसंख्या पाई जाती है।

प्रश्न 15.
विश्व में उच्च अथवा सघन जनसंख्या वाले मुख्य क्षेत्रों के नाम लिखें।
उत्तर:
जिन क्षेत्रों में जनसंख्या का घनत्व 200 व्यक्ति प्रति वर्ग कि०मी० से अधिक है, वे क्षेत्र उच्च घनत्व वाले क्षेत्र अथवा प्रदेश कहलाते हैं; जैसे-
- मानसून एशिया
- पश्चिमी यूरोप
- संयुक्त राज्य अमेरिका तथा कनाडा के पूर्वी भाग।

प्रश्न 16.
उत्प्रवास किसे कहते हैं?
उत्तर:
उत्प्रवास के द्वारा मनुष्य अपने प्रदेश से दूसरे स्थान को जाते हैं; जैसे यूरोप के मनुष्य उत्तरी अमेरिका, दक्षिणी अमेरिका तथा ऑस्ट्रेलिया आदि गए। जिन प्रदेशों में कोई भौतिक प्रकार का कष्ट; जैसे जलवायु, बाढ़, सूखा अथवा जीवन निर्वाह की अन्य कठिनाइयाँ अथवा सामाजिक या आर्थिक कठिनाई उत्पन्न होती हों, उन स्थानों से मनुष्य बाहर की ओर स्थानान्तरण करने लगते हैं।
प्रश्न 17.
जन्म-दर और जनसंख्या की वृद्धि दर में क्या अंतर हैं?
उत्तर:
जन्म-दर और जनसंख्या की वृद्धि दर में निम्नलिखित अंतर हैं-
| जन्म-दर | जनसंख्या वृद्धि दर |
| 1. किसी देश में एक वर्ष में प्रति हजार व्यक्तियों पर जन्म लेने वाले बच्चों की संख्या जन्म-दर कहलाती है। | 1. दो समयावधियों के बीच होने वाले जनसंख्या परिवर्तन को जनसंख्या वृद्धि दर कहा जाता है। |
| 2. यह दर प्रति हजार व्यक्ति होती है। | 2. यह दर प्रतिशत में होती है। |
प्रश्न 18.
जनसंख्या की प्राकृतिक वृद्धि तथा वास्तविक वृद्धि में अंतर स्पष्ट करें।
उत्तर:
जनसंख्या की प्राकृतिक वृद्धि तथा वास्तविक वृद्धि में निम्नलिखित अंतर हैं-
| प्राकृतिक वृद्धि | वास्तबिक वृद्धि |
| दो समय बिंदुओं के बीच प्राकृतिक तौर पर होने वाले जन्म-दर तथा मृत्यु-दर के अंतर को प्राकृतिक वृद्धि कहते हैं। | वास्तविक वृद्धि में जन्म-दर व मृत्यु-दर के साथ-साथ प्रवास व आप्रवास की भी गणना की जाती है। |
प्रश्न 19.
जनसंख्या की प्राकृतिक तथा प्रवासी वृद्धि में अंतर बताइए।
उत्तर:
जनसंख्या की प्राकृतिक तथा प्रवासी वृद्धि में निम्नलिखित अंतर हैं-
| प्राकृतिक वृद्धि | प्रवासी वृद्धि |
| 1. जन्म-दर में से मृत्यु-दर घटाने से प्राकृतिक वृद्धि प्राप्त होती है। | 1. जब किसी देश से लोग आकर बस जाएँ तो यह प्रवासी वृद्धि होती है.। |
| 2. इसका देश की कुल जनसंख्या पर प्रभाव पड़ता है। | 2. इसका देश की कुल जनसंख्या पर विशेष प्रभाव नहीं पड़ता। |
प्रश्न 20.
प्रवास एवं दिक् परिवर्तन में अंतर स्पष्ट करें।
उत्तर:
प्रवास एवं दिक् परिवर्तन में निम्नलिखित अंतर हैं-
| प्रवास | दिक् परिवर्तन |
| 1. जनसंख्या के एक स्थान से दूसरे स्थान पर जाकर बसने को प्रवास कहते हैं। | 1. किसी नगर तथा उसके पृष्ठ प्रदेश में स्थित गांवों के लोगों का स्थानांतरण दिक परिवर्तन कहलाता है। |
| 2. यह स्थायी होता है। | 2. यह अस्थायी होता है। |
प्रश्न 21.
अंतःराज्यीय प्रवास तथा अंतर्राज्यीय प्रवास में क्या अंतर हैं?
उत्तर:
अंतःराज्यीय प्रवास तथा अंतर्राज्यीय प्रवास में निम्नलिखित अंतर हैं-
| अंतःराज्यीय प्रवास | अंतर्राज्यीय प्रवास |
| 1. अपने ही राज्य में व्यक्तियों के स्थानांतरण को अंतःराज्यीय प्रवास कहते हैं। | 1. एक राज्य से दूसरे राज्य में व्यक्तियों के स्थानांतरण को अंतर्राज्यीय प्रवास कहते हैं। |
| 2. यह स्थानांतरण अधिक होता है। | 2. यह अपेक्षाकृत कम होता है। |
प्रश्न 22.
उत्प्रवास तथा आप्रवास में क्या अंतर है?
उत्तर:
उत्प्रवास तथा आप्रवास में निम्नलिखित अंतर हैं-
| उत्प्रवास | आप्रवास |
| 1. जब किसी प्रदेश के निवासी दूसरे प्रदेश में जाते हैं तो उसे उत्प्रवास कहते हैं। | 1. जब दूसरे प्रदेशों के निवासी किसी प्रदेश में आकर निवास करते हैं तो उसे आप्रवास कहते हैं। |
| 2. इससे मूल प्रदेश की जनसंख्या घटती है। | 2. इससे किसी प्रदेश की जनसंख्या में वृद्धि होती है। |
| 3. अधिक जनसंख्या वाले क्षेत्रों से उत्प्रवास होता है। | 3. कम जनसंख्या के क्षेत्रों की ओर आप्रवास होता है। |
प्रश्न 23.
विश्व के विरल जनसंख्या वाले तथा जन विहीन प्रदेशों के नाम लिखें।
उत्तर:
- उष्ण मरुस्थल-सहारा, कालाहारी, अटाकामा, पश्चिमी ऑस्ट्रेलिया, अरब तथा थार।
- अति शीत क्षेत्र-कनाडा, साइबेरिया का उत्तरी भाग, ग्रीनलैंड तथा अंटार्कटिक महाद्वीप।
- ठंडे मरुस्थल व उच्च पर्वतीय प्रदेश मध्य एशिया, गोबी मरुस्थल, राकीज, एंडीज व हिमालय पर्वत।
- विषुवत् रेखीय क्षेत्र-अमेजन तथा जायरे बेसिन।
प्रश्न 24.
प्रवास को प्रभावित करने वाले अपकर्ष व प्रतिकर्ष कारक क्या हैं?
उत्तर:
अपकर्ष कारक-नगरीय सुविधाओं तथा आर्थिक परिस्थितियों के कारण जब. लोग नगरों की ओर प्रवास करते हैं तो इसे अपकर्ष कारक (Pull Factors) कहा जाता है। अपकर्ष कारक के कारण लोग गन्तव्य स्थान को आकर्षक बनाते हैं।
प्रतिकर्ष कारक-जब लोग जीविका के साधन उपलब्ध न होने के कारण गरीबी तथा बेरोज़गारी के कारण नगरों की ओर प्रवास करते हैं तो इसे प्रतिकर्ष कारक (Push Factors) कहा जाता है। प्रतिकर्ष कारक के कारण लोग अपने उद्गम स्थान से दूसरे स्थान की ओर जाते हैं।
लघूत्तरात्मक प्रश्न
प्रश्न 1.
प्रवास क्या होता है? अस्थायी प्रवास के विभिन्न रूपों का वर्णन कीजिए।
उत्तर:
जनसंख्या का एक निवास स्थल से दूसरे निवास स्थल तक किसी भी कारणवश संचलन या गतिशीलता प्रवास कहलाता है। संयुक्त राष्ट्र संघ (UNO) के अनुसार, “प्रवास आवास परिवर्तन युक्त जनसंख्या की गतिशीलता को इंगित करता है।”
स्थानांतरण विभिन्न प्रकार का होता है। प्रवास को दूरी, अवधि, मात्रा, दिशा आदि के आधार पर कई भागों में विभाजित किया जा सकता है। प्रवास स्थायी और अस्थायी भी हो सकता है।
अस्थायी प्रवास के विभिन्न रूप-अस्थायी प्रवास को विभिन्न प्रकार से व्यक्त किया गया है। कुछ महत्त्वपूर्ण अस्थायी प्रवास निम्नलिखित हैं-
1. दैनिक प्रवास-नगरों में विविध प्रकार की सुविधाओं के उपलब्ध होने के कारण लोग प्रायः प्रतिदिन गांवों से नगरों में आते हैं और सायंकाल लौट जाते हैं। यदि व्यक्ति एक सप्ताह तक नगर में रुककर वापस लौट आता है तो इसे दैनिक या साप्ताहिक प्रवास कहते हैं।
2. मौसमी प्रवास-शीत ऋतु में पर्वतीय लोग सर्दी से बचने के लिए घाटियों में आ जाते हैं। इसी प्रकार गन्ने की पेराई के काल में मजदूर चीनी मिलों में काम करते हैं और पेराई बंद होने पर घरों में वापस चले जाते हैं। यह प्रवास मौसमी होता है। टुंड्रा, टैगा व स्टैप्स प्रदेश के निवासी मौसमी प्रवास करते हैं।
प्रश्न 2.
निम्नलिखित पर संक्षिप्त टिप्पणी लिखिए (क) विश्व जनसंख्या की दुगुना होने की अवधि, (ख) जनांकिकीय संक्रमण।।
उत्तर:
(क) विश्व जनसंख्या की दुगुना होने की अवधि किसी भी देश की जनसंख्या के दुगुना होने की अवधि का संबंध जनसंख्या की प्रति वर्ष प्रतिशत वृद्धि दर से है। वृद्धि दर जितनी कम होगी जनसंख्या के दुगुना होने का समय उतना ही अधिक होगा। इसके विपरीत यदि वृद्धि दर अधिक है तो जनसंख्या के दुगुना होने में कम समय लगेगा। इसे निम्नलिखित सूत्र द्वारा निकाला जा सकता है

विकसित देशों में जनसंख्या के दुगुना होने का समय अधिक है जबकि विकासशील देशों की जनसंख्या के दुगुना होने का समय अपेक्षाकृत बहुत कम है।
(ख) जनांकिकीय संक्रमण जनसंख्या का विकास कुछ क्रमिक अवस्थाओं में होता है। जैसे-जैसे किसी देश का आर्थिक विकास होता जाता है उसमें जनसंख्या परिवर्तन भी होते रहते हैं। आर्थिक विकास की अवस्था में स्वास्थ्य सुविधाओं के प्रसार से पहले मृत्यु-दर में कमी आती है। तत्पश्चात् जन्म-दर भी घटनी प्रारंभ हो जाती है जिसके फलस्वरूप जनसंख्या वृद्धि दर कम हो जाती है। इस प्रकार की कमी पहले मृत्यु-दर में जिसके कारण वृद्धि दरें बढ़ीं। फिर जन्म-दरों में जिससे जन्म-दरें और मृत्यु-दरें लगभग बराबर हो गईं, जिसके परिणामस्वरूप बहुत कम या शून्य वृद्धि दर हुई। इस स्थिति को जनांकिकीय संक्रमण कहते हैं।
प्रश्न 3.
जनसंख्या परिवर्तन तथा आर्थिक विकास में क्या सम्बन्ध है? व्याख्या कीजिए। अथवा “विकास सबसे उत्तम गर्भ निरोधक है।” वर्णन कीजिए।
उत्तर:
विश्व जनसंख्या का विकास बढ़ती हुई जनसंख्या के विकास दर का प्रतिपादक है। विकसित देशों में पहले मृत्यु-दर में कमी हुई। फिर जन्म-दर में भी कमी हुई जिससे जनसंख्या वृद्धि दर में भी कमी आई। यह प्रक्रिया जनसंख्या परिवर्तन कहलाती है। जनसंख्या के बढ़ने के साथ उनकी माँगें और आवश्यकताएँ भी बढ़ जाती हैं। जनसंख्या बढ़ने से राष्ट्रीय आय बढ़ जाती है। राष्ट्रीय आय के घटने-बढ़ने से प्रति व्यक्ति आय और उसी के अनुरूप जीवन स्तर घटता-बढ़ता है।
कम आय से वस्तुओं की माँग पर प्रतिकूल असर पड़ता है, जिससे विकास अवरुद्ध हो जाता है। यदि जनसंख्या इष्टतम (Optimum) है तो संसाधनों का उचित उपयोग होगा और जीवन स्तर बढ़ेगा। विकासशील देशों की बढ़ती जनसंख्या के कारण आज वे गरीबी, कुपोषण और बेरोज़गारी जैसी समस्याओं से जूझ रहे हैं। आर्थिक विकास के साथ जनसंख्या की वृद्धि कम होती चली जाती है। इसलिए कहा गया है कि विकास सबसे उत्तम गर्भ निरोधक है।

प्रश्न 4.
जनसंख्या के अंकगणितीय घनत्व और कायिक घनत्व में अंतर स्पष्ट करें।
उत्तर:
जनसंख्या के अंकगणितीय घनत्व और कायिक घनत्व में निम्नलिखित अंतर हैं-
| अंकगणितीय घनत्व | कायिक घनत्व |
| 1. किसी देश की कुल जनसंख्या तथा कुल क्षेत्रफल के अनुपात को अंकगणितीय घनत्व कहते हैं। | 1. किसी देश की कुल जनसंख्या तथा कुल कृषि-भूमि के अनुपात को कायिक घनत्व कहते हैं। |
| 2. बेशक भूगोलवेत्ता इसका प्रयोग करते हैं, फिर भी इस ढंग की अपनी त्रुटि है- ऋणात्मक क्षेत्र भी इस ढंग में धनात्मक दर्शाए जाते हैं। | 2. इस ढंग में कृषि अयोग्य भूमि को कुल भूमि में से घटा देते हैं। अतः इस ढंग द्वारा कृषि भूमि पर जन-दबाव का ठीक अनुमान लगता है। |
| 3. इस ढंग से लोगों की संपन्नता का कोई पता नहीं लगता। | 3. इस ढंग से लोगों क् संपन्नता का कुछ अनुमान लगाया जा सकता है। |
प्रश्न 5.
ईसा से 8000 वर्ष पूर्व से वर्तमान तक विश्व की जनसंख्या किस प्रकार बढ़ी है?
उत्तर:
ईसा से 8000 वर्ष पूर्व विश्व की जनसंख्या लगभग 0.8 करोड़ थी। लगभग 2000 वर्ष पूर्व ईसा मसीह के समय में जनसंख्या 30 करोड़ के लगभग थी। वर्ष 1830 तक यह 100 करोड़ तक पहुँच गई और तब से यह बहुत तेजी से बढ़ती आ रही है जो लगभग 160 वर्षों में 700 करोड़ से भी अधिक हो गई है। निम्नलिखित तालिका में विश्व की जनसंख्या वृद्धि को दर्शाया गया है
तालिका : विश्व की जनसंख्या में वृद्धि
| इन वर्षों के दौरान | विश्व जनसंख्या | इस संख्या तक पहुँचने के लिए लिया गया समय |
| आदिमानव से ईसा | 30 करोड़ | संपूर्ण मानव इतिहास के दौरान |
| 0-1500 ई० | 50 करोड़ | 1500 वर्ष |
| 1500-1850 ई० | 100 करोड़ | 350 वर्ष |
| 1850-1930 ई० | 200 करोड़ | 100 वर्ष |
| 1930-1960 ईం | 300 करोड़ | 30 वर्ष |
| 1960-1974 ई | 400 करोड़ | 14 वर्ष |
| 1974-1987 ई० | 500 करोड़ | 13 वर्ष |
| 1987-1999 ई० | 600 करोड़ से अधिक | 12 वर्ष |
| 1999-2011 ई० | लगभग 700 करोड़ | 12. वर्ष |
प्रश्न 6.
विश्व के अधिक घनत्व वाले प्रदेश कौन-कौन से हैं और क्यों?
उत्तर:
वे क्षेत्र जहाँ जनसंख्या का घनत्व 200 व्यक्ति प्रति वर्ग कि०मी० से अधिक है। इनके प्रमुख क्षेत्र हैं-
- पूर्वी एशिया तथा दक्षिणी एशिया।
- पश्चिमी यूरोप तथा उत्तर पूर्वी अमेरिका।
कारण-
- ऊष्ण आर्द्र व समशीतोष्ण जलवायु जनसंख्या को आकर्षित करती है।
- नदी घाटियों की उपजाऊ मिट्टी, जल-सिंचाई, समतल भूमि और चावल का अधिक उत्पादन, अधिक घनत्व में सहायक हैं।
- निर्माण उद्योगों का अधिक होना तथा समुद्री मार्गों के कारण व्यापार का अधिक उन्नत होना भी जनसंख्या के उच्च घनत्व का कारण है।
- मिश्रित कृषि का विकास, नगरीकरण के कारण बड़े-बड़े नगरों का विकास जनसंख्या को आकर्षित करता है।
- वैज्ञानिक तथा तकनीकी ज्ञान में अधिक वृद्धि जनसंख्या के उच्च घनत्व का प्रमुख कारक है।
प्रश्न 7.
विश्व के मध्यम घनत्व वाले प्रदेश कौन-कौन से हैं और क्यों?
उत्तर:
वे क्षेत्र जहाँ 25 से 200 व्यक्ति प्रति वर्ग कि०मी० तक घनत्व मिलता है। इसमें निम्नलिखित क्षेत्र हैं
- उत्तरी अमेरिका में प्रेयरीज का मध्य मैदान
- अफ्रीका का पश्चिमी भाग
- पूर्वी यूरोप और पूर्वी रूस
- पूर्वी ऑस्ट्रेलिया
- दक्षिणी अमेरिका में उत्तर:पूर्वी ब्राजील, मध्य चिली, मैक्सिको का पठार।
कारण –
- विस्तृत खेती-बाड़ी में आधुनिक मशीनों का प्रयोग किया जाता है।
- पर्वतीय व पठारी क्षेत्र के कारण जनसंख्या कम है।
प्रश्न 8.
विश्व में जनसंख्या का घनत्व असमान क्यों है?
उत्तर:
विश्व के सर्वाधिक जनसंख्या वाले देशों में विश्व की 60% से अधिक जनसंख्या रहती है और यह जनसंख्या विश्व के कुल क्षेत्रफल के लगभग 20% भाग पर रहती है। विश्व की 40% से भी कम जनसंख्या विश्व के लगभग 80% क्षेत्रफल पर निवास करती है। इस कारण विश्व में जनसंख्या का घनत्व असमान है। जनसंख्या की विशालता और इसके अत्याधिक ग्रामीण स्वरूप के अतिरिक्त नृ-जातीय विविधता, तीव्र वृद्धि दर और जनसंख्या का असमान वितरण अन्य पक्ष हैं जो देश की सामाजिक, आर्थिक विकास की प्रक्रिया और गति को धीमा कर रहे हैं।
प्रश्न 9.
विश्व में जनसंख्या के वितरण को प्रभावित करने वाले राजनीतिक कारक का वर्णन कीजिए।
उत्तर:
राजनीतिक कारक भी कुछ सीमा तक जनसंख्या के वितरण को प्रभावित करते हैं। सरकार की जनसंख्या नीति मानव के बसाव को अनुकूल तथा प्रतिकूल बना सकती है। रूस सरकार साइबेरिया में जनसंख्या वृद्धि को प्रोत्साहित करके उनको पारितोषिक देती है। फ्रांस में जनसंख्या वृद्धि के लिए करों में रियायतें दी जाती हैं, जबकि चीन व भारत में जनसंख्या की विस्फोटक स्थिति है। चीन में एक बच्चा होने के बाद सरकार ने दूसरे बच्चे के जन्म देने पर प्रतिबन्ध लगा रखा है। भारत में भी जनसंख्या को नियन्त्रित करने के प्रयास किए जा रहे हैं, लेकिन पिछले एक दशक से चीन की जनसंख्या में वृद्धि-दर निरन्तर अधिक है। वह दिन निकट ही है जब भारत की जनसंख्या विश्व में सबसे अधिक हो जाएगी।

प्रश्न 10.
प्रवास कितने प्रकार के होते हैं? वर्णन करें।
उत्तर:
प्रवास मुख्यतः दो प्रकार के होते हैं-
1. उत्प्रवास (Emigration) – उत्प्रवास के द्वारा मनुष्य अपने प्रदेश से दूसरे स्थान को जाते हैं। जैसे यूरोप के मनुष्य उत्तरी अमेरिका, दक्षिणी अमेरिका तथा ऑस्ट्रेलिया आदि गए। जिन प्रदेशों में कोई भौतिक प्रकार का कष्ट; जैसे जलवायु, बाढ़, सूखा अथवा जीवन निर्वाह की अन्य कठिनाइयाँ अथवा सामाजिक या आर्थिक कठिनाई उत्पन्न होती हों, उन स्थानों से मनुष्य बाहर की ओर स्थानान्तरण करने लगते हैं।
2. अप्रवास (Immigration)-अप्रवास के द्वारा बाहरी स्थानों से मनुष्य किसी प्रदेश या स्थान के अन्दर आते हैं। उदाहरण उत्तरी अमेरिका में ब्रिटेन, इटली, फ्रांस आदि देशों से मनुष्यों का प्रवास होता है। जिन देशों में जीविका निर्वाह की सुविधाएँ प्रचुर मात्रा में होती हैं, वे बाहर से मनुष्यों को अपनी ओर आकर्षित करते हैं। कभी-कभी आर्थिक या सामाजिक आवश्यकताओं के कारण भी बाहरी क्षेत्रों से प्रवास होता है।
प्रश्न 11.
जनसंख्या की वृद्धि-दर की प्रवृत्तियों का उल्लेख कीजिए।
अथवा
विश्व में जनसंख्या वृद्धि की प्रवृत्तियों का वर्णन कीजिए।
उत्तर:
जनसंख्या की वृद्धि-दर की प्रवृत्तियाँ निम्नलिखित हैं-
1. प्राकृतिक वृद्धि-दर (Natural Growth Rate) – दो समय बिन्दुओं में जन्म-दर और मृत्यु-दर में अन्तर से बढ़ने वाली जनसंख्या को उस क्षेत्र की प्राकृतिक वृद्धि-दर कहते हैं अर्थात् प्राकृतिक वृद्धि-दर = जन्म-दर – मृत्यु-दर।
2. वास्तविक वृद्धि-दर (Real Growth Rate) – इसमें जनसंख्या की जन्म-दर व मृत्यु-दर के साथ-साथ आप्रवास व अप्रवास की भी गणना की जाती है अर्थात् वास्तविक वृद्धि-दर = जन्म-दर – मृत्यु-दर + आप्रवासी – उत्प्रवासी।
3. धनात्मक वृद्धि-दर (Positive Growth Rate) – धनात्मक वृद्धि-दर तब होती है जब दो समय बिन्दुओं के बीच जन्म-दर, मृत्यु-दर से अधिक हो या अन्य देशों के लोग स्थायी रूप से उस देश में प्रवास कर जाएँ।
4. ऋणात्मक वृद्धि-दर (Negative Growth Rate) – यदि दो समय बिन्दुओं के बीच जनसंख्या कम हो जाए तो उसे ऋणात्मक वृद्धि-दर कहते हैं। यह तब होती है जब जन्म-दर मृत्यु-दर से कम हो जाए या लोग अन्य देशों में प्रवास कर जाएँ।
प्रश्न 12.
विश्व में न्यून (विरल) जनसंख्या वाले क्षेत्रों का वर्णन कीजिए।
उत्तर:
जिन क्षेत्रों में 1 से 2 व्यक्ति प्रति वर्ग किलोमीटर रहते हैं, उन्हें विरल जनसंख्या वाले प्रदेश कहते हैं। इनमें प्रमुख निम्नलिखित प्रदेश सम्मिलित हैं-
1. उष्ण मरुस्थल-सहारा, कालाहारी, अटाकामा, पश्चिमी ऑस्ट्रेलिया, अरब, थार तथा सोनोरैन मरुस्थल । इन क्षेत्रों में न्यून . वर्षा के कारण जल की कमी है और जनसंख्या विरल है।
2. अति-शीत क्षेत्र-ये ध्रुवीय क्षेत्र हैं, जिनमें कनाडा का उत्तरी भाग, ग्रीनलैंड, साइबेरिया का उत्तरी भाग तथा दक्षिणी ध्रुव के चारों ओर फैला हुआ अंटार्कटिक महाद्वीप सम्मिलित हैं। इन क्षेत्रों में तापमान कम है तथा फसलों के लिए वर्धनकाल छोटा है। अंटार्कटिक महाद्वीप तो बिल्कुल ही जनविहीन है।
3. विषुवत् रेखीय क्षेत्र इसमें दक्षिणी अमेरिका का अमेजन बेसिन तथा अफ्रीका का जायरे बेसिन सम्मिलित हैं। इन क्षेत्रों में वर्षा तथा तापमान दोनों ही अधिक हैं, जिससे घने वन उगते हैं, जिन्हें पार करना कठिन है। यह जलवायु मरुस्थल के स्वास्थ्य के लिए भी हानिकारक है।
प्रश्न 13.
विकसित तथा विकासशील देशों की जनांकिकीय प्रवृत्तियों में अंतर स्पष्ट कीजिए।
उत्तर:
विकसित और विकासशील देशों की जनांकिकीय प्रवृत्तियों में निम्नलिखित अंतर हैं-
| अभिलक्षण | विकसित देश | विकासशील देश |
| (1) वृद्धि दर | निम्न (0.6 प्रतिशत) | उच्च (2.1 प्रतिशत) |
| (2) द्विगुणन अवधि | उच्च (116 वर्ष) | निम्न (35 वर्ष) |
| (3) शिशु मृत्यु-दर | निम्न (5-25) | उच्च (50 – 100) |
| (4) साक्षरता | उच्च 95 प्रतिशत | निम्न 35-75 प्रतिशत |
| (5) औद्योगीकरण | उच्च | निम्न |
| (6) मुख्य जनसंख्या | नगरीय 75 प्रतिशत | ग्रामीण 54 प्रतिशत |
| (7) जीवन स्तर | उच्च | निम्न |
प्रश्न 14.
जनसंख्या घनत्व और जनसंख्या वितरण में क्या अंतर हैं?
उत्तर:
जनसंख्या घनत्व और जनसंख्या वितरण में निम्नलिखित अंतर हैं-
| जनसंख्या घनत्व | जनसंख्या वितरण |
| 1. किसी स्थान में प्रति वर्ग कि०मी० में निवास करने वाले व्यक्तियों की संख्या है। | 1. किसी स्थान की कुल जनसंख्या ही वहाँ का वितरण है। |
| 2. जनसंख्या घनत्व एक अनुपात है। | 2. जनसंख्या वितरण की प्रकृति स्थितिगत है। |
| 3. जनसंख्या वितरण को उसके घनत्व द्वारा अधिक सुचारु ढंग से प्रस्तुत किया जाता है। | 3. जनसंख्या वितरण का प्रारूप क्षेत्रीय होता है। |
| 4. घनत्व को प्रति वर्ग कि०मी० में व्यक्त करते हैं; जैसे भारत की जनसंख्या का घनत्व 382 व्यक्ति प्रति वर्ग कि०मी० है। | 4. वितरण को व्यक्त करने के लिए कोई इकाई नहीं है। |
प्रश्न 15.
जनसंख्या के वितरण को प्रभावित करने वाले भौतिक कारकों का वर्णन कीजिए।
उत्तर:
भौतिक कारक-किसी भी देश अथवा प्रदेश की जनसंख्या के वितरण को निम्नलिखित भौतिक कारक प्रभावित करते हैं-
1. धरातल-जनसंख्या के वितरण को प्रभावित करने में धरातल की विभिन्नता सबसे महत्त्वपूर्ण कारक है। ऊबड़-खाबड़ तथा ऊँचे पर्वतीय प्रदेशों में जनसंख्या कम आकर्षित होती है। इन प्रदेशों में जनसंख्या विरल पाई जाती है, क्योंकि यहाँ पर मानव निवास की अनुकूल परिस्थितियाँ उपलब्ध नहीं होती, कृषि के लिए उपजाऊ मिट्टी का अभाव होता है, यातायात के साधनों का विकास आसानी से नहीं हो पाता, कृषि फसलों के लिए वर्धनकाल (Growing Period) छोटा होता है तथा जलवायु कठोर होती है।
2. जलवायु अनुकूल तथा आरामदेय जलवायु में कृषि, उद्योग तथा परिवहन एवं व्यापार का विकास अधिक आसानी से होता है। विश्व में मध्य अक्षांश का क्षेत्र (शीतोष्ण कटिबन्धीय क्षेत्र) जलवायु की दृष्टि से अनुकूल है। इसलिए विश्व की अधिकांश जनसंख्या इन्हीं प्रदेशों में निवास करती है। इसके विपरीत अत्यधिक शीत प्रदेशों में जनसंख्या विरल पाई जाती है। इसी प्रकार शुष्क मरुस्थली प्रदेशों की जलवायु ग्रीष्म ऋतु में झुलसाने वाली तथा शीत ऋतु में ठिठुराने वाली होती है। यही कारण है कि विश्व के मरुस्थलों; जैसे सहारा, थार, कालाहारी, अटाकामा तथा अरब के मरुस्थलों में जनसंख्या विरल है।
3. मृदा मनुष्य की पहली आवश्यकता है भोजन। भोजन हमें मिट्टी से मिलता है। मिट्टी में ही विभिन्न कृषि उपजें पैदा होती विश्व के जिन क्षेत्रों में उपजाऊ मिट्टी है, वहाँ जनसंख्या अधिक पाई जाती है। भारत में गंगा-सतलुज के मैदान, संयुक्त राज्य अमेरिका में मिसीसिपी के मैदान, पाकिस्तान में सिन्धु के मैदान, मिस्र में नील नदी के मैदान आदि में उपजाऊ मिट्टी की परतें हैं, जिससे अधिक लोग वहाँ आकर बस गए हैं।
4. वनस्पति-वनस्पति भी जनसंख्या के वितरण को प्रभावित करती है। उदाहरणार्थ, भूमध्य-रेखीय क्षेत्रों में सघन वनस्पति (सदाबहारी वनों) के कारण यातायात के साधनों का विकास कम हुआ है। आर्द्र जलवायु के कारण मानव-जीवन अनेक रोगों से ग्रसित रहता है, इसलिए यहाँ की जनसंख्या विरल है। इसके विपरीत जिन क्षेत्रों में वनस्पति आर्थिक उपयोग वाली होती है, वहाँ मानव लकड़ी से सम्बन्धित अनेक व्यवसाय आरम्भ हो जाते हैं; जैसे टैगा के वनों का आर्थिक महत्त्व है इसलिए वहाँ जनसंख्या अधिक पाई जाती है। वनस्पति विहीन क्षेत्रों (मरुस्थलों) में भी जनसंख्या विरल है।
5. खनिज सम्पदा-जिन क्षेत्रों में खनिज पदार्थों के भण्डार मिलते हैं, वहाँ खनन व्यवसाय तथा उद्योगों की स्थापना के कारण बेत होती है। ब्रिटेन में पेनाइन क्षेत्र, जर्मनी में रूर क्षेत्र, संयुक्त राज्य अमेरिका में आप्लेशियन क्षेत्र, रूस के डोलेत्स बेसिन तथा भारत के छोटा नागपुर के पठार में जनसंख्या का केन्द्रीयकरण वहाँ की खनिज सम्पदा की ही देन है।

प्रश्न 16.
जनसंख्या के वितरण को प्रभावित करने वाले मानवीय कारकों का वर्णन कीजिए।
उत्तर:
जनसंख्या के वितरण को प्रभावित करने वाले मानवीय कारक निम्नलिखित हैं-
1. कृषि विश्व में जो क्षेत्र कृषि की दृष्टि से अनुकूल हैं, वहाँ जनसंख्या का अधिक आकर्षण होता है। वहाँ लोग प्राचीन समय से ही अधिक संख्या में निवास करते आ रहे हैं। प्रेयरीज तथा स्टेपीज प्रदेश कृषि के लिए उपयुक्त हैं, इसलिए वहाँ जनसंख्या का घनत्व अधिक है।
2. नगरीकरण-बीसवीं शताब्दी में नगरीकरण की प्रवृत्ति के कारण नगरों की जनसंख्या में निरन्तर वृद्धि हो रही है। नगरों में रोज़गार, शिक्षा, स्वास्थ्य, परिवहन, व्यापार आदि की अधिक सुविधाएँ सुलभ हैं इसलिए जनसंख्या का जमघट नगरों में अधिक देखने को मिलता है। न्यूयॉर्क, लन्दन, मास्को, बीजिंग, शंघाई, सिडनी, दिल्ली, कोलकाता, मुम्बई आदि नगरों में जनसंख्या में तीव्र वृद्धि हो रही है।
3. औद्योगिकीकरण-जिन क्षेत्रों में औद्योगिक विकास तीव्र हुआ है, वहाँ जनसंख्या का आकर्षण बढ़ा है। जापान, ब्रिटेन, संयुक्त राज्य अमेरिका का उत्तर:पूर्वी भाग, जर्मनी का रूर क्षेत्र, यूरोपीय देशों तथा भारत में पिछले दो दशकों से दिल्ली, मुम्बई तथा हुगली क्षेत्र में औद्योगिक विकास के कारण जनसंख्या में तीव्र वृद्धि हुई है।
4. परिवहन-परिवहन की सुविधाओं का भी जनसंख्या के वितरण पर अत्यधिक प्रभाव पड़ता है। जिन क्षेत्रों में यातायात की अधिक सुविधाएँ हैं, वहाँ जनसंख्या का अधिक आकर्षण होता है। महासागरीय यातायात के विकास के कारण कई बन्दरगाह विश्व के बड़े नगर बन चुके हैं। सिंगापुर, शंघाई, सिडनी, न्यूयॉर्क आदि नगर बन्दरगाहों के रूप में विकसित हुए थे, लेकिन आज इन नगरों में रेल, सड़क तथा वायु यातायात की सभी सुविधाएँ उपलब्ध हैं।
दीर्घ-उत्तरात्मक प्रश्न
प्रश्न 1.
जनसंख्या घनत्व क्या है? विश्व में जनसंख्या घनत्व के वितरण का वर्णन कीजिए।
अथवा
विश्व में न्यून या विरल जनसंख्या घनत्व वाले क्षेत्रों का वर्णन कीजिए।
अथवा
विश्व में सघन जनसंख्या वाले क्षेत्रों का वर्णन कीजिए।
अथवा
संसार के सघन और विरल जनसंख्या वाले क्षेत्रों का उल्लेख कीजिए।
उत्तर:
किसी भी प्रदेश की जनसंख्या और उस प्रदेश की भूमि के क्षेत्रफल के पारस्परिक अनुपात को जनसंख्या का घनत्व कहते हैं। इससे किसी प्रदेश के लोगों की सघनता का पता चलता है। यह जनसंख्या के विश्लेषणात्मक अध्ययन करने का महत्त्वपूर्ण माप है। इसे प्रति इकाई क्षेत्रफल पर व्यक्तियों की संख्या द्वारा व्यक्त किया जाता है। घनत्व इस प्रदेश की उन्नति और भावी विकास का अनुमान लगाने का मुख्य आधार होता है। इसका मुख्य लक्ष्य किसी क्षेत्र के संसाधनों पर जनसंख्या दबाव ज्ञात करना होता है। इसे निम्नलिखित रूपों में परिभाषित किया जाता है
1. गणितीय घनत्व (Arithmetic Density) किसी देश अथवा प्रदेश की कुल जनसंख्या तथा उसके कुल क्षेत्रफल के अनुपात को वहाँ की जनसंख्या का गणितीय घनत्व कहा जाता है। यह जनसंख्या तथा क्षेत्रफल के बीच एक साधारण अनुपात है। इसे निम्नलिखित सूत्र से ज्ञात किया जाता है

उदाहरण के लिए, जनसंख्या 376.80 करोड़ व क्षेत्रफल 440 लाख वर्ग कि०मी० है, तो जनसंख्या का घनत्व निम्नलिखित प्रकार से ज्ञात किया जा सकता है
गणितीय घनत्व = \(\frac { 37680 }{ 440 }\)
= 85.64 या 86 व्यक्ति प्रति वर्ग कि०मी०
यह जनसंख्या घनत्व का सबसे सरल रूप है, परन्तु इसमें कई त्रुटियाँ हैं। जैसे इससे जनसंख्या निवास तथा जीवन-स्तर का सही अनुमान नहीं लग पाता। लेकिन उपरोक्त त्रुटियों के बावजूद यह विभिन्न देशों की जनसंख्या विशेषताओं की तुलना करने की एक अच्छी विधि है।
2. कायिक घनत्व (Physiological Density)-इसे प्रति वर्ग किलोमीटर कृषि भूमि (Cultivated Land) पर कुल निवास करने वाली जनसंख्या के अनुपात में व्यक्त किया जाता है। किसी देश या प्रदेश की कुल जनसंख्या वहाँ की कुल कृषि भूमि (Cultivated Land) के अनुपात को कायिक घनत्व कहते हैं। इसे निम्नलिखित सूत्र से ज्ञात किया जाता है-

उदाहरण के लिए, यदि कुल कृषि भूमि 14.26 लाख वर्ग कि०मी० व जनसंख्या 10270 लाख है तो जनसंख्या का कायिक घनत्व निम्नलिखित प्रकार से होगा
कायिक घनत्व = \(\frac { 10270 }{ 14.26 }\) = 720 व्यक्ति प्रति वर्ग कि०मी०
कायिक घनत्व द्वारा यह पता चलता है कि कृषि भूमि के प्रति वर्ग कि०मी० पर कितने व्यक्ति निर्भर हैं। कृषि प्रधान विकासशील देशों के लिए इस घनत्व का विशेष महत्त्व है।
3. आर्थिक घनत्व (Economic Density) इससे उस देश या प्रदेश के साधनों की उत्पादन क्षमता (Productive Capacity) तथा उस प्रदेश में निवास करने वाली जनसंख्या के अनुपात को लिया जाता है।

4. कृषि घनत्व (Agriculture Density) इसमें उस देश या प्रदेश की कृषि की जाने वाली भूमि के क्षेत्रफल (Cultivated Area) तथा उसमें निवास करने वाली कृषक जनसंख्या (Agricultural Population) के अनुपात को लिया जाता है।

5. पोषण घनत्व (Nutrition Density)-इसमें खेती की भोज्य फसलों (Food Crops) का क्षेत्रफल तथा उस प्रदेश की कुल जनसंख्या (Total Population) को लिया जाता है।

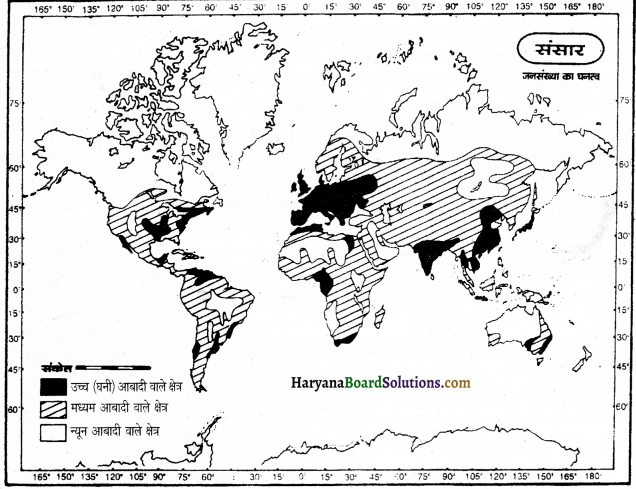
जनसंख्या का विश्व वितरण-विश्व की जनसंख्या के वितरण पर यदि नजर डालें तो इसके आँकड़े चौंकाने वाले हैं। जनसंख्या का वितरण अत्यधिक असमान एवं विषम है। विश्व की लगभग 90 प्रतिशत आबादी केवल एक चौथाई भू-भाग पर निवास करती है और शेष 10 प्रतिशत जनसंख्या तीन-चौथाई क्षेत्रफल घेरे हुए है। सन् 2001 में विश्व की अनुमानित जनसंख्या 605 करोड़ थी, जोकि सन् 2011 में बढ़कर 693 करोड़ से अधिक हो चुकी है। उत्तरी गोलार्द्ध में विश्व की 90% जनसंख्या रहती है तथा दक्षिणी गोलार्द्ध में 10% से भी कम जनसंख्या रहती है। विश्व का लगभग 33% भाग जनविहीन है।
जनसंख्या के वितरण के आधार पर विश्व को तीन प्रदेशों में वर्गीकृत किया जा सकता है-
1. विरल जनसंख्या अथवा निम्न घनत्व वाले क्षेत्र-विश्व में कुछ ऐसे भी क्षेत्र हैं जहाँ जनसंख्या का घनत्व 1 से 2 व्यक्ति प्रति वर्ग कि०मी० है। ऐसे क्षेत्रों को विरल जनसंख्या के क्षेत्र कहते हैं। विरल जनसंख्या वाले क्षेत्रों में कुल विश्व के क्षेत्रफल का तीन-चौथाई भाग आता है। इस प्रकार के प्रदेश निम्नलिखित हैं-
(1) उष्ण कटिबन्धीय क्षेत्र-उष्ण मरुस्थलीय भू-भाग अधिकांश महाद्वीपों के पश्चिमी भागों में स्थित हैं। यहाँ जनसंख्या का घनत्व 1 व्यक्ति से 2 व्यक्ति प्रति वर्ग कि०मी० है। ऐसे क्षेत्रों में वर्षा की न्यूनता तथा जल का अभाव है। यहाँ वर्षा के अभाव में केवल काँटेदार झाड़ियाँ ही उगती हैं। इन क्षेत्रों में कृषि बहुत कम होती है। यहाँ निवास करने वाले लोगों का मुख्य व्यवसाय भेड़-बकरी तथा ऊँट पालना है। इस प्रकार के मरुस्थलों में सहारा, कालाहारी, अटाकामा, थार, पश्चिमी ऑस्ट्रेलिया तथा अरब का मरुस्थल प्रमुख हैं।
(2) अति-शीत प्रदेश-इन प्रदेशों में ध्रुवीय प्रदेश सम्मिलित हैं। यहाँ की जलवायु अत्यन्त शीतल होती है और हर समय अधिकतर बर्फ जमी रहती है। यहाँ वर्धनकाल इतना छोटा होता है कि कोई भी फसल उगाना कठिन है। इस प्रकार के प्रदेशों में लोगों का मुख्य व्यवसाय आखेट करना तथा मछली पकड़ना है। इनमें ग्रीनलैण्ड, साइबेरिया का उत्तरी भाग, कनाडा का उत्तरी भाग, अलास्का तथा दक्षिणी ध्रुव का अंटार्कटिक महाद्वीप निर्जन हैं। ऐसे क्षेत्रों में 10 महीने तापमान हिमांक बिन्दु से नीचे ही रहता है। अधिकांश चलवासी चरवाहे हैं जो रेडियर पालते हैं और सील तथा व्हेल का शिकार करते हैं।
(3) उच्च पर्वतीय प्रदेश मध्य एशिया चारों ओर से सागरीय प्रभाव से वंचित शुष्क तथा अनाकर्षक प्रदेश हैं। पर्वतीय एवं पठारी होने के कारण मिट्टी की गहराई कम है तथा कृषि फसलें न के बराबर हैं या कहीं-कहीं साल-भर में केवल एक ही फसल उगाई जाती है। 4000 मीटर से अधिक ऊँचाई वाले पवर्तीय भागों में तो वायु का दबाव कम हो जाता है, जिससे साँस लेना भी कठिन हो जाता है। उत्तरी अमेरिका में रॉकीज पर्वत, दक्षिणी अमेरिका में एण्डीज़ तथा भारत में महान हिमालय तथा चीन के दक्षिण-पश्चिमी भाग में इस प्रकार के उच्च पर्वतीय प्रदेश हैं।
(4) विषुवत रेखीय क्षेत्र-यह प्रदेश अत्यधिक वर्षा तथा साल-भर ऊँचा तापक्रम होने के कारण मानवं बसाव की दृष्टि से अनुकूल नहीं है। यहाँ जनसंख्या विरल है। चारों ओर घने जंगल तथा वन्य प्राणियों का साम्राज्य है। यहाँ जलवायु उमस वाली है तथा विभिन्न प्रकार के कीटाणु तथा जहरीले कीड़े-मकौड़े यहाँ देखने को मिलते हैं। इनमें दक्षिणी अमेरिका का अमेज़न बेसिन, अफ्रीका का जायरे बेसिन आदि सम्मिलित हैं।
2. मध्यम जनसंख्या और घनत्व वाले क्षेत्र-विश्व के जिन भागों में जनसंख्या का घनत्व 11 से 50 व्यक्ति प्रति वर्ग कि०मी० है, उन्हें मध्यम या साधारण जनसंख्या वाले क्षेत्र में रखा जा सकता है। ये प्रदेश सभी महाद्वीपों में पाए जाते हैं।
- एशिया-म्यांमार, दक्षिणी भारत, पश्चिमी चीन, थाईलैण्ड, कम्बोडिया आदि हैं।
- यूरोप डेनमार्क, स्वीडन, नॉर्वे, लिथुआनिया, बाल्टिक गणराज्य तथा रूस के उत्तर-पश्चिमी भाग।
- अमेरिका-संयुक्त राज्य अमेरिका का पश्चिमी तथा मध्यवर्ती भाग, कनाडा का दक्षिण-पश्चिमी भाग।
- अफ्रीका-अफ्रीका के तटीय भाग, नील नदी का डेल्टा, नाइजीरिया तथा दक्षिणी अफ्रीका के कुछ क्षेत्र।
- दक्षिण अमेरिका-वेनेजुएला, उत्तरी-पूर्वी ब्राजील, मध्यवर्ती चिली आदि।
- ऑस्ट्रेलिया ऑस्ट्रेलिया का तटवर्ती भाग तथा मरे-डार्लिंग, नदियों का बेसिन।
3. सघन जनसंख्या अथवा उच्च घनत्व के क्षेत्र-जिन प्रदेशों में जनसंख्या का घनत्व 200 व्यक्ति प्रति वर्ग कि०मी० से अधिक है, उन्हें सघन जनसंख्या वाले प्रदेश कहते हैं। उच्च घनत्व वाले प्रदेश विश्व में निम्नलिखित हैं
(1) मानसून एशिया – इस प्रदेश की जलवायु मानव तथा कृषि दोनों के लिए अनुकूल है। कृषि फसलों के लिए वर्धनकाल लम्बा है। जलवायु विभिन्नता के कारण अनेक ऋतुएँ तथा उनमें विभिन्न प्रकार की कृषि फसलें उगाई जाती हैं। वर्ष में 2 से 3 फसलें उगाई जाती हैं। यहाँ की जनसंख्या अधिकांशतः कृषि पर निर्भर करती है। इन क्षेत्रों में समतल मैदानी भू-भाग हैं, जिनमें कहीं-कहीं जनसंख्या का घनत्व 700 से 1000 व्यक्ति प्रति वर्ग कि०मी० तक है। इस क्षेत्र में चीन, भारत, पाकिस्तान, बांग्लादेश, इण्डोनेशिया, जापान, सिंगापुर आदि आते हैं। नगरीकरण एवं औद्योगिकीकरण के कारण कई क्षेत्रों में जनसंख्या का घनत्व 2000 व्यक्ति प्रति वर्ग कि०मी० से भी अधिक है। सिंगापुर में जनसंख्या का घनत्व 5000 व्यक्ति प्रति वर्ग कि०मी० से अधिक है।
(2) पश्चिमी यूरोप – पश्चिमी यूरोप में औद्योगिकीकरण एवं नगरीकरण की प्रक्रिया 19वीं शताब्दी से ही चल रही है। लोग उद्योग, व्यापार तथा वाणिज्य को मुख्य व्यवसाय के रूप में अपना रहे हैं। यहाँ सघन जनसंख्या दक्षिणी तथा पश्चिमी भाग में है। उत्तर में जनसंख्या अपेक्षाकृत कम है। सघन जनसंख्या वाला क्षेत्र इंग्लिश चैनल से पूर्व में नीपर नदी तक है। इसमें स्पेन, पुर्तगाल, दक्षिणी फ्राँस, ब्रिटेन, जर्मनी, हॉलैण्ड और बेल्जियम आदि सम्मिलित हैं।
(3) संयुक्त राज्य अमेरिका का मध्य – पूर्वी भाग संयुक्त राज्य अमेरिका के मध्य-पूर्वी भाग में यूरोपीय लोग आकर बसे और उसके बाद इस क्षेत्र में औद्योगिकीकरण तथा नगरीकरण की गति भी तीव्र रही, जिसके कारण जनसंख्या का घनत्व वर्तमान समय में अधिक हो गया है। जीवन की सभी सुविधाएँ सुलभ हैं। कृषि, उद्योग, व्यापार, वाणिज्य आदि सभी व्यवसायों का विकास द्रुतगति से हुआ है। दक्षिणी-पूर्वी कनाडा भी जनसंख्या की दृष्टि से सघन क्षेत्र हैं। देश की राजधानी तथा अन्य व्यापारिक नगर इसी क्षेत्र में हैं।
प्रश्न 2.
जनांकिकीय संक्रमण सिद्धान्त की विभिन्न अवस्थाओं का विस्तारपूर्वक वर्णन करें।
अथवा जनांकिकीय
संक्रमण पर एक संक्षिप्त टिप्पणी लिखिए।
उत्तर:
संसार में जनसंख्या की वृद्धि के इतिहास पर दृष्टिपात करने से जनसंख्या के विकास की विभिन्न अवस्थाएँ (Stages) दिखाई देती हैं। समय के साथ-साथ जनसंख्या में होने वाले क्रमिक परिवर्तन को जनांकिकीय संक्रमण कहते हैं। जैसे-जैसे कोई देश विकास करता है, उसकी जन्म-दर और मृत्यु-दर में परिवर्तन होने लगता है। उस देश की जनसंख्या का विकास होने लगता है, जो कुछ क्रमिक अवस्थाओं में होता है। जनसंख्या के विकास चक्र में सामान्यतः पाँच अवस्थाएँ होती हैं। इन अवस्थाओं को जनसंख्या चक्र (Population Cycle) कहते हैं। बर्गडौरफर (Burgdorfer), ब्लेकर (Blaker), साइमन (Simon), संयुक्त राष्ट्र (United Nations) आदि ने जनसंख्या चक्र की विभिन्न अवस्थाओं पर अपने विचार दिए हैं। जनांकिकीय संक्रमण की प्रायः पाँच अवस्थाएँ देखने को मिलती हैं
1. प्रथम अवस्था (First Stage)-जनांकिकीय संक्रमण की यह पहली अवस्था होती है। इसमें उच्च जन्म-दर और उच्च मृत्यु-दर दोनों होते हैं। अतः जनसंख्या धीमी गति से बढ़ती है। यह 40 से 50 तक जन्म तथा मृत्यु प्रति हजार होती है। जन्म-दर तथा मृत्यु-दर बराबर होने के कारण इन देशों में जनसंख्या वृद्धि-दर बहुत मन्द होती है। यहाँ लोगों की मान्यता होती है कि “बहुत सारे बच्चों में से कुछ तो जिएँगे।” इसमें जनसंख्या की शुद्ध वृद्धि-दर लगभग 1 प्रतिशत होती है। इसे उच्च स्थिरता की अवस्था भी कहा जाता है।
2. द्वितीय अवस्था (Second Stage)-जनांकिकीय संक्रमण की दूसरी अवस्था में आर्थिक विकास होते हैं। अकाल तथा सूखे पर नियंत्रण, खान-पान में सुधार, स्वास्थ्य सेवाओं के विकास की प्रक्रिया के आरम्भ होने से मृत्यु-दर कम हो जाती है। परन्तु जन्म-दर ऊँची बनी रहती है। अतः इस अवस्था में जनसंख्या तेजी से बढ़ती है। विकासशील देश इसी अवस्था से गुजर रहे हैं। एशिया में पूर्वी दक्षिणी और मध्य एशिया के देश इसी अवस्था में हैं।
3. तृतीय अवस्था (Third Stage)-जनांकिकीय संक्रमण की इस अवस्था में जन्म-दर में कमी आने से जनसंख्या वृद्धि-दर कम हो जाती है। यह अवस्था उच्च जन्म-दर (High Fertility) तथा मध्यम मृत्यु-दर (Moderate Mortality) वाली होती है। अमेरिका, ब्राजील, इक्वाडोर तथा पेरू इसी अवस्था में है। आधुनिक खेती, नगरीकरण, औद्योगिकीकरण इस अवस्था की पहचान हैं। इस अवस्था को विलम्ब से वृद्धि वाली अवस्था कहा जाता है।
4. चौथी अवस्था (Fourth Stage)-जनांकिकीय संक्रमण की इस अवस्था में जन्म-दर एवं मृत्यु-दर दोनों ही कम हो जाती है। यह अवस्था मध्यम जन्म-दर (Moderate Fertility) तथा निम्न मृत्यु-दर (Low Mortality) वाली होती है। फलस्वरूप जनसंख्या की वृद्धि-दर बहुत ही कम हो जाती है। कुछ देशों में तो वृद्धि-दर शून्य हो जाती है। इसे न्यून स्थिरता की अवस्था कहते हैं। संयुक्त राज्य अमेरिका, कनाडा, ऑस्ट्रेलिया एवं न्यूजीलैण्ड आज इसी अवस्था में हैं।
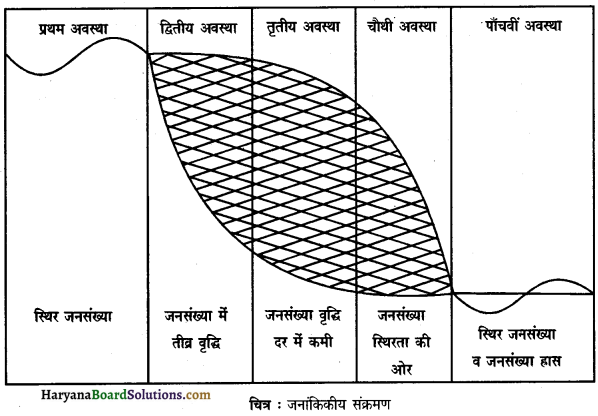
5. पाँचवीं अवस्था (Fifth Stage)-जनांकिकीय संक्रमण की यह अन्तिम अवस्था मानी जाती है। इस अवस्था में जन्म-दर कम होकर प्रायः शून्य त है। मृत्यु-दर जन्म-दर से अधिक हो जाती है, जिससे जनसंख्या घटने लगती है। इस अवस्था में आर्थिक विकास अपने उच्चतम स्तर पर होता है। लोगों में बच्चे पैदा करने की चाहत नहीं रहती है और न ही उनके पास समय होता है। इस अवस्था को जनांकिकीय संक्रमण की ह्रासमान अवस्था कहा जाता है। पश्चिमी यूरोप के प्रायः सभी देश और जापान इसी अवस्था में हैं। रूस, यूक्रेन, फ्रांस व इटली में भी लगभग यही अवस्था है। यहाँ जनसंख्या बढ़ने की बजाय कम हो रही है।
प्रश्न 3.
प्रवास से आपका क्या अभिप्राय है? इसे निर्धारित करने वाले कारकों का विस्तृत वर्णन करें। अथवा प्रवास को प्रभावित करने वाले कारकों/तत्त्वों का वर्णन कीजिए।
उत्तर:
प्रवास का अर्थ एवं परिभाषाएँ-युगों से ही मानव वर्गों (Human Groups) का प्रवास होता रहा है। मानव जातियाँ (Human Races) आदिकाल से ही अपने उद्गम प्रदेश के बाहर प्रवास करती रही हैं। ऐतिहासिक काल में भी, पृथ्वी के विभिन्न भागों, एक स्थान से दूसरे स्थान पर, मानव वर्गों का प्रवसन होता रहा है, इसे जनसंख्या का स्थानान्तरण या प्रवास कहते हैं। स्थानान्तरण या प्रवास मात्र स्थान परिवर्तन ही नहीं, बल्कि क्षेत्रीय तत्त्वों को समझने का आधार भी है। यह सामाजिक और आर्थिक पक्षों से जुड़ी हुई एक महत्त्वपूर्ण घटना है। संयुक्त राष्ट्र संघ के जनांकिकीय शब्दकोष के अनुसार, “प्रवास/प्रवसन एक प्रकार की भौगोलिक अथवा स्थानिक प्रवासिता है जो एक भौगोलिक इकाई के बीच देखने को मिलती है, जिनमें रहने का मूल स्थान अथवा पहुँचने का स्थान दोनों भिन्न होते हैं। यह प्रवास स्थायी होता है, क्योंकि इसमें मानव का निवास स्थान स्थायी रूप से परिवर्तित हो जाता है।” इसी प्रकार डेविड हीर के अनुसार, “अपने सामान्य निवास स्थान से किसी दूसरे स्थान पर जाकर बसना स्थानान्तरण (प्रवसन) कहलाता है।”
स्थानान्तरण या प्रवास को निर्धारित करने वाले कारक-प्रवास को निर्धारित करने वाले अनेक कारक हैं। प्रवास के कारणों का कोई सामान्य नियम नहीं है, क्योंकि प्रवास की प्रक्रिया व्यक्ति के अपने निर्णय से जुड़ी होती है। बड़े पैमाने पर प्रवास के कई कारण हैं, जिन्हें मुख्य रूप से निम्न भागों में बाँटा जा सकता है आर्थिक कारक, भौतिक कारक, धार्मिक या सांस्कृतिक कारक, राजनीतिक कारक और जनसांख्यिकीय कारक आदि। इनका संक्षिप्त विवरण निम्नलिखित है-
1. आजीविका (Earning) – सीमित संसाधन तथा बढ़ती जनसंख्या के कारण कृषि एवं अन्य क्षेत्रों में एक निश्चित जनसंख्या को ही रोजगार मिलता है। इस कारण जनसंख्या का एक बड़ा भाग आजीविका की खोज में गाँवों से नगरों की ओर प्रवास होता है। इसके अतिरिक्त किसी क्षेत्र में जनसंख्या का दबाव बढ़ने से जनसंख्या-संसाधन सन्तुलन बिगड़ने के कारण लोग आजीविका के लिए विकसित और सिंचाई समृद्ध कृषि क्षेत्रों में जाना पसन्द करते हैं। उत्तरी अमेरिका, लैटिन अमेरिका, ऑस्ट्रेलिया एवं दक्षिणी अफ्रीका में उपलब्ध विस्तृत कृषि योग्य भूमि ने यूरोप, चीन और जापान में लोगों को आकर्षित किया है।
2. विवाह (Marriage) – सामाजिक रीति के अनुसार लड़कियों को विवाह के पश्चात् ससुराल में रहना पड़ता है। यही कारण है कि भारत में स्त्रियों की प्रवास दर काफी ऊँची है। यह प्रवास गाँव या नगरों से नगरों की ओर होता है। नगरों से गाँव की ओर प्रवास कम होता है।
3. शिक्षा (Education) – प्रायः गाँवों में उच्च शिक्षा की सुविधाएँ नहीं होतीं। उच्च शिक्षा व योग्यता में वृद्धि हेतु लोग शहरों में उपलब्ध विभिन्न प्रकार की उच्च तथा तकनीकी शिक्षा प्राप्त करने के लिए शहरों में प्रवास करते हैं। सुशिक्षित, निपुण, कलाकार, वैज्ञानिक तथा अन्य क्षेत्रों में योग्य लोग शहरों में अपनी उन्नति के अवसरों की तलाश में प्रवास करते हैं। इसके अतिरिक्त आर्थिक रूप से समृद्ध परिवार अपने बच्चों की शिक्षा के लिए गाँवों से शहरों व छोटे शहरों से बड़े शहरों में, जहाँ शिक्षा की अच्छी सुविधाएँ होती हैं, प्रवास करते हैं।
4. सामाजिक असुरक्षा (Social Unsecurity) – जिस किसी देश या प्रदेश में राजनीतिक अस्थिरता एवं गड़बड़ी, जातीय दंगे, वर्ग-संघर्ष आदि की सम्भावनाएँ अधिक होती हैं तो ऐसे क्षेत्रों की जनसंख्या क्षेत्र को छोड़कर अन्य शांत क्षेत्रों को प्रवास कर जाते हैं। उदाहरण के लिए, कश्मीर में राजनीतिक अस्थिरता व अशान्ति के कारण कश्मीरी पंडित कश्मीर प्रवास कर गए। इसी प्रकार सन् 1947 के देश विभाजन में भारत व पाकिस्तान से लोगों का प्रवास हुआ।
5. प्राकृतिक प्रकोप (Natural Destroy) – प्राकृतिक प्रकोप भी जनसंख्या को प्रवास करने पर मजबूर करते हैं। भयंकर बाढ़ें, सूखा, बीमारियाँ आदि प्राकृतिक प्रकोपों से लोग भयभीत व मजबूर होकर प्रवास करते हैं। ज्वालामुखी के आकस्मिक विस्फोट के कारण भी मानव को अपने निवास स्थान को छोड़ने के लिए बाध्य होना पड़ता है। सिसली, फिलीपीन और हवाई द्वीपों से इसी कारण लोग अन्य देशों में जाकर बस गए हैं। भूकम्प भी प्रवास का एक मुख्य कारण है। सन् 1934 में बिहार के भूकम्प के समय हजारों लोग पश्चिमी बंगाल, उत्तर प्रदेश और ओडिशा में जाकर स्थाई रूप से बस गए थे।

प्रश्न 4.
मर्त्यता से क्या तात्पर्य है? इसे निर्धारित करने वाले कारकों का वर्णन कीजिए।
उत्तर:
मर्त्यता का अर्थ (Meaning of Mortality) जन्म की तरह मृत्यु भी एक निश्चित घटित होने वाली महत्त्वपूर्ण जैविक घटना है। सन् 1953 में संयुक्त राष्ट्र संघ (UNO) द्वारा मर्त्यता की दी गई परिभाषा के अनुसार “जन्म के बाद जीवन के सभी लक्षणों का स्थायी रूप से समाप्त हो जाना मर्त्यता कहलाता है।”
मर्त्यता की माप (Measures of Mortality)-जनसंख्या वृद्धि के निर्धारण में मर्त्यता की महत्त्वपूर्ण भूमिका है। मर्त्यता में कमी आने के कारण भी जनसंख्या वृद्धि हो जाती है। मर्त्यता को मुख्य रूप से निम्नलिखित विधियों द्वारा मापा जाता है
- अशोधित मृत्यु-दर
- शिशु मृत्यु-दर
- मातृ मृत्यु-दर
- आयु विशिष्ट मृत्यु-दर।
इन विधियों में अशोधित मृत्यु-दर अधिक सर्वमान्य है जिसका वर्णन निम्नलिखित है-
अशोधित मृत्यु-दर (Crude Death Rate)-एक वर्ष में प्रति हजार जनसंख्या के अनुपात में मरने वाले व्यक्तियों की संख्या को अशोधित मृत्यु-दर कहा जाता है। इसे निम्नलिखित सूत्र द्वारा दर्शाया जाता है-

मर्त्यता के निर्धारक कारक (Determinants of Mortality)-अधिक जन्म-दर और अधिक मृत्यु-दर किसी देश के पिछड़ेपन का सूचक है जबकि कम जन्म-दर और कम मृत्यु-दर किसी देश की आर्थिक उन्नति के सूचक हैं। मृत्यु-दर किसी देश की जनसांख्यिकी संरचना सामाजिक प्रगति तथा आर्थिक विकास की सूचक है। मर्त्यता को प्रभावित करने वाले कारक निम्नलिखित हैं
1. आयु संरचना (Age Structure) युवाओं की अपेक्षा प्रौढ़ों में मृत्यु की संभावना अधिक होती है। अच्छी चिकित्सा सुविधाओं के कारण मृत्यु को कुछ समय के लिए रोका जा सकता है तथा जीवन प्रत्याशा को बढ़ाया जा सकता है। इसी कारण विकसित देशों में प्रौढ़ों की जनसंख्या में बढ़ोत्तरी प्रतीत हो रही है।
2. लिंग संरचना (Sex Structure) स्त्रियों और पुरुषों की मृत्यु-दर भी अलग-अलग होती है। स्त्रियों की रोग प्रतिरोधक क्षमता पुरुषों की अपेक्षा अधिक है। इसलिए प्रत्येक आयु वर्ग में स्त्रियों की मर्त्यता भी कम है और उनकी जीवन प्रत्याशा भी पुरुषों की अपेक्षा अधिक है, परंतु विकासशील और पिछड़े देशों में स्थिति बिल्कुल विपरीत है। इन देशों में स्त्रियों की मृत्यु-दर पुरुषों से अधिक है। इसका प्रमुख कारण इन देशों में लड़कियों और स्त्रियों के प्रति भेदभावपूर्ण दृष्टिकोण का होना है।
3. नगरीकरण (Urbanization)-नगर में होने वाली दुर्घटनाएँ, प्रदूषित वातावरण तथा वहाँ की तनावपूर्ण जिंदगी भी उच्च मृत्यु-दर के लिए उत्तरदायी है।
4. सामाजिक कारक (Social Factors)-भ्रूण हत्या, स्वास्थ्य सुविधाओं का अभाव, साक्षरता दर तथा धार्मिक विश्वास आदि सामाजिक कारक भी मर्त्यता को प्रभावित करते हैं।
प्रश्न 5.
प्रजननशीलता क्या है? प्रजननशीलता को निर्धारित या प्रभावित करने वाले कारकों की व्याख्या कीजिए।
उत्तर:
प्रजननशीलता का अर्थ (Meaning of Fertility)-प्रजननशीलता से तात्पर्य स्त्री द्वारा पूरे समय बाद किसी समय विशेष में जीवित जन्म देने वाले बच्चों की संख्या से है। कुछ स्त्रियों में गर्भ धारण करने की क्षमता तो होती है परंतु प्रजननशीलता नहीं होती। किसी देश की जनसंख्या वृद्धि को प्रभावित करने में प्रजननशीलता महत्त्वपूर्ण कारक है। यदि प्रजननशीलता मृत्यु-दर से अधिक है तो जनसंख्या में वृद्धि होगी। इसके विपरीत प्रजननशीलता से मृत्यु-दर अधिक होने पर जनसंख्या में कमी होगी।
प्रजनन दर मापने की विधियाँ (Methods of Measuring Fertile Rate)-प्रजनन दर को निम्नलिखित दो विधियों द्वारा व्यक्त किया जाता है-
1. अशोधित जन्म-दर (Crude Birth Rate)-किसी क्षेत्र में प्रति वर्ष हजार व्यक्तियों में जीवित जन्म लेने वाले बच्चों की संख्या को जन्म-दर कहा जाता है। किसी क्षेत्र की जनसंख्या में जन्म-दर को निम्नांकित प्रकार से दर्शाया जा सकता है-
B = \(\frac{\mathbf{N}_{\mathbf{n}}}{\mathbf{P}}\) x 100
B = जन्म-दर, Nn = एक वर्ष में जन्मे नवजात शिशुओं की संख्या।
P = उस वर्ष के मध्य की जनसंख्या
यद्यपि इस विधि का प्रचलन अधिक है, फिर भी यह दोषयुक्त है, क्योंकि इसमें संपूर्ण जनसंख्या से भाग दिया जाता है कि संपूर्ण जनसंख्या कभी भी प्रजनन क्षमता की परिधि में नहीं आती।
2. सामान्य प्रजनन दर (General Fertile Rate)-प्रजनन आयु वर्ग (15-49 वर्ष) की 1000 स्त्रियों के पीछे जन्मे जीवित बच्चों की संख्या को सामान्य प्रजनन दर कहते हैं। इसे निम्नलिखित प्रकार से निकाला जा सकता है-

प्रजननशीलता/प्रजननता को निर्धारित या प्रभावित करने वाले कारक (Factor-Effecting of Fertility)-प्रजननशीलता को निर्धारित करने वाले कारकों को निम्नलिखित दो वर्गों में रखा गया है-
(क) जैव कारक (Biological Factors) – जैव कारकों में लोगों की प्रजातियाँ, प्रजनन क्षमता तथा उनके शारीरिक और मानसिक स्वास्थ्य का प्रभाव आता है। विश्व में विभिन्न प्रजातियों के लोगों का जनसंख्या स्तर एक जैसा नहीं पाया जाता जबकि वे एक समान पर्यावरण में रहते हैं। शारीरिक और मानसिक स्वास्थ्य भी प्रजननशीलता को प्रभावित करता है। अच्छे शारीरिक और मानसिक स्वास्थ्य की दशा में प्रजनन दर ऊँची पाई जाती है जबकि अस्वस्थ शारीरिक और मानसिक वातावरण में मर्त्यता (Mortality) ऊँची पाई जाती है। स्त्रियों की प्रजनन क्षमता भी प्रजननशीलता को प्रभावित करती है। प्रजनन क्षमता या संतानोत्पादकता स्त्रियों में सामान्यतया 14 से 44 वर्ष की आयु तक पाई जाती है, लेकिन यह अवधि विभिन्न स्त्रियों में अलग-अलग पाई जाती है। भारत में यह आयु 15 से 49 वर्ष की है जबकि ठंडे देशों में यह आयु वर्ग कुछ भिन्न होती है।
(ख) प्रजननता को प्रभावित करने वाले अन्य कारक (Other factor-Effecting of Fertility) प्रजननता को अन्य निम्नलिखित कारक प्रभावित करते हैं
1. शिक्षा का स्तर (Stage of Education) – शिक्षा का उच्च स्तर प्रजननता को निश्चित रूप से प्रभावित करता है। शिक्षित पति-पत्नी की अपेक्षा अशिक्षित पति-पत्नियों में प्रजननता अधिक पाई जाती है। अतः शिक्षा का प्रजननता से सीधा संबंध है।
2. विवाह की आयु (Age of Marriage) – 15 से 49 वर्ष के वर्ग की स्त्रियाँ सामान्य रूप से बच्चे पैदा करने में सक्षम होती हैं। यदि 15 वर्ष की आयु में विवाह किया जाए तो 34 वर्ष बच्चे पैदा करने के लिए मिलते हैं। इस अवधि में नारी लगभग 14-15 बच्चे पैदा कर सकती है। यदि 21 वर्ष की आयु के बाद कन्या का विवाह किया जाए तो अपेक्षाकृत कम बच्चे पैदा करने का अवसर मिलता है। अतः विवाह की आयु प्रजननता को प्रभावित करती है। इसलिए सरकार ने जनसंख्या वृद्धि को रोकने के लिए लड़कियों की विवाह आयु 18 वर्ष तथा लड़कों की 21 वर्ष निर्धारित की है।
3. आर्थिक स्तर (Economic Stage) – गरीबी और जनसंख्या वृद्धि का सीधा संबंध है। यहाँ विभिन्न आय वर्ग के लोगों में प्रजननता दर में भिन्नता पाई जाती है। सामान्यतया निम्न आय वर्ग या गरीबी की रेखा से नीचे जीवन-यापन करने वाले लोगों में उच्च प्रजननता दर मिलती है, जबकि उच्च आय वर्ग के लोगों में कम प्रजननता मिलती है।
4. व्यवसाय (Business) – प्रत्येक व्यवसाय के लोगों में प्रजननता दर समान नहीं पाई जाती। किसान और मजदूरों में प्रजनन दर सामान्य से अधिक होती है, जबकि अन्य सेवाओं में लगे लोगों की प्रजननता दर कुछ कम होती है।
5. धार्मिक मान्यताएँ (Realistic Assumptions) – धर्म के अनुसार भी प्रजननता की दर में भिन्नता पाई जाती है। प्रायः सभी धर्म जनसंख्या नियंत्रण का विरोध करते हैं, फिर भी यह नियंत्रण भिन्न-भिन्न धर्मों में भिन्न-भिन्न है। जिन धर्मों में परिवार कल्याण के साधनों का उपयोग नहीं किया जा रहा है, उस धर्म के लोगों की प्रजनन दर अधिक है। हिंदुओं की प्रजननता दर मुसलमानों की प्रजननता दर से कम है।
प्रश्न 6.
विश्व में जनसंख्या वृद्धि के कारणों का वर्णन कीजिए।
उत्तर:
विश्व में जनसंख्या वृद्धि के कारण निम्नलिखित हैं-
1. उच्च जन्म-दर तथा निम्न मृत्यु-दर (High Birth Rates and Low Death Rates)-जनसंख्या की वृद्धि-दर जन्म-दर तथा मृत्यु-दर के अन्तर से ज्ञात की जाती है। जब मृत्यु-दर कम तथा जन्म-दर अधिक होती है, तब जनसंख्या में वृद्धि होती है। प्राकृतिक तौर पर होने वाले जन्म-दर तथा मृत्यु-दर के अन्तर को प्राकृतिक वृद्धि-दर कहते हैं तथा दो समयावधियों के बीच होने वाले जनसंख्या सम्बन्धी परिवर्तन को वृद्धि-दर कहते हैं। जब जन्म-दर अधिक तथा मृत्यु-दर कम हो या किसी अन्य देश से आकर जनंसख्या में बढ़ोत्तरी हो जाए तो इसे धनात्मक वृद्धि कहते हैं। जब दो समयावधियों के बीच जनसंख्या में कमी आए तो इसे ऋणात्मक वृद्धि कहते हैं। ऐसा तब होता है, जब मृत्यु-दर अधिक तथा जन्म-दर कम हो या जनसंख्या बाहर प्रवास कर जाए।
2. प्रवास (Migration)-किसी स्थान पर धनात्मक कारकों के कारण दूसरे स्थान से लोग प्रवासित होते हैं तो भी जनसंख्या में वृद्धि होगी। शहरों तथा कस्बों में उच्च शिक्षा, रोजगार की सुविधा, सुरक्षा, यातायात के साधन, चिकित्सा सुविधाएँ आदि विकसित अवस्था में होते हैं तो आस-पास के क्षेत्र से लोग यहाँ पर आकर रहने लगते हैं। ब्रिटेन, संयुक्त राज्य अमेरिका, कनाडा, जर्मनी में जनसंख्या वृद्धि इसी कारण से हुई है।
3. खनिज संसाधनों का आकर्षण (Attraction of Minerals)-संसार में जिन भागों में खनिज संसाधन अधिक हैं, वे क्षेत्र मानव को बसाव के लिए आकर्षित करते हैं। मानव उन क्षेत्रों में श्रमिकों के रूप में कार्य करते हैं। चाहे वहाँ की जलवायु सम हो या विषम। स्वीडन में लौह-अयस्क के कारण गेलिवारे नगर में जनसंख्या बढ़ी है। कनाडा की यक्रेन में केपर बैंक नगर, पश्चिमी ऑस्ट्रेलिया में कालगुर्ली, भारत में दामोदर घाटी, जर्मनी में रूस घाटी, रूस का डोनेट्स बेसिन, अल्लेशिन क्षेत्र आदि कई उदाहरण हैं, जहाँ खनिजों के कारण ही उन क्षेत्रों में जनसंख्या आकर्षित हुई।
4. उद्योगों का प्रभाव (Effect of Industries)-किसी भी क्षेत्र में यदि उद्योग विकसित होते हैं, तब वहाँ पर जनसंख्या में वृद्धि होने लगती है, क्योंकि उद्योगों में काम करने के लिए उन क्षेत्रों में अन्य देशों से श्रमिक आते हैं और वहाँ बसते हैं। आबादी श्रम के रूप में आती है और उस क्षेत्र में इस प्रकार उद्योगों के साथ-साथ जनसंख्या भी बढ़ती जाती है; जैसे पूर्वी संयुक्त राज्य अमेरिका तट, पश्चिमी यूरोप का तटीय भाग, भारत में छोटा नागपुर पठार आदि ऐसे क्षेत्र हैं, जहाँ उद्योगों के विकास के साथ-साथ जनसंख्या भी बढ़ती गई।
5. निम्न जीवन-स्तर (Low Life Standard)-जिन क्षेत्रों में लोगों का जीवन-स्तर निम्न होगा, वहाँ अज्ञानता की बढ़ोतरी होगी, इसलिए वहाँ पर जनसंख्या वृद्धि तीव्र गति से होगी, क्योंकि वहाँ के लोगों को वहाँ के संसाधनों को प्रयोग करने का पूर्ण ज्ञान नहीं होता। वहाँ प्रति व्यक्ति आय कम होने से जनसंख्या में बढ़ोतरी होती है।
6. आर्थिक विकास (Economic Development)-जनसंख्या वृद्धि का मुख्य प्रभाव क्षेत्रीय अर्थव्यवस्था पर पड़ता है। प्राथमिक अर्थव्यवस्था वाले विकासशील देशों में वृद्धि-दर दो प्रतिशत से चार प्रतिशत के बीच होती है; जैसे एशिया, अफ्रीका, दक्षिण अमेरिका आदि। विकसित अर्थव्यवस्था वाले क्षेत्रों में जनसंख्या वृद्धि-दर 1.7% से भी कम पाई जाती है। इस प्रकार आर्थिक विकास तथा जनसंख्या वृद्धि-दर व सह-सम्बन्ध स्पष्ट देखने को मिलता है। आर्थिक रूप से पिछड़े क्षेत्रों में जन्म-दर अधिक पाई जाती है। आर्थिक पिछड़ेपन के कारण मृत्यु-दर भी अधिक होती है; जैसे कालाहारी मरुस्थल के बुशमैन।
7. स्वास्थ्य सेवाएँ (Health Services)-विकसित देशों में स्वास्थ्य सेवाओं के कारण मृत्यु-दर पर अंकुश लग जाता है, लेकिन जन्म-दर बढ़ती जाती है, जिससे जनसंख्या तीव्र गति से बढ़ने लगती है; जैसे दक्षिणी पूर्वी एशियाई देशों में ऐसी स्थिति बनी हुई है।

प्रश्न 7.
जनसंख्या परिवर्तन के घटकों का वर्णन कीजिए।
उत्तर:
जनसंख्या परिवर्तन के तीन घटक होते हैं-
- प्रजननशीलता या जन्म दर
- मृत्यु दर या मर्त्यता
- प्रवास।
1. प्रजननशीलता-प्रजननशीलता से तात्पर्य स्त्री द्वारा पूरे समय बाद किसी समय विशेष में जीवित जन्म देने वाले बच्चों की संख्या से है। कुछ स्त्रियों में गर्भ धारण करने की क्षमता तो होती है परंतु प्रजननशीलता नहीं होती। किसी देश की जनसंख्या वृद्धि ननशीलता महत्त्वपूर्ण कारक है। यदि प्रजननशीलता मृत्यु-दर से अधिक है तो जनसंख्या में वृद्धि होगी। इसके विपरीत प्रजननशीलता से मृत्यु-दर अधिक होने पर जनसंख्या में कमी होगी।
प्रजनन दर मापने की विधियाँ – प्रजनन दर को निम्नलिखित दो विधियों द्वारा व्यक्त किया जाता है-
(1) अशोधित जन्म-दर-किसी क्षेत्र में प्रति वर्ष हजार व्यक्तियों में जीवित जन्म लेने वाले बच्चों की संख्या को जन्म-दर कहा जाता है। किसी क्षेत्र की जनसंख्या में जन्म-दर को निम्नांकित प्रकार से दर्शाया जा सकता है
B = \(\frac{\mathbf{N}_{\mathbf{n}}}{\mathbf{P}}\) x 100
B = जन्म-दर, Nn = एक वर्ष में जन्मे नवजात शिशुओं की संख्या।
P = उस वर्ष के मध्य की जनसंख्या
यद्यपि इस विधि का प्रचलन अधिक है, फिर भी यह दोषयुक्त है, क्योंकि इसमें संपूर्ण जनसंख्या से भाग दिया जाता है कि संपूर्ण जनसंख्या कभी भी प्रजनन क्षमता की परिधि में नहीं आती।
(2) सामान्य प्रजनन दर-प्रजनन आयु वर्ग (15-49 वर्ष) की 1000 स्त्रियों के पीछे जन्मे जीवित बच्चों की संख्या को सामान्य प्रजनन दर कहते हैं। इसे निम्नलिखित प्रकार से निकाला जा सकता है-

2. मर्त्यता-जन्म की तरह मृत्यु भी एक निश्चित घटित होने वाली महत्त्वपूर्ण जैविक घटना है। सन् 1953 में संयुक्त राष्ट्र संघ (UNO) द्वारा मर्त्यता की दी गई परिभाषा के अनुसार “जन्म के बाद जीवन के सभी लक्षणों का स्थायी रूप से समाप्त हो जाना मयंता कहलाता है।”
मर्त्यता की माप – जनसंख्या वृद्धि के निर्धारण में मर्त्यता की महत्त्वपूर्ण भूमिका है। मर्त्यता में कमी आने के कारण भी जनसंख्या वृद्धि हो जाती है। मर्त्यता को मुख्य रूप से निम्नलिखित विधियों द्वारा मापा जाता है
- अशोधित मृत्यु-दर
- शिशु मृत्यु-दर
- मातृ मृत्यु-दर
- आयु विशिष्ट मृत्यु-दर।
इन विधियों में अशोधित मृत्यु-दर अधिक सर्वमान्य है जिसका उल्लेख निम्नलिखित है
अशोधित मृत्यु-दर – एक वर्ष में प्रति हजार जनसंख्या के अनुपात में मरने वाले व्यक्तियों की संख्या को अशोधित मृत्यु-दर कहा जाता है। इसे निम्नलिखित सूत्र द्वारा दर्शाया जाता है

3. प्रवास-युगों से ही मानव वर्गों (Human Groups) का प्रवास होता रहा है। मानव जातियाँ (Human Races) आदिकाल से ही अपने उद्गम प्रदेश के बाहर प्रवास करती रही हैं। ऐतिहासिक काल में भी, पृथ्वी के विभिन्न भागों, एक स्थान से दूसरे स्थान पर, मानव वर्गों का प्रवसन होता रहा है, इसे जनसंख्या का स्थानान्तरण या प्रवास कहते हैं। स्थानान्तरण या प्रवास मात्र स्थान परिवर्तन ही नहीं, बल्कि क्षेत्रीय तत्त्वों को समझने का आधार भी है। यह सामाजिक और आर्थिक पक्षों से जुड़ी हुई एक महत्त्वपूर्ण घटना है।
![]()
![]()