Haryana State Board HBSE 12th Class Chemistry Important Questions Chapter 6 तत्वों के निष्कर्षण के सिद्धांत एवं प्रक्रम Important Questions and Answers.
Haryana Board 12th Class Chemistry Important Questions Chapter 6 तत्वों के निष्कर्षण के सिद्धांत एवं प्रक्रम
बहुविकल्पीय प्रश्न:
1. निम्नलिखित में से किस धातु का निक्षालन (निष्कर्षण) सायनाइड विधि द्वारा किया जाता है?
(अ) सोडियम
(ब) सिल्वर
(स) ऐलुमिनियम
(द) कॉंपर
उत्तर:
(ब) सिल्वर
2. निम्नलिखित अभिक्रिया धातुओं के शोधन की किस विधि से सम्बन्धित है?
![]()
(अ) मंडल परिक्करण
(ब) वॉन-आरकलल विधि
(स) मान्ड प्रक्रम
(द) वर्णलेखिकी
उत्तर:
(ब) वॉन-आरकलल विधि
3. निम्नलिखित में से कौनसा यौगिक ऐलुमिनियम का अयस्क है?
(अ) Al2O3
(ब) Na3AlF6
(स) Al2O3 . H2O
(द) Al2O3 . 2H2O
उत्तर:
(द) Al2O3 . 2H2O
4. भूपर्पटी में सबसे अधिक मात्रा में पायी जाने वाली धातु है-
(अ) Mg
(ब) Ag
(स) Al
(द) Cu
उत्तर:
(स) Al
5. अयस्कों के सान्द्रण की फेन (झाग) प्लवन विधि कौनसे अयस्कों के लिए प्रयुक्त होती है?
(अ) कार्बोनेट अयस्क
(ब) सल्फाइड अयस्क
(स) औंक्साइड अयस्क
(द) हेलाइड अयस्क
उत्तर:
(ब) सल्फाइड अयस्क
![]()
6. सल्फाइड अयस्कों को ऑक्साइड में परिवर्तित करने का प्रक्रम है-
(अ) निस्तापन
(ब) भर्जंन
(स) निक्षालन
(द) फेन प्लवन विधि
उत्तर:
(ब) भर्जंन
7. कॉपर के धातु कर्म में FeO की अशुद्धि को हटाने के लिए प्रयुक्त किया जाने वाला गालक है-
(अ) CaO
(ब) CaCO3
(स) SiO2
(द) Cu2S
उत्तर:
(स) SiO2
8. जिंक ऑक्साइड के अपचयन के लिए कौनसा अपचायक प्रयुक्त किया जाता है?
(अ) CO
(ब) कोक
(स) Al
(द) उपर्युक्त सभी
उत्तर:
(ब) कोक
9. पीतल बनाने में प्रयुक्त धातुएँ है-
(अ) Cu + Ni
(ब) Fe + Cu
(स) Cu + Zn
(द) Cu + Mn
उत्तर:
(स) Cu + Zn
10. निम्नलिखित में से मैग्नेटाइट अयस्क कौनसा है?
(अ) Fe2O3
(ब) ZnO
(स) Na3AlF6
(द) Fe3O4
उत्तर:
(द) Fe3O4
11. जिंक धातु के शोधन की विधि है-
(अ) मंडल परिष्करण
(ब) प्रभाजी आसवन
(स) वाष्म अवस्था परिष्करण
(द) वैद्युत अपघटनी शोधन
उत्तर:
(ब) प्रभाजी आसवन
12. कैलामाइन, निम्नलिखित में से किस धातु का अयस्क है?
(अ) Cu
(ब) Ag
(स) Zn
(द) Al
उत्तर:
(स) Zn
13. धातकर्म में निस्तान प्रत्रम किस प्रक्र है अयस्कों के लिए प्रयुक्त नहाँ होत है?
(अ) कलयेज्ञित औक्साइड
(ब) काबनिद
(स) सक्फाइड
(द) उपर्वुक्त सभी
उत्तर:
(स) सक्फाइड
14. मंड्डल परिफ्राग किजि किस शतु के शोधन के लिए प्रदुम्त्त की जाती है?
(अ) जम्निनिम्म
(ब) गैलिखम
(स) इंध्यिम
(द) उर्ज्युक्त सभी
उत्तर:
(द) उर्ज्युक्त सभी
15. Al2O3 के वैद्युत अपषटन से Al प्राप्त करने की सिधि है-
(अ) मौन्ड प्रक्रम
(ब) बॉन-असक्त विधि
(स) सल- हेराएट प्रक्म
(द) मदल बिंजि
उत्तर:
(स) सल- हेराएट प्रक्म
16. नौतय, निम्नलिखित में से किसका सुनि है?
(अ) Cu
(ब) Al
(स) Zn
(द) Fe
उत्तर:
(ब) Al
17. कौपर के बैद्युत अपषटनी शोधन में सौने की कुछ माता किस हूप में मिलती है?
(अ) कैषेड
(ब) वैद्युत अनबटृद
(स) श्नोड मंक
(द) कैराड पंक
उत्तर:
(स) श्नोड मंक
18. निम्नलिखित में से किस धात्व के पहुकार्म में दर्मद्ध किधि का प्रयोग किवा जाता है?
(अ) Ag
(ब) Pb
(स) Fe
(द) Cr
उत्तर:
(द) Cr
19. मोडिवम के निबर्बें की किषि है-
(अ) केषर की विधि
(ब) धर्नाइट विधि
(स) द्वॉक की विधि
(द) सर्पक की विधि
उत्तर:
(ब) धर्नाइट विधि
20. चौड़ी के धातुकर्म में बना वौगिक है-
(अ) AgCN
(ब) [Na[Ag(CN)2]
(स) Na3[Ag(CN)4]
(द) वपर्वुक्त समी
उत्तर:
(ब) [Na[Ag(CN)2]
![]()
21. धातुं के सल्पद्ड अवस्कों को समान्यक् फेन सबन बिधि दूरा सान्हित किय जल है। निम्नलिखित सार्फाइड अवस्कों में से कौनसा अपवाद है गिले रासायनिक विषिए त्वरा सन्द्रित किया ज्ञाता है?
(अ) अजेंन्टम्ट
(ब) गैलेना
(स) कापर घझढ़्ट
(द) सेलेरइट
उत्तर:
(द) सेलेरइट
22. गालक, अगतनीय अथृद्धियों को गलाइए बनात है-
(अ) अधत्री
(ब) धतुमाल
(सं) मैट
(द) मैट्रिक्य
उत्तर:
(ब) धतुमाल
23. कॉचर के निद्रांग में कौन अयस्क को सिलिक तथा क्षेक दूरा है। घतुमल क अगुसात्र है-
(अ) FeSiO3
(ब) Fe2O3
(स) FeSi ( वोस)
(द) FeSi (बाल)
उत्तर:
(अ) FeSiO3
24. निम्नलिखित कपनों में से गसत क्षच को पहचानिदे-
(अ) अयन्त के सान्दूर में द्रवीब धवन से हूके कैं के कर जल के साध बहकर बाहर निकल वाते हैं तथा अ्यस्क के भागी का शोष चर ज्ञाते हैं।
(ब) श्रद्ध Al2O3 को, बौक्साद्ट अपस्क का सान सोडियम लम्ड्रौस्सद्ड के संथ निषालन से प्राप्त कहीं किपा व्या सकत है।
(स) फेन प्लवन विधि के दौरन अयस्क के कण को फेन के रूप में अलग कर लिया जाता है और गैंग शेष बचा रहता है।
(द) सल्फाइड अयस्कों को, फेन-प्लवन विधि में तेल तथा जल का अनुपात परिवर्तित करके सफलतापूर्वक अलग किया जा सकता है।
उत्तर:
(ब) श्रद्ध Al2O3 को, बौक्साद्ट अपस्क का सान सोडियम लम्ड्रौस्सद्ड के संथ निषालन से प्राप्त कहीं किपा व्या सकत है।
अतिलघूत्तरात्मक प्रश्न:
प्रश्न 1.
प्रकृति में मुक्त अवस्था में पाई जाने वाली तीन धातुएँ बताइए।
उत्तर:
सोना, चाँदी तथा प्लेटिनम।
प्रश्न 2.
सान्द्रण की फेन प्लवन विधि किस प्रकार के अयस्कों के लिए प्रयुक्त की जाती है?
उत्तर:
सल्फाइड अयस्कों के लिए।
प्रश्न 3.
गालक किसे कहते हैं?
उत्तर:
वे पदार्थ जो अशुद्धियों के गलनांक को कम करने के लिए प्रगलन प्रक्रम में मिलाए जाते हैं, उन्हें गालक कहते हैं।
प्रश्न 4.
धातुमल क्या होता है?
उत्तर:
अशुद्धि तथा गालक की क्रिया से बना पदार्थ धातुमल या कीट कहलाता है। इसका गलनांक कम होने के कारण यह आसानी से पिघल जाता है।
प्रश्न 5.
आधात्री या गैंग किसे कहते हैं?
उत्तर:
अयस्क के साथ उपस्थित अवांछनीय पदार्थों जैसे कंकड़, रेत तथा मिट्टी को आधात्री या मैट्रिक्स कहते हैं।
प्रश्न 6.
प्लवन कारक किसे कहते हैं?
उत्तर:
वे पदार्थ जो सल्फाइड अयस्क के कणों को जल प्रतिकर्षी बनाकर जल की सतह पर लाते हैं, उन्हें प्लवन कारक कहते हैं।
प्रश्न 7.
प्लवन कारकों के दो उदाहरण बताइए।
उत्तर:
सोडियम एथिल जेन्थेट तथा सोडियम ऐमिल जेन्थेट प्लवन कारक होते हैं।
प्रश्न 8.
किस प्रकार के अयस्कों के लिए निस्तापन प्रक्रम की आवश्यकता होती है?
उत्तर:
जलयोजित ऑक्साइड, कार्बोनेट तथा हाइड्रॉक्साइड अयस्कों के लिए निस्तापन प्रक्रम की आवश्यकता होती है।
प्रश्न 9.
थर्माइट क्या होता है?
उत्तर:
धातु ऑक्साइड तथा ऐलुमिनियम चूर्ण के मिश्रण को थर्माइट कहते हैं।
प्रश्न 10.
क्रोमियम के ऑक्साइड (Cr2O3) के अपचयन के लिए कार्बन के स्थान पर Al का प्रयोग किया जाता है, क्यों?
उत्तर:
Cr की ऑक्सीजन से बन्धुता, कार्बन की ऑक्सीजन से बन्धुता की तुलना में अधिक होती है, अतः क्रोमियम ऑक्साइड का अपचयन कार्बन के बजाय Al से किया जाता है।
प्रश्न 11.
पायरोधातुकर्म या तापीय अपचयन क्या होता है?
उत्तर:
धातु ऑक्साइडों को गर्म करके धातु में परिवर्तित करने की प्रक्रिया को पायरोधातुकर्म कहते हैं।
प्रश्न 12.
वर्णलेखिकी के विभिन्न प्रकार बताइए।
उत्तर:
वर्णलेखिकी मुख्यतः चार प्रकार की होती है-
- पेपर वर्णलेखिकी
- स्तंभ वर्णलेखिकी
- गैस वर्णलेखिकी
- पतली परत वर्णलेखिकी।
प्रश्न 13.
स्तंभ वर्णलेखिकी में प्रयुक्त अधिशोषक बताइए।
उत्तर:
ऐलुमिना जेल (Al2O3)
प्रश्न 14.
कॉपर का शोधन किस विधि द्वारा किया जाता है?
उत्तर:
कॉपर का शोधन वैद्युत अपघटनी विधि से किया जाता है।
प्रश्न 15.
सिलिकॉन के शोधन की विधि का नाम बताइए।
उत्तर:
मण्डल परिष्करण विधि।
![]()
प्रश्न 16.
कॉपर तथा मैग्नीशियम के मिश्रण में से इन धातुओं को किस विधि द्वारा पृथक् किया जाता है तथा क्यों?
उत्तर:
Mg तथा Cu के मिश्रण में से इन धातुओं को द्रवण विधि द्वारा पृथक् किया जाता है क्योंकि Mg की तुलना में Cu का गलनांक उच्च होता है।
प्रश्न 17.
जिंक तथा आयस के मिश्रण के पुथक्करण की विधि बताइए।
उत्तर:
Zn तथा Fe के मिश्रण को आसवन विधि द्वारा पृथक् किया जाता है क्योंकि Zn का वाष्पीकरण सुगमता से हो जाता है।
प्रश्न 18.
थर्माइट विधि द्वारा कौनसे धातु ऑक्साइडों का अपचयन किया जाता है?
उत्तर:
Cr2O3, MnO2 इत्यादि।
प्रश्न 19.
प्रगलन की प्रक्रिया कौनसी भट्टी में की जाती है?
उत्तर:
वात्या भट्टी।
प्रश्न 20.
Zn, Cd तथा Hg के शोधन के लिए कौनसी विधि प्रयुक्त की जाती है?
उत्तर:
आसवन विधि।
लघूत्तरात्मक प्रश्न:
प्रश्न 1.
भर्जन प्रक्रम को समझाइए।
उत्तर:
भर्जन (Roasting)-इस प्रक्रम में सल्फाइड अयस्कों को वायु (O2) की उपस्थिति में धातु के गलनांक से नीचे के ताप पर परावर्तनी भट्टी में तेजी से गर्म करते हैं जिससे सल्फाइड, ऑक्साइड में परिवर्तित हो जाते हैं तथा SO2 गैस निकल जाती है।
उदाहरण-
2Cu2S + 3O2 → 2Cu2O + 2SO2
2Pbs + 3O2 → 2Pbo + 2SO2
2Zns + 3O2 → 2Zno + SO2
प्रश्न 2.
धातु ऑक्साइडों के अपचयन की थर्माइट विधि को समझाइए।
उत्तर:
धातु ऑक्साइड का धातु में अपचयन – धातु ऑक्साइड का धातु में अपचयन विभिन्न विधियों द्वारा किया जा सकता है जो कि धातु ऑक्साइड की प्रकृति पर निर्भर करता है।
(i) रासायनिक अपचयन (प्रगलन ) – इस विधि में धातु ऑक्साइड का अपचयन कार्बन या CO द्वारा किया जाता है। यह प्रक्रम वात्या भट्टी में किया जाता है, जिसके लिए धातु ऑक्साइड, कार्बन (अपचायक) तथा गालक (फ्लक्स) के मिश्रण को भट्टी में डालकर गर्म किया जाता है तो कार्बन द्वारा धातु ऑक्साइड के अपचयन से धातु प्राप्त होती है जो कि द्रवित अवस्था में होती है। कुछ धातु ऑक्साइड आसानी से अपचयित हो जाते हैं, जबकि कुछ को अपचयित करना कठिन होता है। अपचयन की सामान्य अभिक्रिया निम्नलिखित है-
MxOy + yC → xM + yCO
ऊष्मागतिकी की मूल धारणाएँ धातुकर्मीय परिवर्तनों के सिद्धान्त को समझने में सहायक होती हैं। तापीय अपचयन (पायरो धातुकर्म) के लिए आवश्यक ताप परिवर्तन तथा ऑक्साइड के अपचयन के लिए आवश्यक अपचायक की पहचान गिब्ज ऊर्जा द्वारा की जाती है। इसके लिए यह आवश्यक है कि दिए गए ताप पर गिब्ज ऊर्जा का मान ऋणात्मक हो।
उदाहरण- Fe के धातुकर्म में होने वाली अभिक्रियाएँ-
Fe2O3 + 3C → 2Fe + 3CO
Fe2O3 + CO → 2FeO + CO2
FeO + CO → Fe + CO2
इस प्रक्रम में कार्बन (कोक) ईंधन तथा अपचायक दोनों का कार्य करता है। धातु के साथ उपस्थित अशुद्धियों का गलनांक उच्च होने के कारण वे आसानी से नहीं पिघलतीं अतः इनके गलनांक को कम करने के लिए फ्लक्स या गालक मिलाया जाता है जो अशुद्धि के साथ क्रिया करके धातुमल (slag) बनाता है, यह आसानी से पिघल जाता है तथा हल्का होने के कारण द्रवित धातु की सतह पर तैरता है। आयरन के धातुकर्म में SiO2 की अशुद्धि होती है जिसके लिए गालक के रूप में CaO(CaCO3) प्रयुक्त किया जाता है-

ताँबे के धातुकर्म में FeO की अशुद्धि उपस्थित होने पर SiO2 को गालक के रूप में प्रयुक्त किया जाता है।

ताँबा, कॉपर मेट के रूप में प्राप्त होता है जिसमें Cu2S तथा FeS होता है।
(ii) थर्माइट विधि (गोल्डश्मिट विधि) या एलुमिनोतापी Cr तथा Mn के ऑक्साइड कार्बन द्वारा आसानी से अपचयित नहीं होते अतः इनका अपचयन सक्रिय धातुओं जैसे Al से किया जाता है। धातु ऑक्साइड तथा ऐलुमिनियम चूर्ण के मिश्रण को थर्माइट कहते हैं। अतः इस विधि को थर्माइट विधि भी कहते हैं। इस विधि में ऑक्साइड को ऐलुमिनियम चूर्ण के साथ Mg से जलाते हैं। प्रक्रिया ऊष्माक्षेपी होती है, अतः यह स्वतः चलती रहती है।
Cr2O3 + 2 Al → Al2O3 + 2Cr + x K. Cal
3 MNO2 + 4Al → 2Al2O3 + 3Mn + x K.Cal
भारी धातु (द्रव) नीचे रहती है तथा द्रवित Al2O3 ऊपर की तरफ रहता है, जिसे टेपिंग होल द्वारा बाहर निकाल दिया जाता है।
प्रश्न 3.
(a) कच्चे लोहे तथा ढलवाँ लोहे का संघटन बताइए तथा कच्ये लोहे से ढलवाँ लोहा किस प्रकार प्राप्त किया जाता है?
(b) ढलवाँ लोहे से पिटवाँ लोहा कैसे बनाया जाता है?
उत्तर:
(a) कच्चे लोहे में 4% कार्बन तथा सूक्ष्म मात्रा में S, P, Si तथा Mn की अशुद्धियाँ होती हैं। इसे विभिन्न आकृतियों में ढाला जा सकता है। ढलवाँ लोहा में 3% कार्बन होता है। यह अतिकठोर तथा भंगुर होता है, अतः इसे पीटा नहीं जा सकता। कच्चे लोहे को रद्दी लोहे तथा कोक के साथ गर्म करने पर ढलवाँ लोहा प्राप्त होता है।
(b) ढलवाँ लोहे को हेमाटाइट की परत चढ़ी परावर्तनी भट्टी में गर्म करने से अशुद्धियाँ आक्सीकृत हो जाती हैं तथा हेमाटाइट कार्बन को कार्बन मोनोक्साइड में आक्सीकृत कर देता है-
Fe2O3 + 3C → 2Fe + 3CO
इसमें चूना पत्थर को गालक के रूप में मिलाया जाता है जिससे सल्फर, सिलिकन तथा फॉस्फोरस ऑक्सीकृत होकर धातुमल में चले जाते हैं। धातु को निकाल लिया जाता है तथा रोलरों पर से गुज़ार कर धातुमल से पृथक् कर लिया जाता है। पिटवाँ लोहा, लोहे का शुद्धतम रूप है तथा यह आघातवर्धनीय होता है। इसमें 0.25 तक कार्बन होता है।
प्रश्न 4.
अयस्क के सान्द्रण के लिए निक्षालन प्रक्रम का प्रयोग कब किया जाता है? सोने के निष्कर्षण के उदाहरण द्वारा इस प्रक्रम को समझाइए।
उत्तर:
जब कोई अयस्क, किसी उपयुक्त विलायक में विलेय हो तो प्रायः सान्द्रण की निक्षालन विधि का प्रयोग किया जाता है। सोने के निष्कर्षण में सायनाइड द्वारा निक्षालन किया जाता है। इसमें Au का ऑक्सीकरण होता है। इसके पश्चात् अधिक सक्रिय धातु जैसे जिंक का अपचायक के रूप में प्रयोग करके Au को विस्थापित कर लिया जाता है। इस प्रक्रम में प्रयुक्त अभिक्रियाएँ निम्नलिखित हैं-
4Au(s) + 8CN–(aq) + 2H2O(aq) + O2(g) → 4[Au(CN)2]–(aq) + 4OH–(aq)
2[Au(CN)2]–(aq) + Zn(s) → 2Au(s) + [Zn(CN)4]2-(aq)
बोर्ड परीक्षा के दूष्टिकोण से सम्भावित महत्त्वपूर्ण प्रश्न:
प्रश्न 1.
‘ताप धातुकर्म’ से क्या तात्पर्य होता है?
उत्तर:
धातु ऑक्साइडों को गर्म करके धातु में परिवर्तित करने की प्रक्रिया को ताप धातुकर्म या तापीय अपचयन कहते हैं।
प्रश्न 2.
निम्नलिखित की भूमिका का वर्णन कीजिए-
(i) सिल्वर अयस्क से सिल्वर के निष्कर्षण में NaCN की
(ii) विशुद्ध ऐलुमिना से ऐलुमिनियम के निष्कर्षण में क्रायोलाइट की।
उत्तर:
(i) सिल्वर अयस्क से सिल्वर के निष्कर्षण में NaCN का उपयोग, सिल्वर का संकुल बनाने में किया जाता है जिसे पृथक् करके इसकी क्रिया सक्रिय धातु (Zn) से कराकर Ag को प्राप्त कर लिया जाता है।
(ii) ऐलुमिनियम के धातु कर्म में क्रायोलाइट इसलिए मिलाया जाता है क्योंकि इससे मिश्रण का गलनांक कम हो जाता है तथा विलयन की चालकता बढ़ जाती है।
प्रश्न 3.
निम्नलिखित की भूमिका का वर्णन कीजिए-
(i) टाइटेनियम के परिष्करण में आयोडीन की
(ii) ऐलुमिनियम के धातुकर्म में क्रायोलाइट की।
उत्तर:
(i) जर्कोनियम या टाइटेनियम के शोधन के लिए वॉनआरकैल विधि-यह विधि Zr तथा Ti जैसी धातुओं से अशुद्धियों के रूप में उपस्थित ऑक्सीजन तथा नाइट्रोजन को हटाने में प्रयुक्त की जाती है। अपरिष्कृत धातु को निर्वातित पात्र में आयोडीन के साथ गरम करते हैं, जिससे धातु आयोडाइड बनता है। यह अधिक सहसंयोजी होने के कारण आसानी से वाष्पीकृत हो जाता है तथा अशुद्धि बच जाती है।
Zr + 2I2 → ZrI4
धातु आयोडाइड को 1800K ताप पर विद्युत द्वारा गरम किए गए टंग्टन तंतु पर गर्म किया जाता है, जिससे यह विघटित होकर शुद्ध धातु देता है जो कि तंतु पर जमा हो जाती है।
ZrI4 → Zr + 2I2
(ii) ऐलुमिनियम के धातु कर्म में क्रायोलाइट इसलिए मिलाया जाता है क्योंकि इससे मिश्रण का गलनांक कम हो जाता है तथा विलयन की वालकता बढ़ जाती है।
प्रश्न 4.
एक खनिज और एक अयस्क में अन्तर स्पष्ट कीजिए।
उत्तर:
भूपर्पटी में प्राकृतिक रूप से पाए जाने वाले यौगिक जिन्हें खनन द्वारा प्राप्त किया जाता है, उन्हें खनिज कहते हैं लेकिन अयस्क वे खनिज होते हैं जिनसे धातु का निष्कर्षण आसानी से हो सके तथा आर्थिक दृष्टि से लाभदायक हों।
प्रश्न 5.
निम्नलिखित प्रत्येक प्रक्रम के निर्धारक सिद्धान्त का वर्णन कीजिए-
(i) टाइटेनियम धातु का वाष्प प्रावस्था परिष्करण
(ii) सल्फाइड अयस्क का झाग प्लवन विधि द्वारा सान्द्रण।
उत्तर:
(i) जर्कोनियम या टाइटेनियम के शोधन के लिए वॉनआरकैल विधि-यह विधि Zr तथा Ti जैसी धातुओं से अशुद्धियों के रूप में उपस्थित ऑक्सीजन तथा नाइट्रोजन को हटाने में प्रयुक्त की जाती है। अपरिष्कृत धातु को निर्वातित पात्र में आयोडीन के साथ गरम करते हैं, जिससे धातु आयोडाइड बनता है। यह अधिक सहसंयोजी होने के कारण आसानी से वाष्पीकृत हो जाता है तथा अशुद्धि बच जाती है।
Zr + 2I2 → ZrI4
धातु आयोडाइड को 1800K ताप पर विद्युत द्वारा गरम किए गए टंग्टन तंतु पर गर्म किया जाता है, जिससे यह विघटित होकर शुद्ध धातु देता है जो कि तंतु पर जमा हो जाती है।
ZrI4 → Zr + 2I2
(ii) सान्द्रण की यह विधि सल्फाइड अयस्कों को गैंग से मुक्त करने के लिए प्रयुक्त की जाती है, जैसे कॉपर पाइराइटीज, गैलेना इत्यादि। इस विधि में चूर्णित अयस्क का पानी के साथ निलंबन बनाकर इसमें संग्राही (Collectors) तथा फेन-स्थायीकारी (Froth stabilisers) मिला देते हैं। संग्राही (जैसे चीड़ का तेल, यूकेलिप्टस का तेल, वसा अम्ल, जैंथेट इत्यादि ) अयस्क कणों के नहीं भीगने के गुण अक्लेदनीयता को बढ़ा देते हैं तथा फेन (झाग) स्थायीकारी (जैसे क्रिसॉल, ऐनीलीन ) फेन को स्थायित्व प्रदान करते हैं।
चीड़ का तेल इत्यादि झागकारक होते हैं तथा जैन्थैट जैसे सोडियम एथिलजैन्थैट या सोडियम एमिलजैन्थैट सल्फाइड अयस्क के कणों को जल प्रतिकर्षी बनाकर उन्हें जल की सतह पर लाने तथा तैरने में सहायक होते हैं, अतः इन्हें प्लवनकारक कहते हैं। फेन प्लवन विधि अयस्क तथा आधात्री के भीगने के गुणों में अन्तर पर आधारित है। अयस्क के कण तेल से, जबकि गैंग या (आधात्री ) के कण जल से भीगते हैं।
पैडल मिश्रण को विलोडित करता है तथा इससे वायु प्रवाहित होती है, जिससे झाग बनते हैं जिसमें अयस्क के कण होते हैं। झाग हल्के होते हैं जिन्हें मथकर अलग निकाल लिया जाता है। अयस्क के कणों को प्राप्त करने के लिए इसे सुखा लिया जाता है।
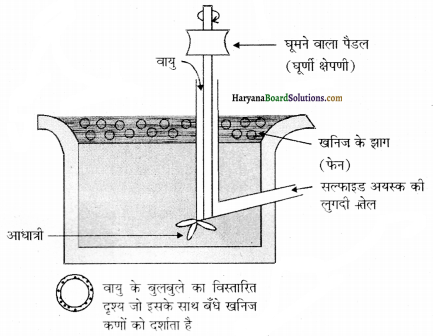
![]()
प्रश्न 6.
निम्न श्रेणी के अपने अयस्कों से कॉपर का निष्कर्षण कैसे किया जाता है?
उत्तर:
निम्न कोटि अयस्कों तथा रद्दी धातु से कॉपर का निष्कर्षण – वैद्युत रासायनिक सिद्धान्त का उपयोग करते हुए निम्न कोटि अयस्कों से कॉपर का निष्कर्षण हाइड्रो धातुकर्म द्वारा किया जाता है। निम्न कोटि अयस्कों में कॉपर बहुत ही कम मात्रा में पाया जाता है। कॉपर प्राप्त करने के लिए, अयस्क का निक्षालन अम्ल या जीवाणु (बैक्टीरिया) के उपयोग द्वारा किया जाता है, जिससे कॉपर आयन (Cu2+) विलयन में चले जाते हैं जिनकी क्रिया H2 या रद्दी आयरन से करके Cu प्राप्त किया जाता है। इस क्रिया में Cu2+ का अपचयन होता है।
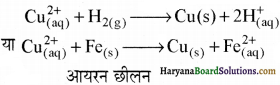
प्रश्न 7.
निम्नलिखित धातुओं को परिष्कृत करने के लिए कौन-कौन सी विधियाँ साधारण रूप से काम में लाई जाती हैं-
(i) निकल
(ii) जर्मनियम
इन विधियों के पीछे निहित सिद्धान्तों का उल्लेख कीजिए।
उत्तर:
(i) वाष्प प्रावस्था परिष्करण – शोधन की इस विधि में, धातु को वाष्पशील यौगिक में बदल कर उसे दूसरी जगह एकत्रित कर लेते हैं तथा इस वाष्पशील यौगिक के विघटन से शुद्ध धातु प्राप्त कर ली जाती है। इस विधि के लिए दो शर्तें आवश्यक हैं-
(i) उपलब्ध अभिकर्मक के साथ धातु वाष्पशील यौगिक बनाती हो तथा
(ii) वाष्पशील पदार्थ आसानी से विघटित होने वाला हो, ताकि धातु आसानी से पुनः प्राप्त की जा सके। इस विधि से Zr, Ti तथा Ni का शोधन किया जाता है।
उदाहरण- (a) निकल के शोधन की मॉन्ड की विधि-इस विधि में Ni को CO के प्रवाह में गर्म करने पर वाष्पशील संकुल यौगिक निकल टेट्राकार्बोनिल बनता है, जिसे उच्च ताप पर गर्म करने पर इसके विघटन से शुद्ध निकैल प्राप्त हो जाता है। इस प्रकार निकल से अशुद्धियाँ पृथक् हो जाती हैं।

(ii) मंडल परिष्करण या जोन परिष्करण – मंडल परिष्करण द्वारा अतिशुद्ध धातु प्राप्त होती है। यह विधि इस सिद्धान्त पर आधारित है कि अशुद्धियों की विलेयता धातु की ठोस अवस्था की अपेक्षा गलित अवस्था में अधिक होती है। इस विधि में अशुद्ध धातु की छड़ के एक किनारे पर एक वृत्ताकार गतिशील हीटर ( तापक) लगा होता है। जो छड़ को हर तरफ से घेरे रहता है। हीटर जैसे ही आगे बढ़ता है, गलित मण्डल भी आगे बढ़ता जाता है और गलित से शुद्ध धातु क्रिस्टलित हो जाती है तथा अशुद्धियाँ पास वाले गलित जोन में चली जाती हैं।
इस प्रक्रिया को कई बार दोहराते हैं तथा हीटर को एक ही दिशा में बार-बार चलाते जाते हैं। अशुद्धियाँ छड़ के एक किनारे पर एकत्रित हो जाती हैं, जिसे काटकर अलग कर लेते हैं। इस विधि से अति शुद्ध अर्धचालकों तथा अन्य शुद्ध धातुओं; जैसे-जर्मेनियम, सिलिकॉन, बोरॉन, गैलियम तथा इंडियम को प्राप्त किया जाता है।
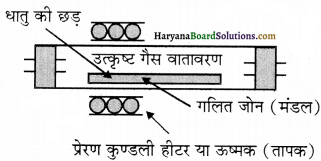
प्रश्न 8.
वैद्युत अपघटन क्रिया का ताँबे के शोधन में किस प्रकार प्रयोग होता है? समीकरणों सहित स्पष्ट कीजिए।
उत्तर:
वैद्युत अपघटनी शोधन – धातुओं के शोधन की इस विधि में अशुद्ध धातु का ऐनोड तथा शुद्ध धातु की पट्टी का कैथोड बनाया जाता है। वैद्युत अपघटनी सेल में उसी धातु के किसी उपयुक्त लवण का जलीय विलयन वैद्युत अपघट्य के रूप में प्रयुक्त किया जाता है। इसमें अधिक क्षारीय धातु विलयन में तथा कम क्षारीय धातुएँ ऐनोड पंक (anode mud) के रूप में प्राप्त होती हैं।
वैद्युत अपघटन की इस प्रक्रिया की व्याख्या इलेक्ट्रॉड विभव, अधिविभव तथा गिब्ज ऊर्जा की सहायता से की जा सकती है। वैद्युत अपघटन करने पर शुद्ध धातु कैथोड पर जमा हो जाती है तथा अशुद्धियाँ ऐनोड पर ऐनोड पंक के रूप में एकत्रित हो जाती हैं। वैद्युत अपघटन की सामान्य अभिक्रियाएँ निम्नलिखित हैं-
कैथोड पर Mn+ + ne– → M
ऐनोड पर M → Mn+ + ne–
प्रश्न 9.
फेन प्लवन विधि में संग्राही व फेन स्थायीकारक के नाम व भूमिका दीजिए।
उत्तर:
फेन प्लवन विधि में संग्राही के रूप में चीड़ का तेल, यूकेलिप्टस का तेल, वसा अम्ल या जैन्थेट प्रयुक्त किया जाता है तथा फेन स्थायीकारक के रूप में क्रिसॉल या ऐनीलिन का प्रयोग किया जाता है। संग्राही अयस्क कणों के नहीं भीगने का गुण बढ़ाता है जबकि फेन स्थायीकारक फेन को स्थायित्व प्रदान करता है।
प्रश्न 10.
बॉक्साइट अयस्क में उपस्थित किन्हीं दो अशुद्धियों के नाम लिखिए।
उत्तर:
बॉक्साइट अयस्क में सिलिका (SiO2) तथा टाइटेनियम आक्साइड (TiO2) की अशुद्धियाँ उपस्थित होती हैं।
प्रश्न 11.
निकल धातु शोधन के मॉन्ड प्रक्रम से सम्बन्धित रासायनिक अभिक्रियाएँ लिखिए।
उत्तर:

प्रश्न 12.
(i) कॉपर का शुद्धिकरण किस विधि से किया जाता है?
(ii) ऐलुमिनियम के मुख्य अयस्क का नाम बताइए तथा ऐलुमिनियम के निष्कर्षण में निक्षालन के महत्त्व की व्याख्या कीजिए।
उत्तर:
(i) कॉपर के शुद्धिकरण में वैद्युत अपघटनी विधि का प्रयोग किया जाता है।
(ii) ऐलुमिनियम का मुख्य अयस्क बॉक्साइट (Al2O3 . 2H2O) है। ऐलुमिनियम के निष्कर्षण में निक्षालन के महत्व की व्याख्या के लिए बॉक्साइट से ऐलुमिना का निक्षालन, बेयर की विधि – निक्षालन विधि से मुख्यतः ऐलुमिनियम के अयस्क बॉक्साइट का सान्द्रण किया जाता है। बॉक्साइट (Al2O3.2H2O) में मुख्यतः सिलिका (SiO2), आयरन ऑक्साइड (Fe2O3) तथा टाइटेनियम ऑक्साइड (TiO2) की अशुद्धियाँ होती हैं।
ऐलुमिना से सिलिका इत्याद को पृथक् करने के लिए 473 – 523K ताप तथा 35 bar दाब पर चूर्ण किए हुए अयस्क को सान्द्र NaOH विलयन से क्रिया कराकर सान्द्रित किया जाता है, चूँकि SiO2 अम्लीय, Al2O3 उभयधर्मी तथा NaOH क्षारीय हैं, अतः इनकी क्रिया से Al2O3, सोडियम ऐलुमिनेट के रूप में एवं SiO2 सोडियम सिलिकेट के रूप में प्राप्त होता है, जो जल में विलेय होने के कारण निक्षालित हो जाते हैं तथा अन्य अशुद्धियाँ बच जाती हैं।
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na [A]
जल में विलेय सोडियम ऐलुमिनेट विलयन में CO2 गैस प्रवाहित करने से ऐलुमिनेट उदासीन होंकर जलयोजित Al2O3 के रूप में अवक्षेपित हो जाता है। यहाँ पर विलयन में थोड़ा-सा ताजा बना जलयोजित Al2O3 डालने पर अवक्षेपण की दर बढ़ जाती है। इसे बीजारोपण कहा जाता है।
2Na[Al(OH)4](aq) + 2CO2(g) → Al2O3 . 2H2O(s) + 2NaHCO3(aq) + H2O
सोडियम सिलिकेट विलयन में बच जाता है तथा जलयोजित ऐलुमिना को छानकर, सुखाकर, गरम करने से पुनः शुद्ध Al2O3 प्राप्त हो जाता है।
![]()
प्रश्न 13.
निम्नलिखित विधियों द्वारा धातुओं के शोधन में प्रयुक्त सिद्धान्तों की विवेचना कीजिए-
(i) वाष्प अवस्था परिष्करण
(ii) मंडल परिष्करण।
उत्तर:
(i) वाष्प प्रावस्था परिष्करण – शोधन की इस विधि में, धातु को वाष्पशील यौगिक में बदल कर उसे दूसरी जगह एकत्रित कर लेते हैं तथा इस वाष्पशील यौगिक के विघटन से शुद्ध धातु प्राप्त कर ली जाती है। इस विधि के लिए दो शर्तें आवश्यक हैं-
(i) उपलब्ध अभिकर्मक के साथ धातु वाष्पशील यौगिक बनाती हो तथा
(ii) वाष्पशील पदार्थ आसानी से विघटित होने वाला हो, ताकि धातु आसानी से पुनः प्राप्त की जा सके। इस विधि से Zr, Ti तथा Ni का शोधन किया जाता है।
उदाहरण:
(a) निकल के शोधन की मॉन्ड की विधि-इस विधि में Ni को CO के प्रवाह में गर्म करने पर वाष्पशील संकुल यौगिक निकल टेट्राकार्बोनिल बनता है, जिसे उच्च ताप पर गर्म करने पर इसके विघटन से शुद्ध निकैल प्राप्त हो जाता है। इस प्रकार निकल से अशुद्धियाँ पृथक् हो जाती हैं।

(b) जर्कोनियम या टाइटेनियम के शोधन के लिए वॉनआरकैल विधि – यह विधि Zr तथा Ti जैसी धातुओं से अशुद्धियों के रूप में उपस्थित ऑक्सीजन तथा नाइट्रोजन को हटाने में प्रयुक्त की जाती है। अपरिष्कृत धातु को निर्वातित पात्र में आयोडीन के साथ गरम करते हैं, जिससे धातु आयोडाइड बनता है। यह अधिक सहसंयोजी होने के कारण आसानी से वाष्पीकृत हो जाता है तथा अशुद्धि बच जाती है।
Zr + 2I2 → Zrl4
धातु आयोडाइड को 1800K ताप पर विद्युत द्वारा गरम किए गए टंग्टन तंतु पर गर्म किया जाता है, जिससे यह विघटित होकर शुद्ध धातु देता है जो कि तंतु पर जमा हो जाती है।
Zrl4 → Zr + 2I2
(ii) मंडल परिष्करण या जोन परिष्करण – मंडल परिष्करण द्वारा अतिशुद्ध धातु प्राप्त होती है। यह विधि इस सिद्धान्त पर आधारित है कि अशुद्धियों की विलेयता धातु की ठोस अवस्था की अपेक्षा गलित अवस्था में अधिक होती है। इस विधि में अशुद्ध धातु की छड़ के एक किनारे पर एक वृत्ताकार गतिशील हीटर (तापक) लगा होता है। जो छड़ को हर तरफ से घेरे रहता है। हीटर जैसे ही आगे बढ़ता है, गलित मण्डल भी आगे बढ़ता जाता है और गलित से शुद्ध धातु क्रिस्टलित हो जाती है तथा अशुद्धियाँ पास वाले गलित जोन में चली जाती हैं।
इस प्रक्रिया को कई बार दोहराते हैं तथा हीटर को एक ही दिशा में बार-बार चलाते जाते हैं। अशुद्धियाँ छड़ के एक किनारे पर एकत्रित हो जाती हैं, जिसे काटकर अलग कर लेते हैं। इस विधि से अति शुद्ध अर्धचालकों तथा अन्य शुद्ध धातुओं; जैसे-जर्मेनियम, सिलिकॉन, बोरॉन, गैलियम तथा इंडियम को प्राप्त किया जाता है।
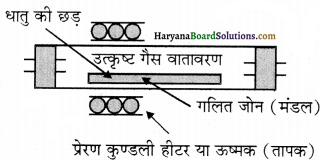
![]()
प्रश्न 14.
निक्षालित निम्न कोटि अयस्क से कॉपर प्राप्त करने के लिए कौनसा अपचायक प्रयुक्त किया जाता है?
उत्तर:
निक्षालित निम्न कोटि अयस्क से कॉपर प्राप्त करने के लिए हाइड्रोजन या रद्दी आयरन (स्क्रेप आयरन) का अपचायक के रूप में प्रयोग किया जाता है।
प्रश्न 15.
ऐलुमिनियम के निष्कर्षण के लिए वैद्युत अपघटनी सेल का नामांकित चित्र बनाइए एवं इसमें होने वाली सम्पूर्ण अभिक्रिया लिखिए।
अथवा
मंडल परिष्करण प्रक्रम का नामांकित चित्र बनाइए। यह विधि मुख्य रूप से किसमें उपयोगी है?
उत्तर:
ऐलुमिनियम के निष्कर्षण के लिए वैद्युत अपघटनी सेल का नामांकित चित्र निम्न है-
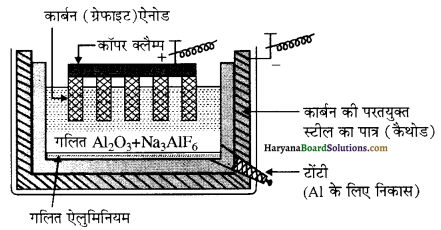
इस प्रक्रम में होने वाली सम्पूर्ण अभिक्रिया को निम्न प्रकार लिखा जा सकता है-
2Al2O3 + 3C → 4Al + 3CO2
अधवा
मंडल परिष्करण प्रक्रम का नामांकित चित्र निम्न है
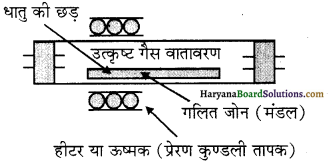
प्रश्न 16.
निस्तापन तथा भर्जन को उदाहरण सहित समझाइए।
उत्तर:
निस्तापन-निस्तापन में अयस्क को धातु के गलनांक से नीचे के ताप पर वायु की अनुपस्थिति में धीर-धीरे गर्म करते हैं जिससे वाष्पशील पदार्थ जैसे CO2, H2O इत्यादि निकल जाते हैं तथा धातु ऑक्साइड बच जाता है।
![]()
भर्जन-भर्जन प्रक्रम में सल्फाइड अयस्कों को वायु की उपस्थिति में धातु के गलनांक से नीचे के ताप पर गर्म करते हैं जिससे सल्फाइड, ऑक्साइड में परिवर्तित हो जाते हैं तथा S, P, As, Sb इत्यादि की अशुद्धियाँ वाष्पशील ऑक्साइड के रूप में निकल जाती हैं।
उदाहरण – 2Cu2S + 3O2 → 2Cu2O + 2SO2
प्रश्न 17.
(i) टाइटेनियम के परिष्करण के लिए प्रयुक्त होने वाली विधि का नाम लिखिए।
(ii) सिल्वर के निष्कर्षण में Zn की क्या भूमिका होती है?
(iii) धातु ऑक्साइड का धातु में अपचयन सरल हो जाता है यदि प्राप्त धातु द्रव अवस्था में हो। क्यों?
उत्तर:
(i) टाइटेनियम के परिष्करण के लिए वॉन-ऑरकेल विधि का प्रयोग किया जाता है।
(ii) सिल्वर के निष्कर्षण में Zn मिलाने पर सिल्वर के संकुल Na[Ag(CN)2] में उपस्थित Ag का विस्थापन होकर Zn का संकुल बन जाता है तथा सिल्वर प्राप्त हो जाती है। यह Zn अपचायक का कार्य करता है।
(iii) जब धातु ठोस अवस्था की अपेक्षा द्रव अवस्था में होती है तो उसकी एन्ट्रॉपी अधिक होती है। जब निर्मित धातु द्रव अवस्था में होती है और अपचयित होने वाली धातु ऑक्साइड ठोस अवस्था में होती है तो अपचयन प्रक्रम के एन्ट्रॉपी परिवर्तन (△S) का मान अधिक धनात्मक हो जाता है। अतः △G° का मान अधिक ऋणात्मक हो जाता है और अपचयन आसान हो जाता है।