Haryana State Board HBSE 11th Class Chemistry Important Questions Chapter 11 p-ब्लॉक तत्त्व Important Questions and Answers.
Haryana Board 11th Class Chemistry Important Questions Chapter 11 p-ब्लॉक तत्त्व
बहुविकल्पीय प्रश्न:
1. बॉक्साइट निम्नलिखित में से किस धातु का अयस्क है ?
(1) जिंक
(2) कॉपर
(3) एलुमिनियम
(4) आयरन।
उत्तर:
(3) एलुमिनियम
2. बोरेक्स बीड परीक्षण में नीली बीड बनाएगा-
(1) Cr3+
(2) Co2+
(3) Ni2+
(4) Cd2+
उत्तर:
(2) Co2+
3. बोरेक्स का रासायनिक नाम है-
(1) सोडियम मेटा बोरेट
(2) सोडियम टेट्राबोरेट डेकाहाइड्रेट
(3) सोडियम टेट्राबोरेट
(4) सोडियम आर्थोबोरेट।
उत्तर:
(2) सोडियम टेट्राबोरेट डेकाहाइड्रेट
4. B2O3 है-
(1) अम्लीय
(2) उभयधर्मी
(3) भास्मिक
(4) आयनिक।
उत्तर:
(1) अम्लीय
5. लीथियम एलम नहीं बना सकता है, क्योंकि-
(1) यह उच्च वैद्युत धनात्मक है
(2) इसका आकार छोटा होता है
(3) इसकी आयनन ऊर्जा अधिक होती है
(4) यह क्रियाशील धातु है।
उत्तर:
(2) इसका आकार छोटा होता है
6. गीली हवा में AlCl3 धुआँ देता है क्योंकि यह है-
(1) सहसंयोजी है
(2) वाष्पशील है
(3) जलग्राही है
(4) गीली हवा में HCl बनाता है।
उत्तर:
(4) गीली हवा में HCl बनाता है।
![]()
7. थर्माइट एक मिश्रण है, आयरन ऑक्साइड तथा-
(1) Al चूर्ण
(2) Zn चूण
(3) Mg चूर्ण
(4) Cd चूर्ण।
उत्तर:
(1) Al चूर्ण
8. एलुमिनियम क्लोराइड है-
(1) ब्रांस्टेड-लॉरी अम्ल
(2) आर्हीनियस अम्ल
(3) लूइस अम्ल
(4) लूइस क्षार।
उत्तर:
(3) लूइस अम्ल
9. हॉल विधि में, मुख्य अभिकर्मक के साथ मिश्रित किया जाता है-
(1) NaF
(2) Na3AlF6
(3) AlF3
(4) इनमें से कोई नहीं।
उत्तर:
(2) Na3AlF6
10. कीचड़युक्त (mudy) जल में एलम मिलाया जाता है-
(1) यह रोगाणुनाशक का कार्य करता है
(2) यह मिट्टी तथा बालू का स्कन्दन कर देता है
(3) मिट्टी एलम में विलेय है। अतः यह इन्हें प्रथक् कर देता है
(4) यह जल को क्षारीय कर देता है जो स्वास्थ्य के लिए अच्छा है।
उत्तर:
(2) यह मिट्टी तथा बालू का स्कन्दन कर देता है
11. क्रोमियम (Cr) क पेरेक्स बीड परीक्षण है-
(1) हरा
(2) नीला
(3) बैंगनी
(4) भूरा।
उत्तर:
(1) हरा
12. AlCl3 के डाइमर में बन्ध होते हैं-
(1) आयनिक
(2) सहसंयोजक
(3) आयनिक तथा सहसंयोजक
(4) सहसंयोजक तथा उप-सहसंयोजक।
उत्तर:
(4) सहसंयोजक तथा उप-सहसंयोजक।
13. बोरेक्स तैयार किया जाता है, कोलेमेनाइट की क्रिया कराकर-
(1) NaNO3 से
(2) NaCl से
(3) Na2CO3 से
(4) NaHCO3 से ।
उत्तर:
(3) Na2CO3 से
14. निम्न में कौन-सा तत्त्व भू-पर्पर्टी में बहुतायत में पाया जाता है-
(1) B
(2) Al
(3) Ga
(4) In
उत्तर:
(2) Al
15. Al की क्रियाशीलता आयरन से अधिक है लेकिन यह आयरन से कम संक्षारित होता है क्योंकि-
(1) Al उत्कृष्ट धातु है
(2) Al के ऊपर ऑक्सीजन की एक परिरक्षी ऑक्साइड की परत बनती है
(3) Fe जल के साथ सरलता से क्रिया करता है
(4) Fe एक संयोजी तथा द्वि-संयोजी आयन बनाता है।
उत्तर:
(2) Al के ऊपर ऑक्सीजन की एक परिरक्षी ऑक्साइड की परत बनती है
16. एलुमिनियम अनेक धातु ऑक्साइडों को अपचयित करता है क्योंकि इसकी अधिक बन्धुता होती है-
(1) ऑक्सीजन के लिए
(2) धातुओं के लिए
(3) इलेक्ट्रॉनों के लिए
(4) हाइड्रोजन के लिए।
उत्तर:
(2) धातुओं के लिए
17. ड्यूरेलुमिन मिश्र धातु में ऐलुमिनियम के साथ होता है-
(1) निकिल
(2) मैग्नीशियम तथा निकिल
(3) मैग्नीशियम, मैगनीज तथा कॉपर
(4) मैग्नीशियम, निकिल तथा मैगनीज।
उत्तर:
(3) मैग्नीशियम, मैगनीज तथा कॉपर
18. आयरन ऑक्साइड की अशुद्धि वाले बॉक्साइट खनिज की शोधन विधि को कहते हैं-
(1) हूप विधि
(2) सर्पेक विधि
(3) बेयर प्रक्रम
(4) विद्युत अपघटन प्रक्रम।
उत्तर:
(3) बेयर प्रक्रम
19. कपड़ा रंगने वाले फिटकरी का प्रयोग करते हैं-
(1) कपड़ों को अग्निरोधक बनाने के लिए
(2) कटे हुए पर प्राथमिक उपचार के लिए
(3) कठोर जल को मृदु बनाने के लिए
(4) रंग-बन्धक की तरह।
उत्तर:
(4) रंग-बन्धक की तरह।
20. निम्न में से कौन गर्म करने पर ऊर्ध्वपातित होता है-
(1) AlF3
(2) AlBr3
(3) Al2Cl6
(4) AlI3
उत्तर:
(2) AlBr3
21. थर्माइट वेल्डिंग प्रक्रम में, हम प्रयुक्त करते हैं-
(1) Al चूर्ण
(2) Fe चूर्ण
(3) Ca चूर्ण
(4) Al + Fe चूर्ण।
उत्तर:
(4) Al + Fe चूर्ण।
22. निम्न में से कौन III-A समूह से सम्बन्धित नहीं है-
(1) B
(2) Al
(3) Ge
(4) In
उत्तर:
(3) Ge
![]()
23. ऐलुमिनियम का प्रमुख अयस्क है-
(1) बॉक्साइट
(2) डोलोमाइट
(3) गैलेना
(4) फेलस्पार।
उत्तर:
(1) बॉक्साइट
24. निम्न में से कौन-सा ऐलुमिनियम का खनिज नहीं है-
(1) ऐनहाइड्राइड
(2) बॉक्साइट
(3) कोरण्डम
(4) डायस्पोर।
उत्तर:
(1) ऐनहाइड्राइड
25. बोरेक्स का सूत्र है-
(1) Na2B4O7
(2) Na2B4O7.4H2O
(3) Na2B4O7.7H2O
(4) Na2B4O7.10H2O
उत्तर:
(4) Na2B4O7.10H2O
26. बोरॉन एक
(1) धातु है
(2) अधातु है
(3) उप-धातु है
(4) यौगिक है।
उत्तर:
(3) उप-धातु है
27. निम्न में से कौन-सा तत्व अक्रिय युग्म प्रभाव दिखाता है-
(1) B
(2) Al
(3) Tl
(4) Sc
उत्तर:
(3) Tl
28. कौन-सी धातु अपने ऑक्साइड की परत द्वारा रक्षित होती है ?
(1) Al
(2) Au
(3) Fe
(4) Ag
उत्तर:
(1) Al
29. क्रायोलाइट अयस्क है-
(1) Fe का
(2) Al का
(3) Cu का
(4) Ag का।
उत्तर:
(2) Al का
30. ऑर्थो-बोरिक अम्ल में बोरॉन का संकरण, कौन-से संकरित ऑर्बिटल देता है ?
(1) sp
(2) sp2
(3) sp3
(4) sp3d
उत्तर:
(2) sp2
31. बोरेक्स का जलीय विलयन होता है-
(1) अम्लीय
(2) क्षारीय
(3) उदासीन
(4) विरंजक।
उत्तर:
(2) क्षारीय
32. डादबोरेन से B का संकरण है-
(1) sp
(2) sp2
(3) sp3
(4) sp3d
उत्तर:
(3) sp3
33. कौन-सा मेटाबोरिक अम्ल है-
(1) HBO2
(2) H2B4O7
(3) B(OH)3
(4) H3BO3
उत्तर:
(1) HBO2
34. ऐल्युमीनियम उपस्थित है-
(1) अल्ट्रामैराइन में
(2) लापिस लाजुली में
(3) रूबी में
(4) इन सभी में।
उत्तर:
(4) इन सभी में।
35. निम्न में लूईस अम्ल है-
(1) PCl3
(2) AlCl3
(3) NCl3
(4) AsCl3
उत्तर:
(2) AlCl3
36. ऐलुमिना है-
(1) अम्लीय
(2) उभयधर्मी
(3) क्षारीय
(4) उदासीन।
उत्तर:
(2) उभयधर्मी
37. वर्ग संख्या-13 का अधात्विक तत्व. है-
(1) B
(2) Al
(3) Ga
(4) In.
उत्तर:
(1) B
38. निम्न में से कौन रोगग्रस्त आँखों को धोने में प्रयुक्त होता है-
(1) Na2CO3
(2) Na2B4O7. 10H2O
(3) NaHCO3
(4) NaCl
उत्तर:
(2) Na2B4O7. 10H2O
39. बोरेक्स प्राप्त करने हेतु कोलेमेनाइट को उबालते हैं-
(1) Na2CO3 के साथ
(2) Na2SO4 के साथ
(3) NaCl के साथ
(4) NaOH के साथ।
उत्तर:
(1) Na2CO3 के साथ
40. बोरेक्स या सुहागा का रासायनिक संगठन है-
(1) CaSO4.B4O7.H2O
(2) MgSO4.B2O4.2H2O
(3) Na2B4O7.10H2O
(4) MgCl2.B4O10.10H2O
उत्तर:
(3) Na2B4O7.10H2O
41. रॉकेट में ईंधन के रूप में प्रयुक्त होते हैं-
(1) बोरॉन के हाइड्राइड्स
(2) एल्यूमीनियम के हाइड्राइड्स
(3) गैलियम के हाइड्राइड्स
(4) इण्डियम के हाइड्राइड्स।
उत्तर:
(1) बोरॉन के हाइड्राइड्स
42. ऊष्मा और विद्युत का अच्छा चालक है-
(1) एस्थ्रेसाइट
(2) हीरा
(3) चारकोल
(4) श्रेफाइ्त।
उत्तर:
(4) श्रेफाइ्त।
43. हीरा तथा ग्रेफाइट हैं-
(1) समाबयवी
(2) समस्थानिक
(3) अपररूप
(4) बहुलक।
उत्तर:
(3) अपररूप
![]()
44. निम्न में सबसे अधिक आयनिक यौगिक है-
(1) PbCl2
(2) PbCl4
(3) CCl4
(4) SiCl4
उत्तर:
(1) PbCl2
45. निम्न में कौन-सा अल में अघुलनशील है ?
(1) CuSO4
(2) CdSO4
(3) PbSO4
(4) Bi2(SO4)3
उत्तर:
(3) PbSO4
46. सौर-सेल में किस पदार्थ का उपयोग होता है ?
(1) Cs
(2) Si
(3) Sn
(4) Ti
उत्तर:
(2) Si
47. कोल गैस के प्रमुख अवयव हैं-
(1) CO + N2
(2) CO + H2
(3) CH4 + H2
(4) CH4 + N2
उत्तर:
(3) CH4 + H2
48. निम्नलिखित में किसका कैलोरीमान अधिकतम है ?
(1) कोल गैस
(2) जल गैस
(3) प्रोइ्यूसर गैस
(4) कार्बन द्वाइ-औक्साइड।
उत्तर:
(1) कोल गैस
49. काँच क्या है ?
(1) द्रव
(2) ठोस
(3) अविशीतित द्रव
(4) पारदर्शक कार्बनिक बहुलक।
उत्तर:
(3) अविशीतित द्रव
50. काँच के औद्योगिक निर्माण में प्रयुक्त कच्चे पदार्थ हैं-
(1) रेत, लाइम स्टोन तथा Na2CO3
(2) रेत, लाइम स्योन तथा NaCl
(3) रेत, जिप्सम तथा Na2CO3
(4) रेत, कास्टिक सोड्या तथा लाइम स्टोन।
उत्तर:
(3) रेत, जिप्सम तथा Na2CO3
51. प्रोड्यूसर गैस मिश्रण है-
(1) CO + N2
(2) CO + H2
(3) CO + जलबाष्प
(4) N2 + CH4
उत्तर:
(1) CO + N2
52. रेड लेड है-
(1) PbO
(2) Pb2O3
(3) Pb3O4
(4) Pb
उत्तर:
(3) Pb3O4
53. सफेद लेड है-
(1) PbSO4
(2) Pb(OH)2
(3) PbO
(4) 2PbCO3.Pb(OH)2
उत्तर:
(3) PbO
54. गैलना एक अयस्क है, इससे प्राप्त धातु है-
(1) गैलियम
(2) लेड
(3) टिन
(4) जर्मेनियम।
उत्तर:
(2) लेड
55. निम्न में कौन-सी धातु बन्दूक की गोली बनाने के काम आती है-
(1) Pb
(2) Sn
(3) Fe
(4) Cu
उत्तर:
(1) Pb
56. एक पदार्थ का जलीय विलयन तनु HCl से क्रिया कराने पर सफेद अवक्षेप देता है जो गर्म करने पर विलेय हो जाता है। इस गर्म अम्लीय विलयन में जब H2S प्रवाहित की जाती है तो काला अवक्षेप प्राप्त होता है। पदार्थ है-
(1) Hg22+ लवण
(2) Cu2+ लवण
(3) Ag2+ लवण
(4) Pb2+ लवण।
उत्तर:
(4) Pb2+ लवण।
57. नवीनतम खोजा गया कार्बन का अपररूप है-
(1) C16
(2) C60
(3) C26
(4) C56
उत्तर:
(2) C60
58. बकमिन्स्टर फुलरीन है-
(1) C60 का खोजकर्ता
(2) कार्बन का एक अपररूप
(3) टिन का एक अयस्क
(4) लेड का एक यौगिक।
उत्तर:
(2) कार्बन का एक अपररूप
59. C, N, P और Si तत्त्वों की विद्युत ऋणात्मकता के बढ़ने का क्रम है-
(1) C, N, Si, P
(2) N, Si, C, P
(3) Si, P, C, N
(4) P, Si, N, C
उत्तर:
(3) Si, P, C, N
60. अक्रिय युग्म प्रभाव प्रदर्शित करता है-
(1) कार्बन
(2) सिलिकन
(3) लेड
(4) ऐलुमिनियम।
उत्तर:
(3) लेड
61. एक आदर्श अर्द्ध-चालक बनाया जाता है-
(1) ग्रेफाइट से
(2) कार्बन से
(3) सिलिकॉन से
(4) सीसे से।
उत्तर:
(3) सिलिकॉन से
62. निम्न में अत्यधिक कठोर पदार्थ है-
(1) हीरा
(2) ग्रेफाइट
(3) फुलेरीन
(4) कार्बेरिण्डम।
उत्तर:
(1) हीरा
63. समूह- 4 का तत्व जो बहुबन्ध नहीं बना सकता है, वह है-
(1) C
(2) Si
(3) Sn
(4) Pb
उत्तर:
(2) Si
64. निम्न में से कौन चूने के पानी को दूधिया कर देता है-
(1) CO2
(2) CO
(3) NO2
(4) Cl2
उत्तर:
(1) CO2
65. फॉस्जीन गैस का रासायनिक नाम है-
(1) फॉस्फीन
(2) कार्बोनिल क्लोराइड
(3) फॉस्फोरस ट्राइक्लोराइड
(4) फॉस्फोरस ऑक्सी क्लोराइड।
उत्तर:
(2) कार्बोनिल क्लोराइड
![]()
66. प्रयोगशाला के बर्नरों में हम प्रयुक्त करते हैं-
(1) प्रोड्यूसर गैस
(2) तेल गैस
(3) कोल गैस
(4) गोबर गैस।
उत्तर:
(2) तेल गैस।
67. संश्लेषित गैस किसका मिश्रण है-
(1) भाप + CO
(2) CO + N2
(3) H2 + CO
(4) H2 + CH4
उत्तर:
(3) H2 + CO
68. निम्न में से किसका गलनांक सर्वाधिक है ?
(1) लैड
(2) हीरा
(3) लोहा
(4) सोडियम।
उत्तर:
(2) हीरा
69. निम्न में से कौन-सा तत्व मुक्त अवस्था में पाया जाता है-
(1) C
(2) Si
(3) Ge
(4) Sn
उत्तर:
(1) C
70. उदासीन ऑक्साइड है-
(1) ZnO
(2) CO
(3) SO
(4) SnO
उत्तर:
(2) CO
71. सिलिकॉन निम्न में से किसका महत्त्वपूर्ण अवयव है-
(1) क्लोरोफिल
(2) चट्टान
(3) हीमोग्लोबिन
(4) अमलगम।
उत्तर:
(2) चट्टान
72. बेल मेटल किसकी मिश्र धातु है-
(1) Cu + Sn
(2) Cu + Ni
(3) Cu + Zn
(4) Cu + Pb
उत्तर:
(1) Cu + Sn
73. कौन शुष्क बर्फ है-
(1) बिना जल की ठोस बर्फ
(2) ठोस SO2
(3) ठोस CO2
(4) ठोस C6H6
उत्तर:
(2) ठोस SO2
74. CO जो कि एक विषैली गैस है, CO का प्रतिरोधी है-
(1) कार्बोरण्डम
(2) शुद्ध CO2
(3) कार्बोजन
(4) COCl2
उत्तर:
(3) कार्बोजन
75. चारकोल है-
(1) क्रिस्टलीय अपररूप
(2) अक्रिस्टलीय अपररूप
(3) आर्द्रताग्राही अपररूप
(4) उत्फुल्ल अपररूप।
उत्तर:
(2) अक्रिस्टलीय अपररूप
76. निम्न में कौन-सा तत्व अपररूपता प्रदर्शित नहीं करता है-
(1) C
(2) Si
(3) Sn
(4) Pb
उत्तर:
(4) Pb
77. निम्न में से कार्बन का सर्वाधिक शुद्ध अपररूप है-
(1) काष्ठ चारकोल
(2) जन्तु चारकोल
(3) लैम्प कालिख
(4) ग्रेफाइट।
उत्तर:
(4) ग्रेफाइट।
78. लैड शर्करा है-
(1) 2PbSO4.PbO
(2) (CH3COO)2Pb
(3) Pb3O4
(4) PbCO3.Pb(OH)2
उत्तर:
(2) (CH3COO)2Pb
79. रासायनिक रूप से लिथार्ज है-
(1) PbO
(2) PbO2
(3) Pb3O4
(4) Pb(CH3COO)2
उत्तर:
(1) PbO
80. किसी पदार्थ के दो या अधिक क्रिस्टलीय रूपों में अस्तित्व में रहने का गुण कहलाता है-
(1) समावयवता
(2) बहुसमाकृतिकता
(3) समाकृतिकता
(4) असमाकृतिकता।
उत्तर:
(2) बहुसमाकृतिकता
81. हीरे में कार्बन परमाणुओं को परस्पर बाँधने वाला बल होता है-
(1) आयनिक
(2) सहसंयोजी
(3) द्विध्रुवीय
(3) वाण्डरवाल।
उत्तर:
(2) सहसंयोजी
82. छद्म ठोस है-
(1) हीरा
(2) काँच
(3) चट्टानी लवण
(4) संगमरमर।
उत्तर:
(2) काँच
83. ग्रेफाइट में इलेक्ट्रॉन-
(1) प्रत्येक तीसरे कार्बन पर स्थानीकृत होते हैं
(2) प्रतिआबन्धन कक्षकों में होते हैं
(3) प्रत्येक कार्बन परमाणु पर स्थानीकृत होते हैं
(4) संरचना के बीच फैले होते हैं।
उत्तर:
(4) संरचना के बीच फैले होते हैं।
अति लघु उत्तरीय प्रश्न:
प्रश्न 1.
बोरॉन के दो महत्त्वपूर्ण अयस्क बताइए।
उत्तर:
- बोरेक्स Na2B4O7.10H2O
- कारनाइट Na2B4O7.2H2O
प्रश्न 2.
बोरॉन के दो समस्थानिकों के नाम बताइए।
उत्तर:
5B10 तथा 5B11 बोरॉन के दो समस्थानिक हैं।
![]()
प्रश्न 3.
एक सेतु आबन्ध के द्वारा कितने परमाणु परस्पर जुड़ते हैं?
उत्तर:
तीन परमाणु।
प्रश्न 4.
बोरॉन के दो अपररूपों के नाम बताइए।
उत्तर:
सरन्ध्र तथा क्रिस्टलीय बोरॉन।
प्रश्न 5.
क्रिस्टलीय बोरॉन कठोर ठोस क्यों होता है ?
उत्तर:
प्रबल सहसंयोजक बन्धों के कारण क्रिस्टलीय बोरॉन कठोर होता है।
प्रश्न 6.
बोरॉन को नाभिकीय रिऐक्टर में प्रयोग क्यों किया जाता है ?
उत्तर:
बोरॉन न्यूट्रॉनों को अवशोषित कर सकता है; अतः इसका प्रयोग नाभिकीय रिऐक्टर में किया जाता है।
प्रश्न 7.
टिंकल क्या है ? इसका रासायनिक सूत्र दीजिए।
उत्तर:
टिंकल (अथवा बोरेक्स) बोरॉन का एक अयस्क है। इसका सूत्र Na2B4O7.10H2O है।
प्रश्न 8.
बोरॉन Si से समानता क्यों दर्शाता है ?
उत्तर:
दोनों में आवेश/त्रिज्या का अनुपात समान होता है अर्थात् समान ध्रुवण-क्षमता होती है; इसीलिए दोनों समानता दर्शाते हैं।
प्रश्न 9.
बोरॉन स्थायी इलेक्ट्रॉन-न्यून यौगिक क्यों बनाता है ?
उत्तर:
बोरॉन में तीन संयोजी इलेक्ट्रॉन होते हैं। यह अन्य तत्वों से तीन इलेक्ट्रॉनों का साझा करके इलेक्ट्रॉन-न्यून यौगिक बनाता हैं जो स्थायी होते हैं।
प्रश्न 10.
बोरिक अम्ल (H3BO3) एकल क्षारकीय अम्ल क्यों होता है ?
उत्तर:
यह H2O के OH– आयन से इलेक्ट्रॉनों का एक युग्म ग्रहण करता है; इसलिए यह एकलक्षारकीय अम्ल होता है।
प्रश्न 11.
किस प्रकार का काँच प्राप्त होता है जब बोरेक्स मिलाया जाता है ?
उत्तर:
पाइरेक्स काँच। यह ऊष्मीय प्रतिरोधक होता है तथा उच्च ताप सह सकता है।
प्रश्न 12.
BH3 डाइबोरेन के रूप में क्यों उपस्थित होता है
उत्तर:
BH3 डाइबोरेन के रूप में उपस्थित होता है; क्योंकि यह सरलतापूर्वक इलेक्ट्रॉन त्याग अथवा ग्रहण कर सकता है। अतः दो BH3 अणु आपस में संयोजन B2H6 करके बनाता है।
प्रश्न 13.
बोरॉन द्वारा किंस प्रकार के बन्ध बनाए जाते हैं तथा क्यों ?
उत्तर:
बोरॉन सह-संयोजक बन्ध बनाता है क्योंकि यह न तो इलेक्ट्रॉन त्याग सकता है और न ही उसे ग्रहण कर सकता है।
प्रश्न 14.
ऑर्थोबोरिक अम्ल की मूल संरचनात्मक इकाई क्या है ? इनमें उपस्थित बन्ध के प्रकार का नाम बताइए।
उत्तर:
ऑर्थोबोरिक अम्ल की मूल संरचनात्मक इकाई \(\mathrm{BO}_3{ }^{3-}\) है। इनमें सहसंयोजी बन्ध उपस्थित होते हैं।
प्रश्न 15.
औद्योगिक प्रक्रमों में BF3 उत्प्रेरक के रूप में किस प्रकार का कार्य करता है ?
उत्तर:
BF3 इलेक्ट्रॉन न्यून होता है; इसलिए औद्योगिक प्रक्रमों में उत्प्रेरक के रूप में कार्य करता है।
प्रश्न 16.
BCl3 की तुलना में BF3 दुर्बल लूइस अम्ल क्यों होता है ?
उत्तर:
BCl3 की तुलना में BF3 दुर्बल लूइस अम्ल होता है; क्योंकि Cl की तुलना में F के छोटे आकार के कारण F की स्थिति में अधिक प्रभावी पश्चगामी बन्ध (back bonding) बनता है।
प्रश्न 17.
बोरेन में उपस्थित तत्वों के नाम लिखिए।
उत्तर:
बोरेन, बोरॉन तथा हाइड्रोजन तत्वों से मिलकर बना होता है।
प्रश्न 18.
BF3 में B की संकरण-अवस्था लिखिए।
उत्तर:
BF3 में B की संकरण-अवस्था sp2 होती है।
प्रश्न 19.
बोरिक अम्ल लूइस अम्ल के समान व्यवहार क्यों करता है ?
उत्तर:
क्योंकि बोरिक अम्ल में, बोरॉन का अष्टक पूर्ण नहीं होता। यह जलीय विलयन में H2O से OH– आयन ग्रहण कर लेता है।
प्रश्न 20.
आवर्त सारणी के वर्ग 13 में बोरॉन के असंगत व्यवहार का मुख्य कारण क्या है ?
उत्तर:
इसका मुख्य कारण बोरॉन परमाणुं का छेटा आकार तथा उच्च आयनन ऊर्जा तथा उच्च आवेश/आकार अनुपात होता है।
प्रश्न 21.
बोरॉन हैलाइड अमोनिया तथा ऐमीन के साथ योगात्पक यौगिक क्यों बनाते हैं ?
उत्तर:
बोरॉन हैलाइड इलेक्ट्रॉन न्यून होते हैं; इसलिए ये अमोनिया तथा ऐमीन के साथ योगात्मक यौगिक बनाते हैं।
प्रश्न 22.
\(\mathrm{BH}_4^{-}\) में B की संकरण-अवस्था एवं ऑक्सीकरण अवस्था बताइये।
उत्तर:
sp3, + 3
प्रश्न 23.
AlF3 तथा ACCl3 के मध्य किसका गलनांक उच्च होता है ?
उत्तर:
AlF3 अधिक आयनिक होता है, इसलिए इसका गलनांक उच्च होता है।
प्रश्न 24.
निम्नलिखित तत्वों में कौन-सा +1 ऑक्सीकरण अवस्था प्रदर्शिंत करता है ?
Al, B, Ca, TL, Be
उत्तर:
Tl,+1 ऑकसीकरण अवस्था प्रदर्शित करता है।
प्रश्न 25.
निर्जलीय AlCl3 का कौन-सा गुण इसे कार्बनिक रसायन में एक अच्छा निर्माण अभिकर्मक बनाता है ?
उत्तर:
यह लूइस अम्ल के समान व्यवहार करता है।
प्रश्न 26.
निम्नलिखित को लूइस अम्ल गुण के बढ़ते क्रम में व्यवस्थित कीजिए-
BF3, BCl3, BBr3 तथा BI3
उत्तर:
BF3 < BCl3 < BBr3 < BI3
प्रश्न 27.
बोरॉन ट्राई ब्रोमाइड से शुद्ध क्रिस्टलीय बोरॉन प्राप्त करने की अभिक्रिया का समीकरण लिखिए।
उत्तर:
2BBr3 + 3H2 → 2B + 6HBr
प्रश्न 28.
बोरिक अम्ल के दो उपयोग लिखिए।
उत्तर:
- पूतिरोधी (संक्रमण रोधी) के रूप में।
- इनैमल और पॉटरी को चमकीला बनाने में प्रयुक्त होता है।
प्रश्न 29.
बोरॉन का एक उपयोग दीजिए।
उत्तर:
5B10 समसंथानिक का नाभिकीय रिएक्टर में नियन्त्रण छड़ों के रूप में प्रयोग किया जाता है।
प्रश्न 30.
डाई बोरेन कैसे प्राप्त करते हैं ?
उत्तर:
सोड्डियम बोरो हाइड्राइड पर आयोडीन की क्रिया द्वारा दाइ बोरेन प्राप्त की जाती है।
प्रश्न 31.
बोरॉन के दो अयस्कों के नाम बताओ ?
उत्तर:
- बोरेक्स (Na2B4O7.10H2O)
- करनाइट (Na2B4O7. 2H2O)
प्रश्न 32.
बोरॉन के दो आइसोटोप के नाम लिखो ?
उत्तर:
5B10 तथा 5B11 बोरॉन के दो आइसोटोप हैं।
प्रश्न 33.
बोरॉन के दो अपररूपों के नाम लिखो ?
उत्तर:
- क्रिस्टलीय,
- अक्रिस्टलीय
![]()
प्रश्न 34.
बोरॉन B3+ आयन क्यों नहीं बनाता ?
उत्तर:
बोरॉन B3+ आयन नहीं बनाता क्योंकि इसके आयनन विभव का मान अत्यधिक उच्च एवं परमाणु आकार काफी छोटा होता है।
प्रश्न 35.
क्रिस्टलीय बोरॉन एक कठोर ठोस है क्यों ?
उत्तर:
क्योंकि इसमें अत्यधिक प्रबल सह-संयोजी बंध पाये जाते हैं।
प्रश्न 36.
निम्न को पूर्ण करें-
(i) B + O2 →
उत्तर:
4B + 3O2 →2B2O3 (बोरॉन ऑक्साइड)
(ii) B + N2 →
उत्तर:
2B + N2 → 2BN (बोरॉन नाइट्राइड)
(iii) B + Cl2 →
उत्तर:
2B + 3Cl2 → 2BCl3 (बोरॉन ट्राइ-क्लोराइड)
(iv) BF3 + NH3 →
उत्तर:
BF3 + : NH3 →[F3B ← : NH3]
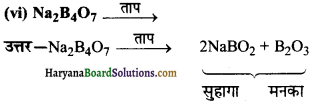
(v) Na2B4O7 + H2O →
उत्तर:
Na2B4O7 + H2O → 2NaOH + 4H3BO3 बोरिक अम्ल
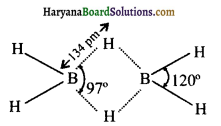
प्रश्न 37.
डाइ-बोरॉन की संरचना बनाइए।
उत्तर:
प्रश्न 38.
डाइ-बोरॉन अमोनिया तथा एमीन के साथ योगोत्पाद क्यों बनाता है ?
उत्तर:
क्योंकि यह एक इलेक्ट्रॉन न्यून यौगिक है।
प्रश्न 39.
विद्युत अपघटन से पूर्व Al2O3 का निर्जल होना आवश्यक है, क्यों ?
उत्तर:
क्योंकि जल की उपस्थिति में Al3+ का कैथोड पर विसर्जन न होकर H+ का विसर्जन होगा क्योंकि Al3+ का विसर्जन विभव H+ से अधिक होता है।
प्रश्न 40.
फिटकरी का सामान्य सूत्र क्या है ?
उत्तर:
इसका सामान्य सूत्र-
M2SO4.M2(SO4)3. 24H2O होता है।
यहाँ पर M = एक-संयोजी क्षारीय धातु या मूलक
M = त्रि-संयोजी क्षारीय धातु या मूलक।
प्रश्न 41.
बोरॉन का गलनांक सामान्य से अधिक होता है। क्यों ?
उत्तर:
क्योंकि यह ठोस तथा द्रव दोनों ही अवस्थाओं में एक बड़े सह-संयोजक बहुलक के रूप में रहता है।
प्रश्न 42.
BF3 के जल-अपघटन की अभिक्रिया लिखें।
उत्तर:
BF3 के जल-अपघटन की अभिक्रिया निम्न है-
BF3 + H2O → H+[BF3OH]–
प्रश्न 43.
एलुमीनियम का प्रयोग उन ऑक्साइडों को अपचयित करने में किया जाता है, जिनका अपचयन कार्बन नहीं कर पाता है। कारण स्पष्ट करो।
उत्तर:
क्योंकि एलुमीनियम कार्बन से प्रबल धनविद्युती तत्व व प्रबल अपचायक होता है।
प्रश्न 44.
AlCl3.6H2O को गर्म करके निर्जल AlCl3 को नहीं बनाया जा सकता है, क्योंकि ?
उत्तर:
AlCl3.6H2O गर्म करने पर निर्जल AlCl3 नहीं Al2O3 देता है।
प्रश्न 45.
क्या होता है जब BF3 की जल से अभिक्रिया होती है ?
उत्तर:
BF3 की जल से अभिक्रिया पर फ्लुओरोबोरिक अम्ल एवं ऑर्थोबोरिक अम्ल प्राप्त होता है।

प्रश्न 46.
B2H6 की HCl से अभिक्रिया लिखिए।
उत्तर:
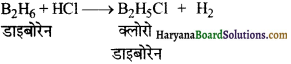
प्रश्न 47.
ड्यूरेलूमिन का प्रयोग हवाई जहाज बनाने में किया जाता है, क्यों ?
उत्तर:
यह Al, Cu, Mg तथा Mn की मिश्र धातु है जो हल्की परन्तु मजबूत होती है जिसके कारण इसका प्रयोग हवाई जहाज बनाने में किया जाता है।
प्रश्न 48.
बोरॉन के समस्थानिक बताएँ।
उत्तर:
बोरॉन के दो समस्थानिक होते हैं-
\(20 \%{ }_5^{10} \mathrm{~B}\) तथा \(80 \%{ }_5^{11} \mathrm{~B}\)
प्रश्न 49.
हीरे से कम कठोर अधात्विक तत्व का नाम बताएँ।
उत्तर:
बोरॉन \(\left({ }_5^{10} \mathrm{~B}\right)\)
प्रश्न 50.
बोरेक्स कैसे बनाते हैं ?
उत्तर:
कोलेमेनाइट पर जब Na2CO3 की क्रिया कराते हैं, तो बोरेक्स का निर्माण होता है।
प्रश्न 51.
ऐलुमिनियम के उस खनिज का नाम बताएँ जो कि साधारण फिटकरी बनाने में प्रयुक्त होता है।
उत्तर:
ऐलुनाइट का प्रयोग साधारण फिटकरी बनाने में करते हैं।
प्रश्न 52.
गैलियम का गलनांक बहुत कम होता है, क्यों ?
उत्तर:
क्योंकि गैलियम Ga2 अणु के रूप में होता है।
![]()
प्रश्न 53.
बोरेन क्या हैं ? इसका सामान्य सूत्र क्या होता है ?
उत्तर:
बोरॉन तथा हाइड्रोजन आपस में क्रिया करके वाष्पशील हाइड्राइड बनाते हैं। जिन्हें बोरेन (Boranes) कहते हैं। इनका सामान्य सूत्र BnHn+4 व BnHn+4 है।
प्रश्न 54.
एलेन से क्या समझते हो ?
उत्तर:
एलमीनियम के हाइड़ाइड को एलेन कहते हैं।
प्रश्न 55.
ऐलुमिना के वैद्युत-अपथटन में प्रयोग होने वाले गालक कौन-कौन से हैं ?
उत्तर:
ऐलुमिना के बैद्युत-अपषटन में क्रायोलाइट (Na3AlF6) तथा फ्लुओरस्पार (CaF2) का प्रयोग होता है।
प्रश्न 56.
बोरॉन की भू-पर्पटी में उपलब्तता कितने प्रतिशत है ?
उत्तर:
0.0001%
प्रश्न 57.
Al की भू-पर्पटी में उपलक्धता कितने प्रतिशत है ?
उत्तर:
8.3%
प्रश्न 58.
निम्न के सूत्र लिखें-
(i) और्थो बोरिक अम्ल,
(ii) बोरेक्स,
(iii) करनाइट,
(iv) बॉक्साइट,
(v) कायोलाइट।
उत्तर:
(i) और्थो बोरिक अम्ल – H3BO3
(ii) बोरेक्स – Na2B4O7.10H2O
(iii) करनाइट – Na2B4O7.4H2O
(iv) बॉक्साइ्ट – Al2O3. 2H2O
(v) क्रायोलाइट – Na3AlF6
प्रश्न 59.
Ga, In व TI तत्वों में +1 ऑक्सीकरण अवस्था प्रदर्शित करने की बङुती प्रवृत्ति दीजिए।
उत्तर:
Ga < ln < TI.
प्रश्न 60.
समूह- 13 के तत्वों में +3 ऑक्सीकरण अवस्था किसमें अधिकतम है ?
उत्तर:
बोरॉन (B) में ।
प्रश्न 61.
निर्जल AlCl3 की प्रकृति सहसंयोजी होती है जबकि जलयोजित AlCl3 वैद्युत संयोजी होता है, क्यों ?
उत्तर:
निर्जल लवप एक द्विलक (Al2Cl6) के रूप में होता है तथा यह सहसंयोजी प्रकृति का होता है। जब AlCl3 जल के सम्पर्क में आता है तो यह जलयोजित हो जाता है तथा जलयोजित लवप [Al(H3O)6]Cl3 को बनाता है। यह जल में आयनीकृत होकर [Al(H2O)6]3+ तथा 3Cl– आयन देता है।
प्रश्न 62.
क्या H3BO3 त्रिक्षारकीय है ?
उत्तर:
नहीं, यह एक क्षारीय है।
प्रश्न 63.
बोरिक अम्ल में BO3 की इकाइयाँ किस बन्ध के द्वारा आबन्धित रहती हैं ?
उत्तर:
बोरिक अम्ल में BO3 की इकाइयाँ हाइड्रोजन बन्ध के द्वारा आबन्धित रहती हैं।
प्रश्न 64.
बोरेक्स मनका परीक्षण के द्वारा किस प्रकार के धनायनों का परीक्षण करते हैं ?
उत्तर:
बोरेक्स मनका परीक्षण के द्वारा ऐसे धनायनौ का परीक्षण करते हैं जो कि रंगीन होते हैं।
प्रश्न 65.
समीकरण को पूर्ण करो-
Na2B4O7 + H2SO4 + 5H2O →… + Na2SO4
उत्तर:
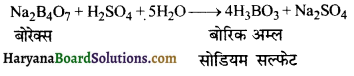
प्रश्न 66.
प्रकृति में कार्बन किस रूप में शुद्ध पाया जाता है ?
उत्तर:
फुलरीन।
प्रश्न 67.
हीरे में कार्बन का संकरण क्या होता है ?
उत्तर:
sp3
प्रश्न 68.
CO2 की संरचना दीजिए।
उत्तर:
O = C = O, इसकी रेखीय संरचना होती है।
प्रश्न 69.
क्या कार्बन डाइ-ऑक्साइड विषैली है ?
उत्तर:
नहीं, कार्बन डाइ-ऑक्साइड (CO2) विषैली नहीं होती।
प्रश्न 70.
प्रोड्यूसर गैस क्या है ?
उत्तर:
प्रोड्यूसर गैस CO तथा N2 का 1: 2 के अनुपात में भिश्रण है।
प्रश्न 71.
बकमिन्सटर फुलरीन किस तत्व का क्रिस्टलीय अपररूप होता है ?
उत्तर:
बकमिन्सटर फुलरीन कार्बन का क्रिस्टलीय अपररूप होता है।
प्रश्न 72.
\(\mathrm{CO}_3^{2-}\) की संकरण-अवस्था क्या है ?
उत्तर:
\(\mathrm{CO}_3^{2-}\) में C की संकरण-अवस्था sp2 होती है।
प्रश्न 73.
\(\mathrm{SiF}_5{ }^{2-}\) आयन में सिलिकन के संकर कक्षकों का प्रकार बताइए।
उत्तर:
sp3d2
प्रश्न 74.
किसी अन्य तत्व की तुलना में कार्बन सर्वाधिक श्रृंखलन क्यों दर्शाता है ?
उत्तर:
कार्बन सर्वाधिक श्रृंखलन प्रदर्शित करता है क्योंकि इसका परमाणु आकार छोटा होता है। यह अन्य कार्बन परमाणुओं के साथ स्थायी सहसंयोजक बन्ध बना सकता है।
प्रश्न 75.
कमरे के ताप पर CO2 गैस होती है, जबकि SiO2 ठोस। इसका एक कारण बताइए।
उत्तर:
CO2 एक विविक्त (discrete) अणु के रूप में होती है; इसलिए इसमें दुर्बल वाण्डरवाल्स आकर्षण बल होते हैं, जबकि SiO2 त्रिविमीय सहसंयोजी ठोस होता है। यही कारण है कि कमरे के ताप पर CO2 गैस व SiO2 ठोस है।
प्रश्न 76.
कार्बन तथा सिलिकन मुख्यतः चतुःसंयोजी होते हैं परन्तु Ge, Sn तथा Pb द्विसंयोजकता प्रदर्शित करते हैं। कारण दीजिए।
उत्तर:
Ge, Sn तथा Pb अक्रिय युग्म प्रभाव के कारण द्विसंयोजी होते हैं जो कि कार्बन तथा सिलिकन में नहीं होता।
प्रश्न 77.
सिलिकॉन का सामान्य सूत्र क्या है ?
उत्तर:
R2SiO.
![]()
प्रश्न 78.
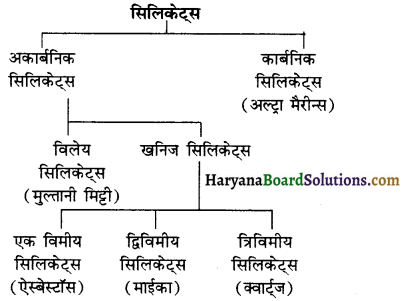
सिलिकेट क्या हैं ?
उत्तर:
सिलिकेट खनिज होते हैं जिनमें \(\mathrm{SiO}_4{ }^{4-}\) इकाइयाँ विभिन्न क्रमों में व्यवस्थित रहती हैं।
प्रश्न 79.
समूह-14 में से उन सदस्य (या सदस्यों) को चुनिए, जो
(i) सबसे अधिक अम्लीय डाइऑक्साइड बनाते हैं;
(ii) सामान्यत: +2 ऑक्सीकरण अवस्था में मिलते हैं;
(iii) अर्द्धचालक (या अर्द्धचालकों) के रूप में प्रयोग में आते हैं।
उत्तर:
(i) कार्बन, (ii) सिलिकन तथा (iii) जर्मेनियम।
प्रश्न 80.
मेथेन किस से प्राप्त की जाती है ?
उत्तर:
एल्युमीनियम कार्बाइड से मेथेन प्राप्त की जाती है।
प्रश्न 81.
\(\left[\mathrm{SFF}_6\right]^{2-}\) ज्ञात है, जबकि \(\left[\left.\mathrm{SiCl}_6\right|^{2-}\right.\) अज्ञात है। इसके सम्भावित कारण दीजिए।
उत्तर:
इसके मुख्य सम्भावित कारण निम्नलिखित हैं-
- सिलिकन परमाणु का आकार छोटा होने के कारण इसके चारों ओर क्लोरीन के छः बड़े आकार वाले परमाणु व्यवस्थित नहीं हो पाते हैं।
- क्लोरीन परमाणु के एकाकी इलेक्ट्रॉन युग्म तथा सिलिकन परमाणु के मध्य अन्योन्यक्रिया अधिक प्रबल नहीं होती है।
प्रश्न 82.
कार्बन डाइऑक्साइड दहन में सहायता नहीं करती है, परन्तु मैग्नीशियम का जलता हुआ तार CO2 के वातावरण में जलता रहता है। क्यों ?
उत्तर:
मैग्नीशियम CO2 को कार्बन में अपचयित कर देता है तथा अभिक्रिया ऊष्माक्षेपी होती है। चूँकि मैग्नीशियम का ज्वलन-ताप बहुत अधिक होता है; अतः यह CO2 के वातावरण में जलता रहता है।
प्रश्न 83.
ग्रेफाइट विद्युत चालक क्यों होता है ?
उत्तर:
ग्रेफाइट में प्रत्येक कार्बन परमाणु sp2 संकरित होता है तथा तीन अन्य कार्बन परमाणुओं से एकल संयोजी बन्धों द्वारा जुड़ा रहता है। प्रत्येक कार्बन परमाणु का एक इलेक्ट्रॉन मुक्त रहता है जिसके कारण ग्रेफाइट विद्युत का सुचालक होता है।
प्रश्न 84.
कार्बन मोनोऑक्साइड रक्त के साथ क्रिया कर कौन-सा यौगिक बनाती है ?
उत्तर:
कार्बोक्सी हीमोग्लोबिन।
प्रश्न 85.
कार्बन मोनोऑक्साइड गैस ‘मौत का फन्दा’ है; समझाइए।
उत्तर:
कार्बन मोनो ऑक्साइड गैस (CO) रक्त के हीमोग्लोबिन से संयुक्त होकर कार्बोक्सी हीमोग्लोबिन बनाती है जिससे हीमोग्लोबिन ऑक्सीवाहक का कार्य करना बन्द कर देता है एवं मनुष्य दम घुटने के कारण मर जाता है। अतः CO गैस ‘मौत का फन्दा’ है।
प्रश्न 86.
कार्बन के अपररूप कौन-कौन से हैं ?
उत्तर:
कार्बन के दो अपररूप हैं-
(i) क्रिस्टलीय कार्बन-यह तीन रूपों में पाया जाता है-
(अ) हीरा, (ब) ग्रेफाइट, (स) फुलरीन।
(ii) अक्रिस्टलीय रूप-यह तीन रूपों में पाया जाता है-
(अ) चारकोल, (ब) काजल, (स) खनिज कोयला।
प्रश्न 87.
कार्बन कौन-से ऑक्साइड बनाता है ?
उत्तर:
- कार्बन सबऑक्साइड (C3O2),
- कार्बन मोनोऑक्साइड (CO),
- कार्बन डाईऑक्साइड (CO2)।
प्रश्न 88.
कार्बन मोनो-ऑक्साइड का औद्योगिक उपयोग बताइए।
उत्तर:
प्रोड्यूसर गैस (CO + N2) तथा भाप अंगार गैस (CO + H2) के रूप में ईंधन में प्रयुक्त होती है।
प्रश्न 89.
CO2 का प्रकृति में क्या उपयोग है ?
उत्तर:
क्लोरोफिल की उपस्थिति में पौधे CO2 को ग्रहण कर सूर्य के प्रकाश में ग्लूकोस, स्टार्च, सेल्यूलोस आदि बनाते हैं।
\(6 \mathrm{CO}_2+6 \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{C}_6 \mathrm{H}_{12} \mathrm{O}_6+6 \mathrm{O}_2\)
प्रश्न 90.
कार्बन के मिश्रित हैलाइडों को समझाइए।
उत्तर:
कार्बन के साथ फ्लोरीन तथा क्लोरीन दो भिन्न तत्वों के जुड़े होने पर प्राप्त यौगिक क्लोरो-फ्लुओरो यौगिक कहलाते हैं। इन्हें मिश्रित हैलाइड कहते हैं। जैसे-फ्रेऑन-11 (CFCl3)$, फ्रेमीन- 12 (CF2Cl2) ये प्रशीतक के रूप में प्रयुक्त होते हैं।
प्रश्न 91.
कार्बन परमाणु का विशिष्ट गुण क्या है ?
उत्तर:
कार्बन परमाणु का विशिष्ट गुण भृंबला बनाने की प्रवृत्ति है।
प्रश्न 92.
कुछ वर्षों पूर्व खोजे गए कार्बन के नए रूप का नाम लिखिए।
उत्तर:
C60 या बकमिन्सटर फुलरीन।
प्रश्न 93.
डायमण्ड में C—C लम्बाई बताइए।
उत्तर:
डायमण्ड में प्रत्येक C—C बंध की दूरी 1.54 Å होती है।
प्रश्न 94.
डायमण्ड में क्राबंन परमाणु पर कौन-सा संकरण होता है ?
उत्तर:
डायमण्ड में प्रत्येक कार्बन परमाणु पर sp3 संकरण होता है।
प्रश्न 95.
गेफाइट में प्रत्येक कावंन परमाणु पर कौन-सा संकरण होता है ?
उत्तर:
ग्रेफाइट में प्रत्येक कावन परमाणु पर sp2 संकरण होता है।
प्रश्न 96.
ऐ्रेफाइट विद्युत का सुचालक क्यों है ?
उत्तर:
ग्रेफाइट में प्रत्येक कार्बन परमाणु पर p-उपकोश में एक इलेक्ट्रॉन शेष रहता है यह π-इलेक्ट्रॉन कहलाता है। इन्ही π-इ्लेक्ट्रॉनों के गतिशील होने के कारण ग्रेफाइट विद्युत का सुचालक है।
प्रश्न 97.
ग्रेफाइट में C—C बंध की दूरी क्या है ?
उत्तर:
प्रत्येक C—C बंध की दूरी 1.42 Å होती है।
![]()
प्रश्न 98.
फुलरीन की खोज कब हुई ?
उत्तर:
1985 में।
प्रश्न 99.
C60 का नाम किसके नाम पर रखा गया ?
उत्तर:
अमरीकी वास्तु स्थापत्य बकमिन्सटर फुलरीन के नाम पर रखा गया।
प्रश्न 100.
C60 में कौन-सा संकरण होता है ?
उत्तर:
C60 में कार्बन परमाणु पर sp2 संकरण होता है।
प्रश्न 101.
प्रकृति में कार्बन किस शुद्ध अवस्था में पाया जाता है ?
उत्तर:
फुलरीन।
प्रश्न 102.
ड्वायमण्ड में कौन-सा संकरण होता है ?
उत्तर:
sp3
प्रश्न 103.
\(\mathrm{SiF}_6{ }^{2-}\) में C संकरण कौन-सा है ?
उत्तर:
sp2 संकरण।
प्रश्न 104.
\(\mathrm{SiF}_6{ }^{2-}\) में Si का संकरण क्या है ?
उत्तर:
sp3d2
प्रश्न 105.
SiCl4 का जल अपघटन हो सकता है परन्तु CCl4 का नहीं; क्यों ?
उत्तर:
Si में रिक्त d-कक्षक पाये जाते हैं जिसके कारण SiCl4 का जल अपघटन हो सकता है, परन्तु CCl4 का नहीं।
प्रश्न 106.
गैसीय ईंधन अत्यधिक उपयोगी क्यों होते हैं ?
उत्तर:
गैसीय ईंधनों का दहन पूर्ण रूप से हो जाता है तथा इसका कोई भी अवशेष नहीं बचता है, इस कारण गैसीय ईंधन अत्यधिक उपयोगी होते हैं।
प्रश्न 107.
सिन्दूर का रासायनिक नाम व सूत्र क्या है?
उत्तर:
ट्राइप्लम्बिक टेट्रॉऑक्साइड (Pb3O4)
प्रश्न 108.
कार्बन के दो क्रिस्टलीय अपररूपों के उदाहरण लिखें।
उत्तर:
डायमण्ड व ग्रेफाइट कार्बन के दो क्रिस्टलीय अपररूप हैं।
प्रश्न 109.
किन्हीं चार ईंधनों के उदाहरण लिखें।
उत्तर:
- भाप-अंगार गैस,
- पेट्रोल गैस,
- तेल गैस,
- प्रोड्यूसर गैस।
प्रश्न 110.
कार्बन परिवार का वह कौन-सा तत्व है जो कि अपररूपता को प्रदर्शिन नहीं करता है ?
उत्तर:
लेड (Pb).
प्रश्न 111.
कार्बन का उदासीन ऑक्साइड कौन-सा है ?
उत्तर:
कार्बन मोनोऑक्साइड (CO).
प्रश्न 112.
प्रयोगशाला में बर्नरों में प्रयोग की जाने वाली गैस कौन-सी है ?
उत्तर:
तेल गैस या पेट्रोल गैस, परन्तु आजकल प्रयोगशाला में L.P.G. प्रयुक्त होती है।
प्रश्न 113.
वाटर ग्लास का सूत्र लिखें।
उत्तर:
Na2SiO3
प्रश्न 114.
ठण्डे देशों में पैकिंग के लिये टिन धातु की पन्नी का प्रयोग क्यों नहीं किया जाता है ?
उत्तर:
कम ताप पर टिन, ग्रे-टिन में परिवर्तित हो जाता है। यह ग्रे टिन भंगुर प्रकृति का होता है तथा पाउडर में बदल जाता है। इसको टिन-प्लेग (tin plague) या टिन की बीमारी (tin disease) भी कहते हैं।
प्रश्न 115.
CH4 व SiH4 के गुणों में भिन्नता क्यों होती है ?
उत्तर:
Si-H की बन्ध ऊर्जा का मान C-H की बन्ध ऊर्जा से कम होता है।
प्रश्न 116.
MgCl2 की आकृति अधुवीय रेखीय है जबकि SnCl2 कोणीय ध्रुवीय होता है। कारण बताओ।
उत्तर:
MgCl2 में Mg पर sp संकरण पाया जाता है जो कि रेखीय आकृति देता है, जबकि SnCl2 में Sn, sp2 संकरण (समतलीय त्रिकोणीय) प्रकृति प्रदर्शित करता है। Sn पर एक अनाबन्धित या एकाकी इलेक्ट्रॉन युग्म इसका आकार कोणीय कर देता है।
प्रश्न 117.
SnCl2ठोस है, जबकि SnCl4 दव है। क्यों ?
उत्तर:
SnCl2 की आयनिक प्रकृति अधिक (Sn2+) होती है अत: इसका गलनांक भी अधिक होता है और इस कारण यह ठोस अवस्था में पाया जाता है। SnCl4 में sp3संकरण होता है, जिसके कारण इसकी प्रवृत्ति सह-संयोजक होती है और यह द्रव अवस्था में होता है।
प्रश्न 118.
अपररूपता को परिभाषित करें।
उत्तर:
जब कोई तत्व दो या दो से अधिक रूपो में पाया जाता है, जिनके भौतिक गुण भिन्न-भिन्न ब रासायनिक गुण समान होते हैं तो इन रूपों को अपररूप व इस गुण को अपररूपता कहते हैं।
प्रश्न 119.
शृंखलित होने का गुण (Catenation) क्या है?
उत्तर:
समान परमाणुओं के आपस में जुड़कर एक लम्बी विवृत भंख्रला अथवा संबृत भृंखला बनाने की प्रवृत्ति को मृंखलित होने का गुण (Catenation) कहते हैं।
प्रश्न 120.
समूह-14 में +2 ऑक्सीकरण अवस्था बनाने की प्रयृत्ति समूह में नीचे जाने पर बक़ी जाती है, क्यों ?
उत्तर:
चूँकि समूह में नीचे जाने पर अक्रिय युग्म प्रभाव (Inert pair effect) बढ़ा जाता है, इसके कारण +2 ऑक्सीकरण अवस्था प्रदर्शित करने की प्रवृत्ति भी बह़ जाती है।
प्रश्न 121.
टिन व लेड क्रमशः Sn2+ तथा Pb2+ आयन बनाते हैं। क्यों ?
उत्तर:
अक्रिय युग्म प्रभाव (inert pair effect) के कारण टिन व लेड क्रमशः Sn2+ तथा Pb2+ आयनों को बनाते हैं।
![]()
प्रश्न 122.
समूह-14 में ऊपर से नीचे जाने पर श्रृंखलित होने का गुण घटता जाता है। क्यों ?
उत्तर:
समूह-14 में ऊपर से नीचे जाने पर भृंखलित होने का गुण घटता जाता है क्यॉकि बन्ध ऊर्जा (Bond energy) का मान कार्बन से लेड की और जाने पर घटता जाता है।
प्रश्न 123.
कार्बन की अधिकतम संयोजकता का मान 4 है जबकि सिलिकन की संयोजकता का मान 6 है, क्यों ?
उत्तर:
सिलिकन के वाद्य कोश में रिक्त d-उपकोश उपस्थित होता है जिसके कारण सिलिकन की संयोजकला का मान 6 हो जाता है।
प्रश्न 124.
कार्बन व सिलिकन दोनों एक ही समूह में होते हुए भी अपने यौगिकों के गुणों में भिन्नता प्रदर्शित करते हैं, क्यों ?
उत्तर:
कार्बन व सिलिकन एक ही समूह में उपस्थित हैं परन्तु इन दोनों तत्वों की विद्युत ऋणात्मकता में काफी अन्तर होता है। इस कारण इनके यौगिकों के गुर्णों में काफी भिन्नता होती है।
प्रश्न 125.
ऐसे CO2 को शुष्क वर्फ क्यों कहा जाता है?
उत्तर:
क्योंकि टेस CO2 के ऊर्ध्वपातन होने से सतह पर किसी भी प्रकार का कोई अवशेष नहीं रहता है, इस को कारण इसे शुष्क बर्फ कहते है।
प्रश्न 126.
रेडियोएक्टिव पदार्थों को लेड के बक्सों में क्यों रखा जाता है ?
उत्तर:
क्योंकि रेडियोएक्टिब पदार्थों से निकलने वाली रेडियोएक्टिव किरणों में लेड धातु को पार करने की क्षमता बहुत कम होती है। इस कारण रेडियोएक्टिव पदायों को लेड वॉक्स में रखते हैं।
प्रश्न 127.
डायमण्ड विद्युत का चालक नहीं होता है, क्यों ?
उत्तर:
डायमण्ड विद्युत का कुचालक है, क्योंकि इसमें प्रत्येक कार्बन परमाणु के चारों संयोजी इलेक्ट्रॉन चार एकल सह-संयोजक बन्ध बनाने में प्रयुक्त हो जाते हैं जिसके कारण डायमण्ड विद्युत् का कुचालक होता है।
प्रश्न 128.
CO2 ऑक्सीजन की उपस्थिति में क्यों नहीं जलती है ?
उत्तर:
CO2 में कार्बन की अधिकतम ऑक्सीकरण अवस्था होती है
अतः CO2 का पुनः ऑक्सीकरण होना सम्भव नहीं होता है। यही कारण है कि CO2 ऑक्सीजन की उपस्थिति में नहीं जलती है।
प्रश्न 129.
कार्बन मोनोऑक्साइड के अम्लीय होने को प्रदर्शित करने वाला एक समीकरण लिखें।
उत्तर:
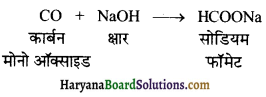
प्रश्न 130.
समूह्न 14 के तत्वों के टेट्राहैलाइडों के स्थायित्व का घटता हुआ क्रम लिखें।
उत्तर:
CX4 > SiX4 > GeX4 > SnX4 > PbX4
प्रश्न 131.
निम्न अभिक्रियाओं को पूर्ण करें-
(i) Pb + 4HNO3→
(ii) SiCl4 + 4H2O→
उत्तर:
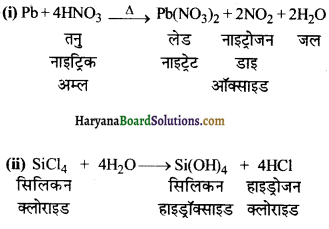
प्रश्न 132.
समूह-14 में सबसे अधिक अम्लीय डाइऑक्साइड कौन बनाता है ?
उत्तर:
कार्बन सबसे अधिक अम्लीय डाइऑक्साइड बनाता है।
प्रश्न 133.
समूह-14 में वह कौन-सा तत्व है जो कि सामान्यता +2 ऑक्सीकरण अवस्था में प्राप्त होता है ?
उत्तर:
समूह-14 में लैड (Pb) सामान्यतः + 2 ऑक्सीकरण अवस्था में पांया जाता है।
प्रश्न 134.
समूह-14 में कौन से तत्व अर्द्ध-चालकों के रूप में प्रयुक्त होते हैं ?
उत्तर:
समूह- 14 में सिलिकन तथा जर्मेनियम अर्द्ध-चालकों के रूप में प्रयुक्त होते हैं।
प्रश्न 135.
क्या कारण है कि हीरे में सहसंयोजन होने के उपरान्त भी गलनांक काफी उच्च होता है ?
उत्तर:
हीरे के अणु में C-C परमाणु के मध्य त्रिविम संरचना होती है। इस चतुष्फलक जालक को तोड़ना काफी कठिन होता है। अत: हीरे का गलनांक काफी उच्च होता है। यद्यपि इसमें सहसंयोजक बन्ध पाया जाता है।
प्रश्न 136.
सिलिकॉन्स की प्रकृति कैसी होती है ?
उत्तर:
सिलिकॉन्स जलरोधी एवं जल-अपकर्षक प्रकृति के होते हैं।
प्रश्न 137.
पृथ्वी अथवा मृदा की ऊपरी परत किस रासायनिक पदार्थ से बनी होती है ?
उत्तर:
पृथ्वी अथवा मृदा की ऊपरी परत सिलिकेट्स की बनी होती है।
प्रश्न 138.
अन्नराकाशी काब्बांइक के उदाइरण दें। क्यादरण है।
उत्तर:
Cr3C2, Fe3C, Mn3C, WC आदि अन्तराकाशी कार्बाइड के उदाहरण हैं।
प्रश्न 139.
सहुसंयोजक कार्बाइड के उदलण दें।
उत्तर:
B4C3 तथा SiC सहसंवोनक काबादह के ददाहय है।
प्रश्न 140.
आयनिक कार्बाइड के उदाइरण बें।
उत्तर:
Li2C3, CaC2 तथा Al4C3 अदि अरणनिक्ष का बाइड के उदाइरण है।
प्रश्न 141.
सिलिकन कार्बांइड (SiC) का मुख्य उप्पयोग क्या है ?
उत्तर:
सितिकन कबोद्ड का मुख्य उन्योग काँच को काटने में तथा अम्स-भार को सुरक्षित रखने के लिए किया जाता है।
प्रश्न 142.
बोरॉन कार्जाइड का उबयोग दें।
उत्तर:
बौरौन कार्बांश्ड को प्रकृजी कठोर सेने के दारण बह Drilling में तथा उन्तु बनामे में प्रयुक किवा जाता है।
![]()
प्रश्न 143.
पढ्रो सिलिकेट में कौन-सा क्रणायन मिलनता है ?
उत्तर:
\(\mathrm{Si}_2 \mathrm{O}_7^{6-}\)
प्रश्न 144.
कार्बों रण्डम (carborandum) किसे कहते है?
उत्तर:
SiC (सिलिकन कार्बाइड) को कार्बोरण्डम कहते हैं।
प्रश्न 145.
क्या होता है जब CO को ZnO के साघ गार्म करते हैं ?
उत्तर:
CO एक प्रबत अपवायक है। यह ZnO को लिक (Zn) में अपवावित कर देत्ता है।
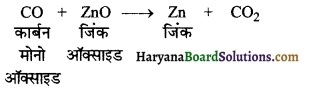
प्रश्न 146.
त्रिबिम मिलिकेट के उद्वाहरण दें।
उत्तर:
क्वारंब तथा रिश्रोलाएट शिविम सिलिकेट के उदाशरण है।
प्रश्न 147.
शिद सिलिकेट के उदाहरण दें। ज्वाहरण है।
उत्तर:
टैल्क, केओलीन तथा मस्क्कोलाइट आदि शिट सिलिकेट के उदाहरण हैं।
प्रश्न 148.
चक्रीय सिलिकेट के उदाहरण दें।
उत्तर:
बेनीटोआइट तथा बोरेल चक्रीय सिलिकेट के उदाहरण हैं।
प्रश्न 149.
श्रृंखला सिलिकेट के उदाहरण दें।
उत्तर:
स्पॉड्यूमीन तथा एन्स्टेटाइट शृंखला सिलिकेट के उदाहरण हैं।
प्रश्न 150.
पायरो सिलिके के उदाइरण दें।
उत्तर:
थौट्टीवीटाइट तथा हेगीमोरफाइर पाबरो सिलिकेट के उदाहरण है।
प्रश्न 151.
औधॉंतिलिकेट के उदाहरण वें ।
उत्नर:
फिनेसदट तथा जिरकॉन और्था सिलिकेट के द्वासण है।
प्रश्न 152.
सिलिका में Si ऑक्सीजन के साथ π-बन्ध क्यों नहीं बना पाता ?
उत्तर:
Si का आकार ऑक्सीजन से बड़ा होता है जिसके कारण यह ऑक्सीजन के साथ π-बन्ध नहीं बना पाता है।
प्रश्न 153.
ऊष्मा भट्टियों में किन इंटों का प्रयोग किया जाता है ?
उत्तर:
ऊष्मा भद्टियों में सिलिका हटं का प्रयोग करते हैं।
प्रश्न 154.
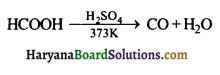
क्या होता है जब HCOOH को सान्द्र H2SO4 के साथ 373 K पर गर्म करते हैं ?
उत्तर:”
HCOOH को सान्द्र H2SO4 के साथ 373 K पर गर्म करने पर CO प्राप्त होती है।
प्रश्न 155.
CO की क्रिया निम्न के साथ प्रदर्शित करें –
(i) ZnO
(ii) Fe2O3
(iii) Ni
(iv) Cl2
उत्तर:
(i) CO की क्रिया ZnO के साथ कराने पर Zn प्राप्त होती है।
\(\mathrm{CO}+\mathrm{ZnO} \longrightarrow \mathrm{Zn}+\mathrm{CO}_2\)
(ii) CO की क्रिया Fe2O3 से कराने पर आयरन व कार्बन डाईंक्साइड बनता है।

(iii) CO की क्रिया Ni से कराने पर कार्बोनिल प्राप्त होता है।

(iv) CO की क्रिया Cl2 से कराने पर एक विर्घली गैस फॉस्जीन प्राप्त होती है।
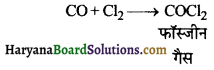
प्रश्न 156.
प्रकाश संश्लेषण पर टिप्पणी लिखें ।
उत्तर:
प्रकाश एवं क्लोरोफिल (पर्णरहित) की उपस्थिति में पौधे कार्बन डाइऑक्साइड गैस ग्रहण करते हैं तथा ऑक्सीजन निकालते हैं। इस अभिक्रिया को प्रकाश संश्लेषण कहते हैं।
\(6 \mathrm{CO}_2+6 \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{C}_6 \mathrm{H}_{12} \mathrm{O}_6+6 \mathrm{O}_2\)
प्रश्न 157.
रात्रि में बड़े वृक्षों के नीचे नहीं सोना चाहिए। क्यों ?
उत्तर:
रात्रि में पेड्ट व पौधे प्रकाश संश्लेषण की क्रिया नहीं करने रात्रि में ये श्वसन की क्रिया करते हैं, जिससे CO2 गैस निकलती है। अतः रात्रि में वृक्ष्र के नीचे नहीं सोना चाहिए।
प्रश्न 158.
C60 की क्रिया पोटैशियम से कराने पर क्या प्राप्त होता है ?
उत्तर:
C60 की क्रिया पोटैशियम के साथ कराने पर K3C60 प्राप्त होता है।
प्रश्न 159.
कार्बन की परमाणवीय त्रिज्या का मान क्या होता है ?
उत्तर:
कार्बन की परमाण्वीय त्रिज्या 77 Å होती है।
प्रश्न 160.
वर्ग-14 के तत्व बताएँ।
उत्तर:
C, Si, Ge, Sn, Pb.
प्रश्न 161.
निम्न के सूत्र लिखें-
(i) केसिटेराइट,
(ii) गैलेना।
उत्तर:
(i) केसिटेराइट- SnO2
(ii) गैलेना-PbS.
प्रश्न 162.
वर्ग-14 के तत्वों को क्वथनांक के बढ़ते क्रम में व्यवस्थित करें।
उत्तर:
Pb < Sn < Ge < Si < C
प्रश्न 163.
स्थायी रूप से अतिशीतित (super cooled) द्रव क्या कहलाता है ?
उत्तर:
स्थायी रूप से अतिशीतित (super cooled) द्रव को अक्रिस्टलीय ठोस (amorphous solid) कहते हैं।
प्रश्न 164.
क्या होता है जब लेड सल्फाइड को वायु में गर्म किया जाता है ?
उत्तर:

प्रश्न 165.
हानिकारक U.V. rays को सोखने वाले काँच का नाम बताओ।
उत्तर:
क्रुक्स काँच (Crookes glass)।
प्रश्न 166.
सफेदा का सूत्र लिखें।
उत्तर:
2PbCO3.Pb(OH)2
प्रश्न 167.
CO2 एक अम्लीय एनहाइड्राइड है जबकि PbO2 एक क्षारीय एनहाइड्राइड है। स्पष्ट करें।
उत्तर:
C एक अधातु है, अतः इसका ऑक्साइड (CO2) अम्लीय है जबकि Pb एक धातु है अतः इसका ऑक्साइड (PbO2) क्षारीय है।
लघु उत्तरीय प्रश्न:
प्रश्न 1.
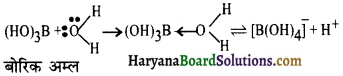
बोरिक अम्ल, B(OH)3 में तीन OH समूह होते हैं परन्तु फिर भी यह दुर्बल क्षारकीय अम्ल होता है। समझाइए।
उत्तर:
बोरिक अम्ल में बोरॉन परमाणु इलेक्ट्रॉन न्यून होता है तथा H2O अणु के परमाणु से इलेक्ट्रॉन युग्म ग्रहण कर लेता है। इसके परिणामस्वरूप एक उपसहसंयोजक बन्ध बनता है। अतः यह जलयोजित हो जाता है। जलयोजित अणु में ऑक्सीजन परमाणु जो इलेक्ट्रॉन अपूर्ण हो चुका है, OH बन्ध से इलेक्ट्रॉन युग्म को खींचता है जिससे प्रोटॉन निकल जाता है। अतः यह अम्ल एक क्षारकीय अम्ल (monobasic acid) की भाँति कार्य करता है।
प्रश्न 2.
BX3 में B-X बन्ध लम्बाई अपेक्षा से कम मानी जाती है, क्यों ?
उत्तर:
pπ-pπ पश्च बन्धन के कारण BX3 में B-X बन्ध आंशिक द्विबन्ध गुण धारण कर लेता है। इसके परिणामस्वरूप B-X बन्ध लम्बाई, अपेक्षित एकल संयोजक B-X बन्ध लम्बाई से कम हो जाती है।
प्रश्न 3.
सुहागा-मनका परीक्षण क्या है ? समीकरण सहित समझाइए।
उत्तर:
सुहागा-मनका परीक्षण (Borax-Bead Test)
यह परीक्षण उन बेसिक मूलकों के परीक्षण में काम आता है जिनके लवण रंगीन होते हैं या जो सुहागा के साथ गर्म किए जाने पर रंगीन पदार्थ बनाते हैं। सबसे पहले प्लैटिनम के तार के छल्ले (ring) पर बोरेक्स का चूर्ण लेकर ज्वाला में खूब गर्म किया जाता है। शुरू में यह फूलता है तथा बाद में काँच के समान गोली बन जाती है।
\(\mathrm{Na}_2 \mathrm{~B}_4 \mathrm{O}_7 \cdot 10 \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{Na}_2 \mathrm{~B}_4 \mathrm{O}_7+10 \mathrm{H}_2 \mathrm{O}\) सोडियम टेट्राबोरेट
\(\mathrm{Na}_2 \mathrm{~B}_4 \mathrm{O}_7 \longrightarrow 2 \mathrm{NaBO}_2+\mathrm{B}_2 \mathrm{O}_3\) काँच के समान गोली
अब मनके पर थोड़ा-सा दिया हुआ पदार्थ रखकर ज्वाला पर रखते हैं। इस काँच के समान गोली का एक विशिष्ट रंग आता है जिसके आधार पर इसके मूलकों का ज्ञान होता है; जैसे-कॉपर के साथ एक नीला मनका बनता है।
\(\mathrm{CuSO}_4 \longrightarrow \mathrm{CuO}+\mathrm{SO}_4 \uparrow\)
\(\mathrm{CuO}+\mathrm{B}_2 \mathrm{O}_3 \longrightarrow \mathrm{Cu}\left(\mathrm{BO}_2\right)_2\)
\(\mathrm{CuSO}_4+\mathrm{B}_2 \mathrm{O}_3 \longrightarrow \mathrm{Cu}\left(\mathrm{BO}_2\right)_2+\mathrm{SO}_3 \uparrow\)
कॉपर मेटाबोरेट (नीला रंग)
इसी प्रकार कुछ अन्य बेसिक मूलकों में उत्पन्न रंगों को नीचे दिया गया है-
Co2+ (गहरा नीला), Ni2+ (भूरा), Mn2+ (बैंगनी), Cr3+ ( हरा) तथा Fe3+ (पीला)। इस प्रकार केवल मनके का रंग देखकर ही मिश्रण में विद्यमान कुछ बेसिक मूलकों का पता लगाया जा सकता है।
![]()
प्रश्न 4.
बोरिक अम्ल से प्रारम्भ करके निम्नलिखित यौगिकों को कैसे प्राप्त करोगे ?
(i) बोरॉन ऐनहाइड्राइड
(ii) बोरॉन ट्राइक्लोराइड
(iii) बोरॉन हाइड्राइड
(iv) बोरॉन ट्राइफ्लुओराइड।
उत्तर:
(i) बोरिक अम्ल से बोरॉन ऐनहाइड्राइड में परिवर्तनबोरिक अम्ल को रक्त तप्त करने पर बोरॉन ऐनहाइड्राइड प्राप्त होता है।

(ii) बोरिक अम्ल से बोरॉन ट्राइक्लोराइड में परिवर्तन-उपर्युक्त विधि से सबसे पहले बोरॉन ऐनहाइड्राइड को प्राप्त कर लिया जाता है। बोरॉन ऐनहाइड्राइड को कार्बन के साथ मिलाकर रक्त तप्त करके, क्लोरीन गैस प्रवाहित की जाती है तो बोरॉन ट्राइक्लोराइड प्राप्त हो जाता है।

(iii) बोरिक अम्ल से बोरॉन ऐनहाइड्राइड में परिवर्तन-उपर्युक्त विधि से प्राप्त बोरॉन ऐनहाइड्राइड को मैग्नीशियम चूर्ण के साथ गर्म करके मैग्नीशियम बोराइड प्राप्त कर लिया जाता है। मैग्नीशियम बोराइड तनु HCl से प्रक्रिया करके वाष्पशील हाइड्राइडों का मिश्रण देता है।
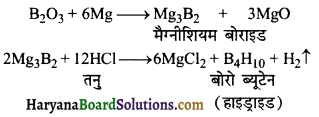
(iv) बोरिक अम्ल से बोरॉन ट्राइफ्लुओराइड में परिवर्तन-जब बोरिक अम्ल को सान्द्र H2SO4 और CaF2 के साथ गर्म किया जाता है तो बोरॉन ट्राइफ्लओओराइड की वाष्प प्राप्त हो जाती है।

प्रश्न 5.
बोरेक्स से बोरॉन प्राप्त करने की विधि को समझाइए। उत्तर-बोरेक्स को सान्द्र HCl के साथ अभिक्रिया कराने पर बोरिक अम्ल प्राप्त होता है जो तेज गर्म करने पर बोरिक एनहाइड्राइड देता है।
\(\mathrm{Na}_2 \mathrm{~B}_4 \mathrm{O}_7+2 \mathrm{HCl} \longrightarrow 2 \mathrm{NaCl}+\mathrm{H}_2 \mathrm{~B}_4 \mathrm{O}_7\)
\(\mathrm{H}_2 \mathrm{~B}_4 \mathrm{O}_7+5 \mathrm{H}_2 \mathrm{O} \longrightarrow 4 \mathrm{H}_3 \mathrm{BO}_3\) बोरिक अम्ल
\(4 \mathrm{H}_3 \mathrm{BO}_3 \longrightarrow \mathrm{B}_2 \mathrm{O}_3+3 \mathrm{H}_2 \mathrm{O}\)
बोरिक एनहाइड्राइड को पोटैशियम के साथ गर्म करने पर बोरॉन प्राप्त होता है।
\(\mathrm{B}_2 \mathrm{O}_3+6 \mathrm{~K} \longrightarrow 2 \mathrm{~B}+3 \mathrm{~K}_2 \mathrm{O}\)
प्रश्न 6.
बोरिक अम्ल कैसे बनाया जाता है ? इसका एक रासायनिक गुण तथा प्रमुख उपयोग लिखिए।
उत्तर:
बनाने की विधि-कोलेमेनाइट को उबलते हुए जल में डालकर SO2 गैस प्रवाहित करने पर बोरिक अम्ल प्राप्त होता है।
\(\mathrm{Ca}_2 \mathrm{~B}_6 \mathrm{O}_{11}+2 \mathrm{SO}_2+9 \mathrm{H}_2 \mathrm{O} \longrightarrow 6 \mathrm{H}_3 \mathrm{BO}_3+6 \mathrm{CaSO}_3\)
गर्म करने पर बोरिक अम्ल अपघटित होकर बोरिक एनहाइड्राइड देता है।

बोरिक अम्ल का उपयोग इनैमल और पोटरी को चमकयुक्त बनाने में किया जाता है।
प्रश्न 7.
BCl3 एकलक के रूप में पाया जाता है जबकि BH3 द्विलक अर्थात् B2H6 बनाता है। क्यों ?
उत्तर:
BCl3 में पश्च आबन्ध (Back bonding) पायी जाती है अर्थात् एकाकी इलेक्ट्रॉन युग्म Cl के द्वारा B को दिया जाता है। जिस कारण बोरॉन की इलेक्ट्रॉन न्यूनता कम हो जाती है। जबकि BH3 में पश्च आबन्ध (Back bonding) नहीं पायी जाती है लेकिन यहाँ दो सेतुबन्ध (B-H-B) पाये जाते हैं। इसलिए यह द्विलक के रूप में पाया जाता है।
प्रश्न 8.
निम्नलिखित को रासायनिक समीकरणों द्वारा सिद्ध करें-
(i) Sn (II) एक अपचायक है जबकि pb (II) नहीं। क्यों ?
(ii) Ga (I) असमानुपातन अभिक्रियायें प्रदर्शित करता है, क्यों ?
उत्तर:
(i) Sn (II) एक अपचायक है जबकि Pb (II) नहीं क्योंकि Pb2+, Pb4+ से ज्यादा स्थायी होता है। ऐसा अक्रिय युग्म प्रभाव के कारण होता है तथा Sn4+, Sn2+ से ज्यादा स्थायी होता है अत: Sn2+ एक अपचायक का कार्य करता है।
\(\mathrm{Sn}^{2+}+\mathrm{Pb}^{4+} \longrightarrow \mathrm{Sn}^{4+}+\mathrm{Pb}^{2+}\)
या \(\mathrm{SnCl}_2+\mathrm{PbCl}_4 \longrightarrow \mathrm{SnCl}_4+\mathrm{PbCl}_2\)
(ii) क्योंकि Ga+1 से ज्यादा स्थायी Ga3+ होता है।
\(3 \mathrm{Ga}^{+} \longrightarrow 2 \mathrm{Ga}+\mathrm{Ga}^{3+}\)
प्रश्न 9.
निम्न को +3 ऑक्सीकरण अवस्था के स्थायित्व के आधार पर बढ़ते क्रम में व्यवस्थित करें ?
BCl3, AlCl3, GaCl3, InCl3, TICl3
उत्तर:
TlCl3 < InCl3 < GaCl3 < AlCl3 < BCl3 ( अक्रिय युग्म प्रभाव के कारण यह क्रम पाया जाता है।)
प्रश्न 10.
निम्न को पूर्ण करें।
(i) NaBH4 + I2→
उत्तर:
2NaBH4 + I2→ 2Nal + B2H6 + H2 डाइ-बोरॉन
(ii) B2H6 + NaH→
उत्तर:
B2H6 + 2NaH→ 2Na BH4 सोडियम बोरो-हाइड्राइड
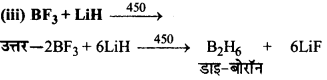
(iv) B2H6 + H2O→
उत्तर:
B2H6 + 6H2O→ 2B(OH)3 + 6H2 बोरिक अम्ल
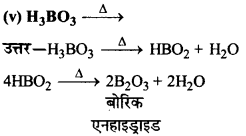
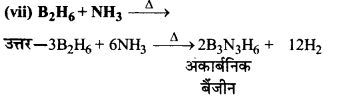
(vi) Al + NaOH→
उत्तर:
Al + 3NaOH →Al(OH)3 + 3Na एल्युमीनियम हाइड्रॉक्साइड
प्रश्न 11.
BF3 की जल से अभिक्रिया का समीकरण लिखिए।
उत्तर:

प्रश्न 12.
B2H6 की HCl से अभिक्रिया लिखें ।
उत्तर:
B2H6 + HCl → B2H5Cl + H2 क्लोरो डाइ-बोरॉन
प्रश्न 13.
कोबाल्ट (II) ऑक्साइड के बोरेक्स बीड परीक्षण की रासायनिक अभिक्रियाएँ लिखिए।
उत्तर:
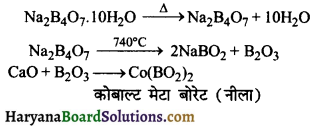
प्रश्न 14.
क्या होगा जब एल्यूमिनियम नाइट्राइड गर्म जल से क्रिया करता है।
उत्तर:
अमोनिया गैस प्राप्त होती है।
\(\mathrm{AlN}+3 \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{Al}(\mathrm{OH})_3+\mathrm{NH}_3\) वाष्प अमोनिया
प्रश्न 15.
कार्बन के गुणों को समझाइए।
उत्तर:
(1) कार्बन की परमाणु त्रिज्या 0.77 Å है।
(2) कार्बन की विद्युत-ऋणात्मकता 2.5 है।
(3) कार्बन अधातु तत्व है। इसकी प्रथम आयनन ऊर्जा 1086 किलो जूल प्रति मोल है।
(4) कार्बन का गलनांक 3727°C (4000 K) है। इसका क्वथनांक 5100 K है।
(5) कार्बन परमाणुओं में शृंखलित होने का गुण बहुत अधिक है, अतः ये परस्पर जुड़कर एकल (Single), द्विक् (Double) तथा त्रिक (Triple) बंध बना लेते हैं। कार्बन, नाइट्रोजन, सल्फर व ऑक्सीजन के साथ एक से अधिक बंध बनाता है।
![]()
प्रश्न 16.
कार्बाइड किसे कहते हैं ? कार्बाइड कितने प्रकार के होते हैं ? उदाहरण सहित समझाइए। कार्बाइड के प्रमुख उपयोग लिखिए।
उत्तर:
कार्बाइड-कार्बन अपने से कम विद्युत-ऋणता वाले तत्वों से अभिक्रिया करके द्विअंगी यौगिक बनाता है। ये यौगिक कार्बाइड कहलाते हैं। जैसे-केल्सियम कार्बाइड (CaC2), सिलिकन-कार्बाइड (SiC), लीधियम कार्बाइड (Li2C2), एल्युमिनियम कार्बाइड (Al4C3) ।
कार्बाइडों के प्रकार-कार्बाइड चार प्रकार के होते हैं-
(i) आयनिक कार्बाइड-प्रथम, द्वितीय तथा तेरहवें वर्ग में (बोरॉन को छोड़कर) अन्य तत्वों के साथ कार्बन संयुक्त होकर आयनिक कार्बाइड बनाता है। उदाहरणार्थ- Li2C2, CaC2, Al4C3 आदि।
(ii) सहसंयोजी कार्बाइड-सिलिकन-कार्बाइड (SiC) तथा बोरॉन कार्बाइड (B4C3) सहसंयोजी कार्बाइड हैं। जैसे-टंगस्टन कार्बाइड (WC तथा W2C) ।
(iii) धात्विक कार्बाइड-चतुर्थ, पंचम, षष्ठम वर्ग की धातुओं के कार्बाइड धात्विक कार्बाइड कहलाते हैं। इनमें सहसंयोजी बंध होता है।
(iv) अन्तराली कार्बाइड- Fe3C, Cr3C, Mn3C आदि कार्बाइड अन्तराली कार्बाइड कहलाते हैं। इन धातुओं के जालकों में रिक्त स्थानों में कार्बन प्रवेश कर लेता है। इसीलिए ये अन्तराली कार्बाइड कहलाते है।
कार्बाइडों के उपयोग-
- कैल्सियम कार्बाइड का उपयोग ऐसीटिलीन बनाने के लिए होता है।
- सिलिकन कार्बाइड को कोरण्डम कहते हैं। इसकी कठोरता के कारण इसका उपयोग पीसने के पत्थर तथा धातुओं में धार बनाने के लिए होता है।
- बोरॉन कार्बाइड का उपयोग हीरे को काटने, तरासने, रॉकेट में छेद बनाने, इलेक्ट्रॉन बनाने तथा लैम्प फिलामेण्ट बनाने में होता है।
- ऐल्युमिनियम कार्बाइड से मेथेन प्राप्त की जाती है।
![]()
प्रश्न 17.
CO2 तथा SiO2 की संरचना में अन्तर बताइये।
उत्तर:
| CO2 | SiO2 |
| 1. यह एक रेखीय यौगिक है तथा एकलक के रूप में पाया जाता है। यह एक गैस है। | 1 . SiO2 कक्ष ताप पर ठोस अवस्था में पाया जाता है क्योंकि इसकी संरचना त्रिविमीय होती है जिसमें Si परमापु चार ऑक्सीजन परमाणु के साथ चतुष्फलकीय सह-संयोजक बंध बनाते हैं। |
| 2. CO2 में कार्बन sp संकरण प्रदर्शित करता है। | 2. SiO2 में Si का संकरण sp3 होता है। |
प्रश्न 18.
निम्न में से कौन अम्लीय ऑक्साइड है और क्यों ?
SiO2, Al2O3, PbO2, SnO2
उत्तर:
SiO2 अम्लीय ऑक्साइड है क्योंकि Si एक अधातु है।
प्रश्न 19.
निम्न को उनके क्वथनांकों के बढ़ते क्रम में व्यवस्थित करें-
उत्तर:
CH4 < SiH4 < GeH4 < SnH4 समूह में नीचे जाने पर पृष्ठीय क्षेत्रफल (Surface area) बढ़ने के कारण वाण्डरवाल बल का आकर्षण बल बढ़ जाता है जिसके कारण क्वथनांक भी बढ़ जाता है।
प्रश्न 20.
कार्बन एलुमीनियम ऑक्साइड का अपचयन नहीं कर सकता, क्यों ?
उत्तर:
क्योंकि Al एक प्रबल अपचायक है। इसकी अपचायक प्रकृति कार्बन से अधिक होती है।
प्रश्न 21.
निम्न के लिए रासायनिक समीकरण लिखें-
(अ) CO2 बनाने की विधि।
(ब) Na2CO3 का क्षारीय गुण।
(स) एसीटिलीन बनाने की विधि।
उत्तर:
(अ) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
(ब) Na2CO3 + 2H2O → 2 NaOH + H2CO3
(स) CaC2 + 2H2O → Ca(OH)2 + C2H2
प्रश्न 22.
क्या होता है जब-
(अ) CaO की क्रिया कोक के साथ करायी जाती है।
(ब) CO की क्रिया Cl2 के साथ होती है।
(स) पौधे CO2 का अवशोषण करते हैं।
उत्तर:
(अ) CaO + 3C → CaC2 + CO कैल्सियम कार्बाइड
(ब) CO + Cl2 → COCl2 (फॉस्जीन)
(स) 6CO2 + 6H2O→C6H12O6 + 6O2 ग्लकोज
प्रश्न 23.
सिलिकॉन कार्बाइड कैसे प्राप्त किया जाता है। इसके गुण समझाइये।
उत्तर:
सिलिकान कार्बाइड, SiC-सिलिकॉन कार्बाइड को सिलिका का कार्बन के द्वारा 2273 K पर विद्युत भट्टी में अपचयन करने पर प्राप्त किया जा सकता है।
![]()
गर्म सिलिकॉन पर C2H2 की क्रिया द्वारा भी इसे प्राप्त किया जा सकता है।
\(2 \mathrm{Si}+\mathrm{C}_2 \mathrm{H}_2 \longrightarrow 2 \mathrm{SiC}+\mathrm{H}_2 \uparrow\)
SiC के गुण-
(i) शुद्ध अवस्था में SiC रंगहीन होता है परन्तु व्यावसायिक रूप से काम में आने वाले SiC में अशुद्धियों के कारण पीला, हरा या नीला रंग आ जाता है।
(ii) यह लगभग हीरे जितना कठोर होता है। 2473 K तक इसका विघटन नहीं होता।
(iii) सामान्य अवस्था में प्रबल अम्लों एवं क्षारों से भी यह क्रिया नहीं करता। गलित NaOH के साथ ऑक्सीजन की उपस्थिति में इसका विघटन होता है।
\(\mathrm{SiC}+4 \mathrm{NaOH}+2 \mathrm{O}_2 \longrightarrow \mathrm{Na}_2 \mathrm{CO}_3+\mathrm{Na}_2 \mathrm{SiO}_3+2 \mathrm{H}_2 \mathrm{O}\)
प्रश्न 24.
सिलिकेटों पर टिप्पणी लिखें।
उत्तर:
ऐसे यौगिक जो कि सिलिकॉन व ऑक्सीजन के मध्य बन्ध बनने के कारण बनते हैं तथा जिसमें \(\mathrm{SiO}_4^{4-}\) संरचनात्मक इकाई होती है। सिलिकेट (silicates) कहलाते हैं। भू-पर्पटी का एक बहुत बड़ा भाग सिलिकेट खनिजों का बना होता है उदाहरण-क्वार्ट्ज, ऐस्बेस्टॉस, फेल्सपार, जिओलाइट आदि।