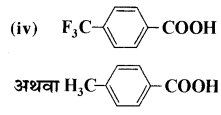
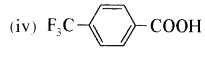
Haryana State Board HBSE 11th Class Biology Important Questions Chapter 11 पौधों में परिवहन Important Questions and Answers.
Haryana Board 11th Class Biology Important Questions Chapter 11 पौधों में परिवहन
(A) वस्तुनिष्ठ प्रश्न
1. जल की परासरणी गति के कारण पादप कोशिका भित्ति पर उत्पन्न दाब कहलाता है –
(A) परासरणी दाब
(B) भित्ति दाब
(C) स्फीति दाब
(D) परासरण विभव
उत्तर:
(C) स्फीति दाब
2. जब कोशिका पूर्णतया आशून हो तब निम्न में से कौन शून्य होगा ?
(A) आशून दाब
(B) भित्ति दाब
(C) चूषण दाब
(D) परासरण दाब
उत्तर:
(C) चूषण दाब
3. जल अवशोषण की क्रिया सबसे अधिक होती है-
(A) मूलरोमों द्वारा
(B) पत्तियों द्वारा
(C) परिपक्व जड़ द्वारा
(D) मूल गोप द्वारा
उत्तर:
(A) मूलरोमों द्वारा
4. पौधे मृदा से किस प्रकार के जल को अवशोषित करते हैं ?
(A) गुरुत्वीय जल
(B) रसायनिकबद्ध जल
(C) केशिकीय जल
(D) इनमें से कोई नहीं
उत्तर:
(C) केशिकीय जल

5. डिक्सन तथा जॉली का रसारोहण सिद्धान्त आधारित है-
(A) जल का संसंजन बल
(B) जल स्तम्भ की निरन्तरता
(C) वाष्पोत्सर्जन अपकर्ष
(D) ये सभी
उत्तर:
(A) जल का संसंजन बल
6. पोटोमीटर का प्रयोग मापने में किया जाता है-
(A) श्वसन
(B) हवा का वेग
(C) प्रकाश संश्लेषण
(D) वाष्पोत्सर्जन
उत्तर:
(D) वाष्पोत्सर्जन
7. शुद्ध जल का विभव तथा परासरण विभव होता है –
(A) 0 तथा 0
(C) 100 तथा 100
(B) 100 तथा 0
(D) 0 तथा 100
उत्तर:
(A) 0 तथा 0
8. जिस विलयन में कोशिका स्फीति होती है, वह है –
(A) अल्पपरासारी
(B) समपरासारी
(C) अतिपरासारी
(D) इनमें से कोई नहीं
उत्तर:
(A) अल्पपरासारी
9. रसारोहण का सिद्धान्त दिया था –
(A) मैक क्लंग ने
(B) जे. सी. बोस ने
(C) फ्लेमिंग ने
(D) लीडर वर्ग ने
उत्तर:
(B) जे. सी. बोस ने
10. वातरन्त्रों का कार्य है –
(A) बिन्दु स्राव
(B) वाष्पोत्सर्जन
(C) रक्त स्राव
(D) गैसों का विनिमय
उत्तर:
(D) गैसों का विनिमय

11. एक विलयन का जल विभव निरूपित किया जाता है –
(A) 4’r से
(B) 4°W से
(C) से
(D) App से
उत्तर:
(B) 4°W से
12. K+ आयन परिकल्पना किसने प्रस्तुत की ?
(A) जे. सी. बोस ने
(B) ए. फ्लेमिंग ने
(C) लैविट ने
(D) मुंच ने
उत्तर:
(C) लैविट ने
13. मूलदाय सिद्धान्त प्रस्तुत किया-
(A) मुंच ने
(B) डिक्सन तथा जॉली ने
(C) लैविट ने
(D) प्रीस्टले ने
उत्तर:
(D) प्रीस्टले ने
14. किसका जल विभव उच्चतम होगा ?
(A) 2% ग्लूकोज
(B) शुद्ध जल
(C) 10% ग्लूकोज
(D) 10% NaCl
उत्तर:
(B) शुद्ध जल
15. जल प्रवेश होने से कोशाओं के फूलने का कारण है-
(A) DPD
(B) स्फीति दाब
(C) अन्तःशोषण
(D) OP
उत्तर:
(B) स्फीति दाब
16. वह प्रक्रिया जिसके द्वारा जल पादप कोशिकाओं में प्रवेश करता है-
(A) विसरण
(B) परासरण
(C) अन्तःचूषण
(D) परासरण और अन्तःचूषण
उत्तर:
(C) अन्तःचूषण

17. वेलामेन एवं स्पंजी ऊतक पाये जाते हैं-
(A) श्वसनमूल में
(B) परजीवी मूल में
(C) कन्दमूल में
(D) उपरिरोही मूल में
उत्तर:
(D) उपरिरोही मूल में
18. जब कोई जीवद्रव्य कुंचित कोशिका अल्प परासारी विलयन में रखी जाती है तो निम्न में से किस बल के कारण जल कोशिका के अन्दर प्रवेश
करता है-
(A) DPD
(B) OP
(C) WP
(D) इनमें से कोई नहीं
उत्तर:
(B) OP
19. परासरण में गति होती है-
(A) केवल विलेय की
(B) केवल विलायक की
(C) दोनों (अ) तथा (ब)
(D) न विलेय न विलायक की
उत्तर:
(B) केवल विलायक की
20. स्टोमेटा कह सकते हैं-
(A) स्टोमेट्स को
(B) लेन्टिसेल को
(C) हाइडेथोड को
(D) वार्म को
उत्तर:
(A) स्टोमेट्स को
21. भूमि में पौधों के लिए आवश्यक जल होता है-
(A) केशिका जल
(B) रासायनिक बन्धित जल
(C) गुरुत्वीय जल
(D) आर्द्रताग्राही जल
उत्तर:
(A) केशिका जल

22. निम्नलिखित में से कोशिका विभाजन का क्षेत्र है-
(A) मूलगोप
(B) विभज्योतक क्षेत्र
(C) मूलरोम प्रदेश
(D) इनमें से कोई नहीं
उत्तर:
(B) विभज्योतक क्षेत्र
23. निम्न में से कौन-सा पदार्थ वाष्पोत्सर्जन की दर को कम करता है-
(A) फिनाइल मरक्यूरिक एसीटेट
(B) ऐब्सीसिक अम्ल
(C) (A) तथा (B)
(D) इनमें से कोई नहीं
उत्तर:
(C) (A) तथा (B)
24. CAM पौधों के रन्ध्र –
(A) रात में खुलते हैं और दिन में बन्द हो जाते हैं
(B) कभी नहीं खुलते
(C) हमेशा खुले रहते हैं
(D) दिन में खुलते हैं तथा रात में बन्द हो जाते हैं।
उत्तर:
(A) रात में खुलते हैं और दिन में बन्द हो जाते हैं
25. यदि पुष्पों को काटकर तनु NaCl विलयन में डुबोया जाए तो-
(A) वाष्पोत्सर्जन कम होगा।
(B) अन्तः परासरण होगा।
(C) जीवाण्विक वृद्धि नहीं होगी।
(D) विलेय का पुष्प कोशिकाओं के अन्दर अवशोषण होगा।
उत्तर:
(B) अन्तः परासरण होगा।
26. एक कोशिका फूल जायेगी, यदि इसे रखा जाए-
(A) अल्प परासारी विलयन में
(B) अति परासारी विलयन में
(C) सम परासारी विलयन में
(D) इन सभी में।
उत्तर:
(A) अल्प परासारी विलयन में
27. पादपों में जल आपूर्ति होती है –
(A) परासरण के कारण
(B) अन्तःशोषण के कारण
(C) बिन्दुस्राव के कारण
(D) आसंजन बल के कारण
उत्तर:
(D) आसंजन बल के कारण

28. रसारोहण के लिए सर्वमान्य परिकल्पना है-
(A) केशिका परिकल्पना
(B) मूल दाबवाद
(C) स्पन्दनवाद
(D) वाष्पोत्सर्जनाकर्षण
उत्तर:
(D) वाष्पोत्सर्जनाकर्षण
29. पथ कोशिकाएँ पतली भित्तियों वाली कोशिकाएँ होती हैं जो-
(A) जड़ों की अन्तस्त्वचा में पायी जाती हैं और ये कार्टेक्स से परिरंभ में जल के परिवहन को सुगम बना देती है।
(B) पोषवाह तत्वों में होती हैं जो पदार्थों के प्रवेश बिन्दु का कार्य करते हैं जहाँ से वे पदार्थ अन्य पादप भागों तक पहुँचा दिए जाते हैं।
(C) बीजों के बीज चोलों में होती हैं ताकि बीजांकुरण के दौरान वृद्धिशील भ्रूण अक्ष उनमें से होकर बाहर आ सकें।
(D) वर्तिका के केन्द्रीय भाग में पायी जाती हैं जिसमें से होकर पराग नलिका अण्डाशय की ओर बढ़ती जाती है।
उत्तर:
(A) जड़ों की अन्तस्त्वचा में पायी जाती हैं और ये कार्टेक्स से परिरंभ में जल के परिवहन को सुगम बना देती है।
30. रसारोहण के दौरान वाहिकाओं / ट्रैकीडों में जल स्तम्भ का टूटना एवं प्रभाजन सामान्यतः किसके कारण नहीं होता-
(A) लिग्नीकृत मोटी भित्तियाँ
(B) संसंजन तथा आसंजन
(C) मंद गुरुत्वाकर्ष अभिकर्ष
(D) वाष्पोत्सर्जन अभिकर्ष
उत्तर:
(B) संसंजन तथा आसंजन
31. द्वार कोशिकाएँ (Guard cells) सहायक होती हैं-
(A) चारण से सुरक्षा प्रदान करने में
(B) वाष्पोत्सर्जन में
(C) बिन्दुस्रावण में
(D) संक्रमण से सुरक्षा प्रदान करने में
उत्तर:
(B) वाष्पोत्सर्जन में
32. वलयकरण प्रयोग (girdling experiment) में निम्नलिखित में से किसे हटा दिया जाता है ?
(A) केवल छाल को
(B) फ्लोएम सहित छाल को
(C) केवल फ्लोएम को
(D) सम्पूर्ण संवहन ऊतक को
उत्तर:
(B) फ्लोएम सहित छाल को
33. स्थलीय पादपों में द्वारा कोशिकाएँ निम्नलिखित में भिन्न होती हैं –
(A) माइटोकॉण्ड्रिया
(B) अन्तः प्रद्रव्यी जालिका
(C) हरित लवक
(D) कोशिका पंजर
उत्तर:
(C) हरित लवक

34. वाष्पोत्सर्जन निम्नलिखित में से किसकी अभिव्यक्ति है ?
(A) स्फीति दाब
(B) भित्तिदाब
(C) मूल दाब
(D) उपरोक्त में कोई नहीं
उत्तर:
(A) स्फीति दाब
35. पूर्णतया स्फीति (fully turgid) कोशिका में होता है-
(A) TPO = 0
(B) WP = 0
(C) DPD = 0
(D) OP = 0
उत्तर:
(C) DPD = 0
36. खनिज तत्वों हेतु मुख्य सिंक (sink) है-
(A) जीर्ण पत्तियाँ
(B) पके फल
(C) पार्श्व विभज्योतक
(D) छाल
उत्तर:
(A) जीर्ण पत्तियाँ
37. रन्धों के खुलने एवं बन्द होने की क्रिया में K+ आयनों का आगम होता है तो निम्नलिखित का निर्गमन होता है-
(A) Na+
(B) K+
(C) Cl+
(D) H+
उत्तर:
(D) H+
38. वातरन्ध्र क्या करते हैं ?
(A) वाष्पोत्सर्जन
(B) गैसीय विनिमय
(C) खाद्य अभिगमन
(D) प्रकाश संश्लेषण।
उत्तर:
(B) गैसीय विनिमय
39. जल में रखी एक कोशिका का परासरणी फैलाव मुख्यतः किसके द्वारा नियन्त्रित होता है ?
(A) रसधानी
(B) लवक
(C) राइबोसोम
(D) सूत्रकणिका।
उत्तर:
(A) रसधानी

(B) अति लघु उत्तरीय प्रश्न (Very Short Answer Type Questions)
प्रश्न 1.
शुद्ध जल का विभव कितना होता है ?
उत्तर:
शून्य बार (bars)
प्रश्न 2.
जल अणुओं का जाइलम वाहिकाओं की भित्ति के प्रति आकर्षण बल क्या कहलाता है ?
उत्तर:
आसंजन (adhesion)
प्रश्न 3.
मूल दाब को किस यन्त्र द्वारा नापा जाता है ?
उत्तर:
मैनोमीटर (manometer) द्वारा।
प्रश्न 4.
उस आयन का नाम बताइए जो रन्धों के खुलने एवं बन्द होने में भाग लेता है।
उत्तर:
पोटैशियम आयन (K+ ions )।
प्रश्न 5.
डोनन साम्यावस्था (Donnan’s equilibrium) के अनुसार यदि कोशिका में स्थिर आयन + ve हैं तो आने वाले आयन कौनसे होंगे ?
उत्तर:
-ve आयन अधिक संख्या में होंगे।
प्रश्न 6.
कार्बनिक भोज्य पदार्थ का स्थानान्तरण किस ऊतक द्वारा होता है ?
उत्तर:
फ्लोएम (phloem) द्वारा।
प्रश्न 7.
द्रव्य प्रवाह परिकल्पना किसने प्रस्तुत की ?
उत्तर:
मुंच (Munch) ने।
प्रश्न 8.
किन पौधों में रन्ध्र दिन में बन्द व रात में खुलते हैं ?
उत्तर:
माँसल पौधों में- जैसे-नागफनी (Opuntia)।
प्रश्न 9.
नमक के घोल में अंगूर क्यों सिकुड़ जाते हैं ?
उत्तर:
बहि परासरण (exosmosis) के कारण।

प्रश्न 10.
रसारोहण का स्पन्दनवाद किसने प्रस्तुत किया था ?
उत्तर:
जे. सी. बोस (J. C. Bose) ने।
प्रश्न 11.
जल अणुओं के मध्य परस्पर आकर्षण को क्या कहते हैं ?
उत्तर:
संसंजन बल (cohesion force)
प्रश्न 12.
जल अवशोषण के दो पथों के नाम लिखिए।
उत्तर:
एपोप्लास्ट पथ तथा सिमप्लास्ट पथ (apolast path and symplast path)
प्रश्न 13.
रन्धों के खुलते समय रक्षक कोशिकाओं का pH कितना होता है ?
उत्तर:
pH 7-8 होता है।
प्रश्न 14.
रसारोहण क्रिया किस ऊतक द्वारा होती है ?
उत्तर:
जाइलम (xylem) द्वारा।
प्रश्न 15.
माइकोराइजा क्या है ?
उत्तर:
उच्च पादप की जड़ों तथा कवक का सहजीवी सम्बन्ध (Symbiotic association ) ।
प्रश्न 16.
जल रन्ध्र कहाँ पाये जाते हैं ?
उत्तर:
शाकीय पौधों जैसे- टमाटर, घास आदि की पत्तियों के किनारों
प्रश्न 17.
कोशिका को आसुत जल में रखने पर क्या होगा ?
उत्तर:
यह जल अवशोषण करके फट जायेगी।
प्रश्न 18.
कौन-सा जल पौधों के लिए सर्वाधिक उपयोगी होता है ?
उत्तर:
केशिका जल (capillary water)

प्रश्न 19.
मूलदाब उत्पन्न होने के लिए ऊर्जा की आवश्यकता क्यों होती
उत्तर:
मूल दाब जल के सक्रिय अवशोषण से उत्पन्न होता है। अतः इसके लिए ऊर्जा की आवश्यकता होती है।
प्रश्न 20.
बिन्दु श्रावण किससे होता है ?
उत्तर:
जलरन्ध्रों (hydrathodas) से ।
(C) लघु उत्तरीय प्रश्न -I ( Short answer type questions-I)
प्रश्न 1.
पौधों में जल एवं खाद्य पदार्थों का स्थानान्तरण किस ऊतक द्वारा होता है ? पदार्थों का दो दिशीय प्रवाह किस ऊतक में होता है ?
उत्तर:
जाइलम द्वारा जल एवं खनिज लवणों का जड़ों से ऊपर पत्तियों की ओर स्थानान्तरण होता है। पत्तियों में निर्मित खाद्य पदार्थ फ्लोएम द्वारा पहले संचयी क्षेत्रों में तथा फिर यहाँ से धीरे-धीरे उपभोग क्षेत्रों की ओर स्थानान्तरण होता है। पदार्थों का द्विदिशीय प्रवाह फ्लोयम द्वारा होता है।
प्रश्न 2.
जल विभव क्या है ?
उत्तर:
जल विभव (Water Potential ) – शुद्ध जल के अणुओं की मुक्त ऊर्जा तथा किसी अन्य तन्त्र (जैसे- विलयन में जल या पादप कोशिका या ऊतक में जल) में जल के अणुओं की मुक्त ऊर्जा में अन्तर को जल विभव ( water potential ) कहते हैं। इसे प्रीक अक्षर साई ( ) से प्रदर्शित करते हैं। जल विभव को दाब के मात्रकों में भी व्यक्त किया जाता है।
1 bar = 14.5lbf / in2 = 750mm Hg = 0.987 atm
प्रश्न 3.
अन्तःशोषण को कौन से कारक प्रभावित करते हैं ?
उत्तर:
अन्तःशोषण को निम्न कारक प्रभावित करते हैं-
1. तापमान के साथ अन्तःशोषण बढ़ जाता है।
2. pH की अधिकता अन्तःशोषण को प्रभावित करती है।
3. विलेय की सान्द्रता अधिक होने पर अन्तःशोषण दर कम हो जाती है।
प्रश्न 4.
प्रतिवाष्पोत्सर्जक क्या हैं ? चार प्रतिवाष्पोत्सर्जकों के नाम लिखिए।
उत्तर:
ऐसे पदार्थ जो वाष्पोत्सर्जन को कम करते हैं, प्रतिवाष्पोत्सर्जक कहलाते हैं।
(i) CO2
(ii) ऐब्सीसिक अम्ल
(iii) फिनाइल मर्क्यूरिक एसीटेट
(iv) ऑक्सीएथीन ।
प्रश्न 5.
पारगम्यता एवं जीवद्रव्य कुंचन में भेद कीजिए।
उत्तर:
पारगम्यता एवं जीवद्रव्य कुंचन (Permeability and Plasmolysis) – कोशिका कला का वह गुण जिसके द्वारा वह अपने से होकर गुजरने वाले अणुओं का नियन्त्रण रखती है, पारगम्यता ( permeabilily ) कहलाती है। जब रिक्तिका में से रिक्तिका रस कोशिका के बाहर निकल जाता है तथा जीवद्रव्य सिकुड़ जाता है तो इसे जीवद्रव्य कुंचन (plamolysis) कहते हैं ।

प्रश्न 6.
परासरण किसे कहते हैं ?
उत्तर:
परासरण (Osmosis) परासरण वह क्रिया है जिसमें अर्द्धपारगम्य झिल्ली द्वारा पृथक् किये गये विभिन्न सान्द्रता वाले घोलों में विलायक के अणुओं का विसरण कम सान्द्रता वाले घोल से अधिक सान्द्रता वाले घोल की ओर होता है।
प्रश्न 7.
भित्ति दाब से आप क्या समझते हैं ?
उत्तर:
जल के प्रासरण के कारण कोशिका की अन्तर्वस्तुएँ कोशिका भित्ति पर दाब डालती हैं जिसे स्फीति दाब कहते हैं। स्फीति दाब के समान कोशिका भित्ति भी एक दाब डालती है जो कि स्फीति दाब के बराबर एवं विपरीत होता है। इसे भित्ति दाव (wall pressure) कहते हैं।
प्रश्न 8.
बिन्दुस्राव के लिए उत्तरदायी दो परिस्थितियाँ लिखिए।
उत्तर:
(i) मूल दाब (root pressure)
(ii) अधिक जल अवशोषण किन्तु कम वाष्पोत्सर्जन ।
(D) लघु उत्तरीय प्रश्न- II ( Short Answer Type Questions-II)
प्रश्न 1.
पारगम्यता क्या है ? पारगम्यता के आधार पर झिल्लियाँ कितने प्रकार की होती हैं। पारगम्यता को प्रभावित करने वाले कारक लिखिए।
उत्तर:
पारगम्यता (Permeability) झिल्लियों का वह गुण जिसके कारण झिल्ली से होकर कोई विलेय अथवा विलायक गुजरता है, झिल्ली की पारगम्यता (permeability) कहलाता है। इसके आधार पर झिल्लियाँ चार प्रकार की होती हैं –
(i) अपारगम्य ( Impermeable ) – ये झिल्लियाँ विलेय या विलायक किसी को भी आर-पार नहीं होने देती, जैसे- कार्क कोशिकाओं की सुबेरिनयुक्त कोशाभित्ति ।
(ii) अर्द्ध- पारगम्य (Semi-permeable ) – यह केवल विलायक के अणुओं को अपने से पार जाने देती है; जैसे- रिक्तिका झिल्ली ।
(iii) वरणात्मक पारगम्य (Selectively permeable ) – यह आवश्यकतानुसार कुछ विलेय अणुओं को आर-पार जाने देती है जैसे—कोशिका झिल्ली (cell membrane) |
(iv) पारगम्य (Permeable ) – यह विलेय तथा विलायक दोनों को आर-पार जाने देती है। जैसे—कोशिका भित्ति ।
पारगम्यता को प्रभावित करने वाले कारक
(i) ताप, pH में अन्तर दाब आदि।
(ii) O2 की कमी, CO2 की अधिकता।
(iii) जीर्णावस्था।
प्रश्न 2.
परासरण तथा अन्तःशोषण में अन्तर लिखिए।
उत्तर:
परासरण तथा अन्तः शोषण में अन्तर
| परासरण ( osmosis): | अन्तःशोषण (Imbibition): |
| (i) यह द्रव पदार्थों द्वारा जल का अवशोषण है। | (i) यह ठोस पदार्थों द्वारा जल का अवशोषण है। |
| (ii) यह क्रिया केवल जीवित कोशिका में होती है। | (ii) जीवित कोशिका में होना आवश्यक नहीं है। |
| (iii) इसमें अर्द्ध-पारगम्य झिल्ली (semi-permeable membrane) की आवश्यकता होती है। | (iii) इसमें अर्द्ध-पारगम्य झिल्ली (semi-permeable membrane) की आवश्यकता नहीं होती है। |
| (iv) विलयन की सान्द्रता के अनुसार ही पररासरण की दिशा निर्धारित होती है। | (iv) इसमें सान्द्रता का महत्व नहीं है। |
प्रश्न 3.
परासरण का पौधों में महत्व लिखिए।
उत्तर:
परासरण का महत्व (Importance of Osmosis) – पौधों में परासरण के निम्नलिखित महत्व हैं-
(i) इसके फलस्वरूप मूलरोमों द्वारा जल का अवशोषण होता है।
(ii) एक कोशिका से दूसरी कोशिका में जल का स्थानान्तरण होता है।
(iii) कोशिका की स्फीति (turgidity) बनी रहती है।
(iv) रन्ध्रों के खुलने एवं बन्द होने की क्रिया होती है।
(v) वाष्पोत्सर्जन में सहायक होता है।

प्रश्न 4.
निम्नलिखित के कारण लिखिए-
(क) बाढ़ के पानी में अधिक दिनों तक डूबे रहने के कारण पौधे नष्ट हो जाते हैं।
(ख) समुद्री जन्तु या पौधे को अलवणीय जल में रखने पर वह जीवित नहीं रहता, जबकि उचित मात्रा में जल यहाँ भी उपलब्ध है।
(ग) रन्ध्रीय एवं उपत्वचीय वाष्पोत्सर्जन की तुलना के लिए केवल पृष्ठाधारी पत्ती ही क्यों प्रयोग की जाती है ?
(घ) पौधघर से पौधों का बगीचे में स्थानान्तरण सायंकाल में करना क्यों लाभदायक है ?
उत्तर:
(क) बाढ़ के पानी में डूबे रहने से पौधों की अनेक क्रियाएँ प्रभावित होती हैं। इनमें प्रकाश संश्लेषण, वाष्पोत्सर्जन एवं श्वसन क्रियाएँ बन्द हो जाती हैं। जड़ों में श्वसन न हो पाने के कारण सक्रिय अवशोषण बन्द हो जाता है। रन्नों के बन्द हो जाने से गैसों का विनिमय (exchange of gases) नहीं हो पाता । अन्ततः पौधे की क्रियाएँ शिथिल होकर वह मर जाता।
(ख) समुद्र जलीय पौधे को अलवणीय जल में रखने पर इनमें अन्त: परासरण (endosmosis) होने लगता है जिससे इनकी कोशिकाएँ फटने लगती हैं।
(ग) पृष्ठाधारी पत्तियों (dorsiventral leaves) के एक ओर अधिक तथा दूसरी ओर कम प्रकाश पड़ता है। इसकी पृष्ठ सतह पर मोटी उपचर्म (cuticle) होती है और रन्ध्रों (stomata) की संख्या भी कम होती है। अतः इन पत्तियों की पृष्ठ सतह से वाष्पोत्सर्जन कम तथा अधर सतह से अधिक होता है।
(घ) सायं के समय पत्तियों में निर्मित खाद्य पदार्थ विलेय अवस्था में आकर निचले भागों में अधिक पहुँचता है। इसी कारण शीर्षो पर वृद्धि की दर भी सायंकाल में बढ़ जाती है। अतः पौधे को जमने में अधिक समय नहीं लगता है।
प्रश्न 5.
निम्नलिखित पर संक्षिप्त टिप्पणियाँ लिखिए – (क) परासरण दाब, (ख) प्लानि या मुर्झाना।
उत्तर:
(क) परासरण दाब (Osmotic Pressure):
परासरण दाब दो भिन्न-भिन्न सान्द्रता वाले विलयनों के बीच रखी गई अर्द्धपारगम्य झिल्ली के दोनों ओर वाले उच्चतम विसरण दाब ( diffusion pressure) को कहते हैं। परासरण दाब के कारण ही अर्द्धपारगम्य झिल्ली के दोनों ओर परासरण की क्रिया होती है। परासरण दाब को वायुमण्डलीय दाब ( atm) में मापा जाता है। यह विलेय अणुओं के अनुक्रमानुपाती होता है। विलेय की मात्रा बढ़ाने पर यह बढ़ता है। दूसरे शब्दों में, “किसी विलयन का परासरण दाब (OP) वह दाब है जो उस विलयन को अर्द्धपारगम्य झिल्ली द्वारा विलायक से पृथक् करने पर अधिक सान्द्रता वाले विलयन में विलायक के परासरण (Osmosis) के कारण उत्पन्न होता है।”
(ख) ग्लानि या मुर्झाना (wilting):
अत्यधिक वाष्पोत्सर्जन या जड़ों द्वारा कम जल अवशोषण के कारण पौधे में जल की कमी हो जाती है जिससे कोशिकाओं का स्फीति दाब (turgor pressure) कम हो जाता है। इसके कारण पत्तियाँ नीचे की ओर लटक जाती हैं। ऐसी स्थिति को ग्लानि या मुर्झाना (wilting) कहते हैं। जब पत्तियाँ दोपहर के समय मुर्झाती हैं तथा सायंकाल फिर सीधी हो जाती हैं तो इसे अस्थाई म्लानि कहते हैं। यदि मृदा में जल की कमी हो जाय तो यह स्थाई म्लानि में बदल सकती है। इस स्थिति में पौधा मर जाता है।
प्रश्न 6.
रन्ध्र तथा जलरन्ध्र में अन्तर स्पष्ट कीजिए।
उत्तर:
रन्ध्र तथा जलरन्ध्र में अन्तर –
| रन्य (Stomata) | जलरन्य (Hydrathodes) |
| रन्ध्र (stomata) पौधों के वायवीय अंगों (पत्ती, कोमल तने) आदि पर मिलते हैं। | जलरन्ध्र (hydrathodes) केवल कुछ पत्तियों पर मिलते हैं। |
| ये पत्ती, दल आदि की ऊपरी तथा निचली बाह्य त्वचा (upper or lower epidermis) पर मिलते हैं। | ये केवल पत्ती के किनारे (margin) पर मिलते हैं। |
| इनमें रक्षक कोशिकाएँ (guard cells) पायी जाती हैं। | इनमें नहीं मिलती हैं। |
| रक्षक कोशिकाओं क्लोरोप्लास्ट मिलता है। | जलरन्ध्र (hydrathodes) को घेरने वाली कोशिकाओं में क्लोरोप्लास्ट नहीं मिलता है। |
| रन्ध्र स्फीति तथा श्लथ (flaccid) दशा में खुलते तथा बन्द होते हैं। | जलरन्ध्र्र हमेशा खुले रहते हैं। |
| केवल, शुद्ध जल बाहर वाष्प (vapour) बनकर निकलता है। | जल द्रव के रूप में निकलता है तथा उसमें शर्करा, खनिज आदि मिले होते हैं। |
| रन्ध्र के नीचे रन्ध्रीय गुहा (stomatal cavity) पायी जाती है। | जलरन्द्र के नीचे की ओर एपीथेम कोशिकाएँ मिलती हैं। |
| रन्ध्र का शिरा से कोई सम्बन्ध नहीं होता है। | यह शिरा के अन्त में बनते हैं। |
प्रश्न 7.
वाष्पोत्सर्जन तथा बिन्दुख्तावण में अन्तर लिखिए।
उत्तर:
वाष्पोत्सर्जन तथा बिन्दुस्रावण में अन्तर
| वाघ्मोत्सर्जन (Transpiration): | बिन्दुसावण (Guttation): |
| यह क्रिया दिन में होती है। | यह क्रिया रात में होती है। |
| पानी वाष्प बनकर उड़ता है। यह क्रिया रन्ध्रों (stomata) द्वारा होती है। | पानी द्रव के रूप में निकलता है। |
| वाष्पोत्सर्जित (transpirated) जल शुद्ध होता है। | यह जलरन्ड्रों (hydrathodes) द्वारा होती है जो शिराओं के अन्त में स्थित होते हैं। |
| यह क्रिया रन्ध्रों (stomata) से नियन्त्रित हैं। | बिन्दु श्रावित जल अशुद्ध होता है परन्तु इसमें खनिज तथा शर्करा आदि पाए जाते हैं। |
| यदि सतह का तापमान घटा दिया जाय तो वाष्पोत्सर्जन (transpiration) की क्रिया धीमी पड़ जाती है। | यह क्रिया अनियन्त्रित है। |
प्रश्न 8.
निक्किय व सक्रिय खनिज अवशोषण में अन्तर लिखिए। उत्तरि्क्रिय व सक्रिय खनिज अवशोषण में अन्तर
उत्तर:
| निक्क्रिय खनिज अवशोषण (Passive Mineral Absorption) | सक्रिय खनिज अवशोषण (Active Mineral Absorption) |
| इसमें ऊर्जा की आवशयकता नहीं होती है। | इसमें ऊर्जा की आवश्यकता होती है। |
| यह कोशिका कला से अधिक सान्द्रता से कम सान्द्रता की ओर होता है । | यह कोशिका कला द्वारा सान्द्रण प्रवणता (concentration gradient) के विरुद्ध कम रासायनिक विभव से अधिक की ओर होता है। |
| यह कोशिका भित्ति व रिक्तिका (vacuole) के मध्य उपस्थित कोशिकाद्रव्य से होता है। | यह कोशिका कला तथा रिक्तिका कला (tonoplast) द्वारा होता है। |
| इसे सामान्यतः पम्प नहीं कहते हैं। | इसे सामान्यतः पम्प कहते हैं। |
| यह क्रिया अचानक होती है तथा सन्तलन होने तक चलती है। | इस क्रिया में किसी प्रकार का सन्तुलन स्थापित नहीं होता है। |
प्रश्न 9.
निष्क्रिय अवशोषण तथा सक्रिय जल अवशोषण में अन्तर लिखिए।
उत्तर:
निक्क्रिय व सक्रिय जल अवशोषण में अन्तर
| निक्किय जल अवशोषण (Passive water Absorption): | सक्रिय जल अवशोवण (Active Water Absorption): |
| क्रियात्मक विभव पौधे के वायवीय भागों में उत्पन्न होता है। | इसके लिए क्रियात्मक विभव मूल की कोशिकाओं में उत्पन्न होता है। |
| तेजी से वाष्पोत्सर्जन (transpiration) के कारण जाइलम वाहिनियों में वाष्पोत्सर्जन खिंबचाव उत्पन्न होता है। | जड़ें धीमी गति से जल को भमि से परासरित करती रहती हैं और दारु वाहिनियों में भेजती रहती हैं। |
| वह खिंचाव मूलीय जाइलम (xylem) में पहुँचा दिया जाता है। | अतः मूलदाब (root pressure) उत्पन्न होता है। |
| जड़ें निक्रिय अवशोषण तल का कार्य करती हैं। | यह क्रिया धीमी गति से वाष्पोत्सर्जन करते हुए पादप के जाइलम (xylem) पर पर्याप्त दाब बनाती है। |
| अवशोषण मूल के माध्यम से होता है। | अवशोषण मूल के द्वारा होता है। |
प्रश्न 10.
निम्नलिखित पर संक्षिप्त टिप्पणियाँ लिखिए –
(क) बिन्दुस्राव
(ख) रसस्राव।
उत्तर:
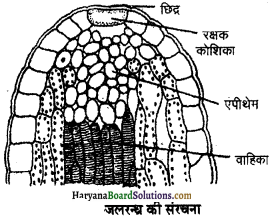
बिन्दुस्राव (Guttation ) – पत्तियों के किनारों (Margins) जल की छोटी-छोटी बूंदों का स्रावण (Secretion) बिन्दुस्राव कहलाता है। छिद्र कोशिका से अरबी (Colocasia ), टमाटर, आलू, घास आदि शाकीय पौधों की पत्तियों में यह क्रिया प्रातः काल के समय स्पष्ट देखी जा सकती है। इनमें पत्तियों के किनारों पर सूक्ष्म छिद्र पाये जाते हैं जिन्हें जलरन्ध्र (hydrathodes) कहते एपीथेम वाहिका हैं। इन जलरन्ध्रों में एपीथेम (epithem) कोशिकाएँ पायी जाती हैं जो जाइलम से जल ग्रहण करके जलरन्ध्रों से होकर इसे बूंदों के रूप में बाहर निकालती हैं।
रसस्राव (Latex secretion) – पौधे के किसी क्षतिग्रस्त या कटे हुए भाग से जल सदृश रस या लैटेक्स (latex) का बाहर निकलना रसस्राव कहलाता है। पाम (palm) के पौधे में यह फ्लोएम से होता है। कनेर (Nerium), आम आदि में यह स्राव लैटेक्स (latex) के रूप में होता है।

(E) निबन्धात्मक प्रश्न (Long Answer Type Questions )
प्रश्न 1.
परासरण किसे कहते हैं ? किसी एक प्रयोग द्वारा परासरण क्रिया प्रदर्शित कीजिए।
उत्तर:
परासरण (Osmosis):
faeft अर्द्धपारगम्य (semi- permeable) कला से होकर एक विलयन से दूसरे विलयन की ओर जल के अणुओं के विसरण को परासरण ( osmosis) कहते हैं। जल के अणुओं का यह विसरण कम सान्द्रता वाले घोल से अधिक सान्द्रता वाले घोल की ओर होता है। परासरण की क्रिया दो प्रकार की होती है –
1. बहि: परासरण (Exosmosis) – कोशिका को किसी सान्द्र विलयन ( अतिपरासारी) में रखने पर कोशिका के अन्दर से जल बाह्य विलयन में जाने लगता है, इसे बहि: परासरण (exomosis) कहते हैं। जैसे- अंगूर को शर्करा या नमक के गाढ़े घोल में रखने पर यह सिकुड़ जाता है।
2. अन्तःपरासरण (Endosmosis) – कोशिका को आसुत या शुद्ध जल (अल्पपरासारी) में रखने पर जल के अणु कोशिका में प्रवेश करते हैं, इसे अन्त:परासरण (endosmosis) कहते हैं। जैसे- किशमिश (dry grapes) को जल में रखने पर ये जल अवशोषित कर फूल जाते हैं।
परासरण का प्रदर्शन (Demonstration of Osmosis)
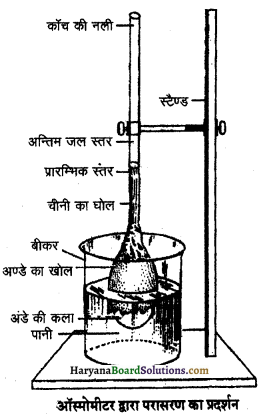
अण्डे का ऑस्मोमीटर (Egg Osmometer ) – मुर्गी का साबुत अण्डा (egg) लेकर इसमें छोटा-सा एक गोल छेद करके इसका अन्तःपदार्थ निकाल देते हैं। अब अण्डे के खोल को हाइड्रोक्लोरिक अम्ल (HCI) में कुछ देर रखते हैं। जिससे इसका कैल्शियम कार्बोनेट का बना कड़ा घोल घुल जाता है और जीवद्रव्य कला बचती है। जीवद्रव्य कला को कांच की एक नली को कला में उपस्थित छिद्र में डालकर बाँध देते हैं। अब इस कला में चीनी का गाढ़ा घोल भरकर इसे जल से भरे बीकर में चित्रानुसार रखकर स्टैण्ड से कस देते हैं। कुछ समय बाद हम देखते हैं कि काँच की नली में जल का तल काफी ऊपर चढ़ गया है। इससे स्पष्ट है कि जीवद्रव्य कला से होकर जल के अणु अन्तःपरासरण (endosmosis) द्वारा अण्डे की झिल्ली के अन्दर घोल में प्रवेश करते हैं।
प्रश्न 2.
निम्नलिखित पर संक्षिप्त टिप्पणियाँ लिखिए –
(क) आयन विनिमय
(ख) डोनन साम्यावस्था
(ग) वाहक संकल्पना
(घ) बेनेट क्लार्क का प्रोटीन लेसीथिन सिद्धान्त
(ङ) खनिज स्थानान्तरण।
उत्तर:
1. आयन विनिमय (Ion Exchange) – मृदा में खनिजों का अवशोषण आयनों (ions) के रूप में होता है। ये आयन मूलरोम (root hairs) की सतह पर अधिशोषित होते हैं तथा उनका विनिमय अपने ही प्रकार के आयनों से हो जाता है। यह क्रिया निम्न दो प्रकार से होती है-
(a) सम्पर्क आयन विनिमय (Contact Ion Exchange) – मृदा के कणों पर उपस्थित आयन जड़ की सतह पर उपस्थित आयनों के सम्पर्क में आकर बदल जाते हैं।
(b) काबोंनिक अम्ल विनिमय (Carbonic Acid Exchange)- जड़ों द्वारा श्वसन प्रक्रिया में छोड़ी गयी CO2मृदा जल से क्रिया करके कार्बोनिक अम्ल H2CO3 बनाती हैं। कारोनिक अम्ल H+तथा HCO3आयनों में टूट जाता है। H+ मृदा में उपस्थित दूसरे विद्युत धनात्मक तत्वों से मिलकर पौधों द्वारा अवशोषित होते
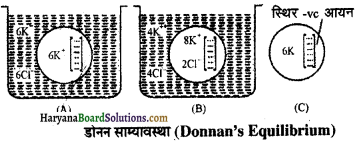
2. डोनन-साम्यावस्था (Donnan’s Equilibrium)-ऐसे आयन जो कोशिका कला से बाहर नहीं आ सकते, स्थिर आयन (fixed ions) कहलाते हैं। कोशिका कला धनात्मक +ve तथा ऋणात्मक -ve दोनों प्रकार के आयनों को भीतर आने दे सकती है। सामान्यतः कोशिका में कला से होकर जितने आयन प्रवेश करते हैं उतने ही
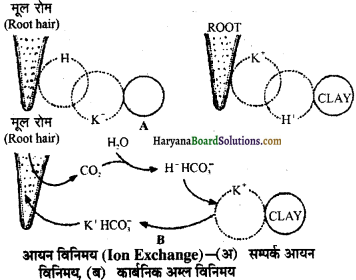
दूसरे प्रकार के आयन बाहर निकल आते हैं। इस प्रकार आयनों की स्थिति सन्तुलित बनी रहती है, जो – ve आयन कोशिका से बाहर नहीं जा सकते उनके लिए +ve आयन बाहर से आते हैं। इस प्रकार अन्दर प्रवेश करने वाले + ve आयन की संख्या – ve आयनों से अधिक होती है। यदि स्थिर आयन + ve हैं तो अन्दर प्रवेश करने वाले – ve आयन्स की संख्या अधिक होगी। इसे डोनन साम्यावस्था कहते हैं।
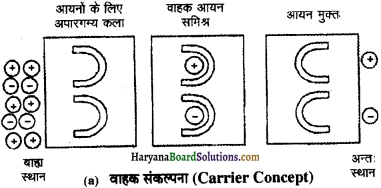
3. वाहक संकल्पना (Carrier Concept) कोशिका कला में मुक्त आयनों के विनिमय के लिए वाहक मिलते हैं, जो आयनों से मिलकर वाहक आयन समिश्र (Carrier Ion Complex) बनाते हैं। ये वाहक (Carriers) उन आयनों को कोशाकला से पार ले जाते हैं। ये वाहक (Carriers) सक्रिय अवशोषण (Active absorption) करते हैं। आयन्स का अवशोषण केवल संतृप्त दशा तक होता है।

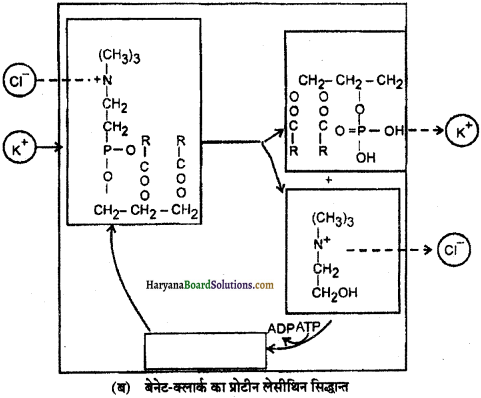
(घ) बैनेट-क्लार्क का प्रोटीन लेसीथिन सिद्धान्त (Protein Lecithin Theory of Bennet Clark) – बेनेट तथा क्लार्क (1956) ने कोशिका कला में प्रोटीन तथा फॉस्फोलिपिड की उपस्थिति को बताया। जहाँ प्रोटीन लैसीथिन (फॉस्फोटाइड) से बन्धित होते हैं। इनमें उपस्थित फाँस्फेट समूह + ve आयनो का बाँधता है जो कला के अन्दर की ओर लैसीथिनेज़ (lacithinase) विकर की क्रिया से मुक्त होते हैं। लेसीथिन का संश्लेषण पुनः कोलीन एसीटाइलेज (cholineacetylase) विकर की उपस्थिति में फॉस्फेटिडिक अम्ल (phosphatidic acid) एवं कोलीन (choline) से होता है।
खनिज आयनों का स्थानान्तरण (Translocation of Mineral Ions) – जब आयन सक्रिय या निक्क्रिय उद्र्रहण से या फिर दोनों की सम्मिश्रित प्रक्रिया के माध्यम से जाइलम में पहुँच जाते हैं, तब उनका परिवहन पादप तने एवं सभी भागों तक वाष्पोत्सर्जन प्रवाह के माध्यम से होता है। खनिज तत्वों के लिए मुख्य कुंड पौधे की वृद्धि का क्षेत्र होता है जैसे कि शिखाग एवं पार्श्व विभज्योतक (meristems), तरुण पत्तियाँ, विकासशील फूल, फल एवं बीज तथा भंडारण अंग। खनिज आयनों का विसर्जन महीन शिराओं के अन्तिम छोर पर कोशिकाओं के द्वारा विसरण एवं सक्रिय उद्ग्रण से होता है। खनिज आयनों को जल्दी ही पुनः संघटित विशेष रूप से पुराने जरावस्था (senescing) वाले भाग से किया जाता है। पुरानी तथा मरती हुई पत्तियाँ अपने भीतर के खनिजों को नई पत्तियों में निर्यातित (export) कर देती है।
ठीक इसी प्रकार से पत्तियाँ पर्णपाती वृक्ष (deciduous tree) से झड़ने से पहले अपने खनिज तत्त्वों को अन्य भागों को दे देती हैं। जो पदार्थ प्रायः त्वरित संचारित या संघटित होते हैं, वे हैं फॉस्फोरस, सल्फर, नाइट्रोजन तथा पौटेशियम। कुछ तत्व जो कि संरचनात्मक कारक होते हैं, जैसे कि कैल्सियम इन्हें पुनः संघटित नहीं किया जाता है। जाइलम स्राव का विश्लेषण यह दर्शाता है कि कुछ नाइट्रोजन अकार्बनिक आयनों के रूप में ढोए (carried) जाते हैं। इसी तरह फॉस्फोरस एवं सल्फर भी कार्बनिक यौगिकों के रूप में पहुँचाए जाते हैं। इसके अलावा जाइलम एवं फ्लोएम के बीच भी पदार्थों का आदान-्रदान होता है। अतः हम स्पष्ट रूप से अन्तर नहीं कर पाते कि जाइलम केवल अकार्बनिक पोषकों का परिवहन करता है तथा फ्लोएम कार्बनिक पदार्थों का, जैसा कि पहले विश्वास किया जाता है।
प्रश्न 3.
विसरण दाब न्यूनता से आप क्या समझते हैं ?
अथवा
पौधों की कोशिका में विसरण दाब न्यूनता, परासरण दाब, स्फीति दाब एवं भित्ति दाव में सम्बन्ध स्थापित कीजिए।
उत्तर:
1. परासरण दाब (Osmotic Pressure or OP)-परासरण दाब (O P) वह दाब है जो किसी विलयन पर बाहर से अनुप्रयुक्त करने पर विलायक के उस परासरण को रोकती है जो उस विलयन (solution) को उसके विलायक (solvent) से अर्द्धपारगम्य कला द्वारा पृथक् करने पर विलयन की ओर होता है। दूसरे शब्दों में, किसी भी विलयन को उसके विलायक (जल) से अर्द्धपारगम्य झिल्ली द्वारा पृथक् करने पर विलयन में उत्पन्न होने वाले अधिकतम दाब को परासरण दाब (OP) कहते है। किसी विलयन का परासरण दाब (OP) विलायक में उपस्थित विलेय पदार्थ के अणुओं की संख्या के समानुपाती होती है। किसी कोशिका में परासरण दाब (OP) तथा स्फीति दाब (TP) दोनों परासरण क्रिया के कारण उत्पन्न होते हैं। कुछ पदार्थों में जल का परासरण दाब (OP) सदैव शून्य होता है। जल का प्रवाह सदैव कम परासरी सान्द्रता से अधिक परासरी सान्द्रता की ओर होता है। परासरण दाब मापने के लिए ओस्मोमीटर (osmometer) नामक यन्त्र का प्रयोग किया जाता है।
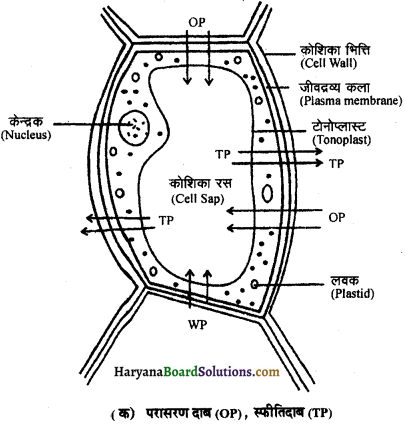
2. आशून या स्पीति दाब (Turgor Pressure TP) – किसी भी कोशिका में कोशिकाद्रव्य तथा कोशिकांग कोशिकाकला (plasmalemma) द्वारा घिरे रहते हैं। कोशिका झिल्ली के बाहर कोशिकाभित्ति (cell wall) होती है जो सेल्युलोज की बनी होती है जब किसी पादप कोशिका को जल में रखा जाता है तो जल कोशिका की रिक्तिका में रस का परासरण दाब (OP) अधिक होने लगता है, क्योंकि बाहर से जल के अणु कोशिका में विसरित होने लगते हैं, जिसके फलस्वरूप जीवद्रव्य कला या प्लाज्मालेमा कोशिकाभित्ति पर दबाव डालने लगती है जिसे आशून या स्पीति दाब्ब (TP) कहते हैं।
3. भित्ति दाब (Wall Pressure ; WP) – कोशिकाभित्ति मजबूत होती है जिसके फलस्वरूप स्फीति दाब के समान किन्तु विपरीत दिशा में जीवद्रव्य पर कोशिका भित्ति एक दाब उत्पन्न करती है अर्थात् स्फीति दाब (TP) का विरोध करती है, इसे भित्ति दाब (WP) कहते हैं। भित्ति दाब (WP) तथा स्फीति दाब (TP) के कारण ही कोशिकाएँ आशून (turgid) रहती हैं और आशून दाब (TP) के कम होने पर ही पत्तियाँ मुरझाती हैं।
विसरण दाब न्यूनता (Diffusion Pressure Deficit):
जीवित कोशिकाएँ प्रायः परासरण मापी (osmometer) के रूप में कार्य करती हैं। पादप कोशाभित्ति पूर्णत: पारगम्य (permeable) होती है। अतः ये शरीर क्रियात्मक दृष्टि से अधिक उपयोगी नहीं हैं, परन्तु यह कोशिका को एक निश्चित आकार प्रदान करती हैं। कोशाभित्ति के अन्दर की ओर अर्द्धपारगम्य कला (semipermeable membrane) होती है। पादप कोशिकाओं (plant cells) में एक बड़ी रसधानी (vacuole) होती है जिसमें कोशिका रस (cell Sap) भरा होता है। कोशिकाद्रव्य (cytoplasm) को रसधानी से अलग करने वाली झिल्ली टोनोप्लास्ट (tonoplast) कहलाती है। यह भी प्लाज्माकला (plasma membrane) के समान होती है। कोशिका के परासरण (osmosis) के लिए आवश्यक दशाएँ होती हैं।
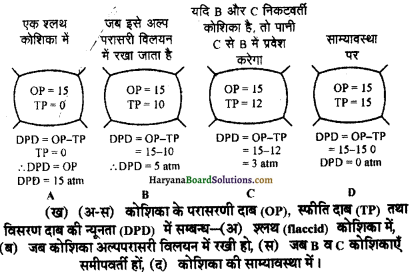
जब कोशिका को जल में रखा जाता है तो इसके द्वारा जल अवशोषण (absorption) के कारण स्फीति दाब (TP) बढ़ता है और साथ ही भित्ति दाब (WP) भी बढ़ता जाता है। साम्यावस्था स्थापित होने पर स्फीति दाब (TP) परासरण दाब के बराबर होता है।
परासरण दाब = स्फीति दाब
OP = TP
OP – TP = 0
साम्यावस्था स्थापित होने से पूर्व परासरणी दाब (OP) एवं स्पीति दाब (TP) के कारण जल के अणु कोशिका में प्रवेश करते हैं। अतः जल का कोशिका के अन्दर प्रवेश करना अथवा न करना इन दोनों दाबों के अन्तर पर ही निर्भर करता है। अतः वह शक्ति जो कोशिका में जल (अथवा विलायक) के अणुओं के आने-जाने को नियत्रित करती है, उसे विसरण दाव्ब न्यूनता (Diffusion Pressure Deficit : DPD) कहते हैं। इसे कोशिका का चूष्ण दाब (Suction Pressure; SP) भी कहते हैं।
विसरण दाब न्यूनता = परासरण दाब – स्फीति दाब
DPD (SP) = OP – TP
चूँकि साम्यावस्था में OP = TP
इसलिए इस स्थिति में विसरण दाब न्यूनता
DPD = 0
श्लथ (Flaccid) कोशिका का स्फीति दाब (TP) शून्य होता है तथा ऐसी
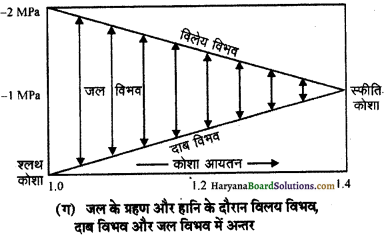
स्थिति में कोशिका रस का परासरण दाब (OP) विसरण दाब न्यूनता (DPD) के बराबर होता है।
यदि TP = 0 हो, तो
DPD = OP
जब कोशिका को अल्पपरासरी विलयन (hypotonic solution) में रखा जाता है तो स्फीति दाब (TP) धीरे-धीरे बढ़ने लगता है साथ ही परासरण दाब (OP) कम होने लगता है। स्फीति दाब के बढ़ने तथा परासरण दाब के कम होने से DPD भी कम होता रहता है। जब कोशिका पूर्ण रूप से स्सीति (turgid) होती है तब OP, TP के बराबर हो जाता है। उस समय DPD का मान शून्य होता है।

प्रश्न 5.
मूलदाब किसे कहते हैं ? चित्र द्वारा मूल दाब का प्रदर्शन के लिए एक प्रयोग लिखिए।
उत्तर:
मूल दाब्ब सिद्धात (Root Pressure Theory) – सर्वप्रथम स्टीफन हेल्स (1727) ने मूल दाब (Root Pressure) शब्द का प्रयोग किया था। मूलरोम मृदा से जल अवशोषित करते हैं। वल्कुट कोशिकाएँ (cortical cells) मूलरोमों (root hairs) से जल प्रहण करके जाइलम वाहिनियों (xylem vessels) में अत्यधिक दबाव के साथ पहुँचाती हैं, इस दाब को मूलदाब (root pressure) कहते हैं।
मूल दाब का प्रदर्शन निम्न प्रयोग द्वारा किया जा सकता है –
मूलदाब का एक प्रयोग द्वारा प्रदर्शन (Demonstration of Root Pressure by an Experiment) – गमले में लगा एक छोटा पौधा लेकर इसे जल से भरी एक नाद में रख देते हैं। जल के अन्दर ही पौधे को मिट्टी से 7.8 cm ऊपर से तेज चाकू से काटकर ऊपरी भाग अलग कर देते हैं। तने के कटे हुए सिरे पर रबर की सहायता से काँच की एक नली लगा देते हैं। उपकरण को चित्रानुसार स्टैण्ड में कस देते हैं। काँच की नली के स्थान पर मैनोमीटर (manometer) भी लगाया जा सकता है।
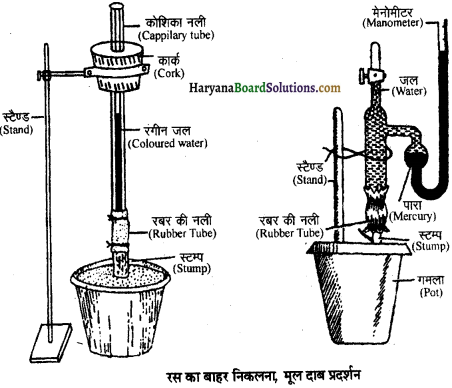
मैनोमीटर की U नली में पारा Hg भरा होता है। रबर की नली के अन्दर तथा मैनोमीटर के शेष भाग में जल भर लेते हैं। उपकरण को चित्रानुसार स्टैण्ड में कस देते हैं। मैनोमीटर के स्केल पर जल या पारे का तल प्रयोग प्रारम्भ करने से पहले तथा प्रयोग समाप्त होने के बाद पढ़ लेते हैं। मैनोमीटर की खड़ी भजा में पारे का तल में वृद्धि दाब को प्रदर्शित करता है। कटे हुए तने की जाइलम वाहिनियों से मूलदाब (root pressure) के कारण जल रबर की नली में उपस्थित जल में आता है, जिससे मैनोमीटर में पारे का तल ऊपर की ओर बढ़ जाता है।
2. जैव शक्तिवाद (Vital Force Theory) – रसारोहण की क्रियाविधि को समझाने के लिए भारतीय वनस्पति विज्ञानी सर जे. सी. बोस (Sir J. C. Bose) ने 1923 में जैविक शक्तिवाद प्रस्तुत किया। इसे बोस का स्पद्दन सिद्धान्त (Bose’s Pulsation Theory) भी कहते हैं। इन्होंने रसारोहण की क्रिया को स्वनिर्मित क्रिस्कोग्राफ उपकरण द्वारा प्रदर्शित किया। ड्वाक्टर बोस ने अपने प्रयोग द्वारा सिद्ध किया कि तने की सबसे भीतरी कारेंक्स की कोशिकाओं में स्पन्दन गति (pulsation movement) होती है, जिसके कारण रसारोहण होता है जैसा कि चित्र में दर्शाया गया है।
3. भौतिक बल सिद्धांत (Physical Force Theory):
इस वाद के अनुसार रसारोहण की क्रिया निर्जीव कोशिकाओं में ही होती है, अनेक वैज्ञानिकों ने इसका समर्थन किया है। इसके अन्तर्गत महत्वपूर्ण सिद्धान्त निम्न प्रकार हैं –
(i) कोशिका बल सिद्धातत (Capillary Force Theory) – वोहम (1809) के मतानुसार जाइलम की वाहिकाएँ केशिका नली की भांति कार्य करती हैं जिनमें जल केशिका बल (capillary force) के कारण ऊपर चढ़ता है, किन्तु इस मत को मान्यता प्राप्त नहीं हो सकी क्योंकि वाहिकाओं का व्यास इतना कम नहीं होता और न ही इस के अनुसार जल पौधों की इतनी ऊँचाई तक पहुँच सकता है।
(ii) अन्त:शोषणवाद (Imbibition Theory) – सेक्स (1878) के अनुसार जाइलम वाहिनियों में जल अन्तःशोषण के कारण चढ़ता है परन्तु यह मत भी मान्य नहीं है।
(iii) वाद्योत्सर्जन खिंचाव एवं डिक्सन का ससंजनवाद (Transpiration Pull and Dixon’s Theory of Cohesion)
इस मत के अनुसार पौधों में लगातार वाष्पोत्सर्जन (transpiration) के कारण जल ऊपर चढ़ता रहता है तथा खड़ी दिशा में पानी का स्तथ (water column) टूटता नहीं है। इस मत को डिक्सन तथा जौली (1894) ने अपने प्रयोगों द्वारा सिद्ध किया।
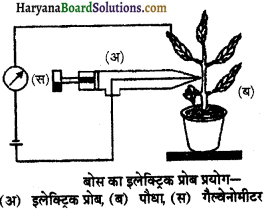
इस सिद्धान्त को निम्न तीन भागों में समझा जा सकता है –
(i) वाप्योत्सर्जन कर्षण (Transpiration Pull) – पौधों में वाष्पोत्सर्जन (transpiration) की क्रिया द्वारा जल की कमी होने से पर्णमध्योत्तक कोशिकाओं (mesophyll cells) में भी जल की कमी हो जाती है। यह कमी जाइलम द्वारा जल की आपूर्ति से पूर्ण की जाती है। जाइलम में जल की कमी या विसरणदाब न्यूनता (DPD) से एक खिंचाव या तनाव उत्पन्न होता है जिसे वायोत्सर्जन कर्षण (transpiration pull) कहते हैं। यह कर्षण पत्ती के जाइलम से जड़ों के जाइलम तक उत्पन्न होता जाता है। यह कर्षण ॠणात्मक खिंचचाव कहलाता है, क्योंकि यह वायवीय भाग.से भूमिगत भाग की ओर उत्पन्न होता है तथा वाष्पोत्सर्जन के कारण उत्पन्न होता है।

(ii) जल का संसंजक बल (Cohesive Force of Water)-जल के अणुओं के बीज एक प्रबल बल कार्य करता है जिसे संसंजक बल (cohesive force) कहते हैं। इस बल के कारण जल के अण अधिक मजबती से ज़ड़े रहते हैं तथा जल के अणुओं को पृथक् करना कठिन होता है। जल के अणुओं तथा कोशिका भित्ति (cell wall) के बीच उत्पन्न बल को आसंजक बल (adhesive Force) कहते हैं। ये दोनों बल जाइलम कोशिका में एक साथ कार्य करते हैं जिससे जल स्तंभ की निरन्तरता बनी रहती है।
(iii) जल स्तम्भ की निरन्तरता (Continuity of Water Column) – जल का स्तम्भ जाइलम कोशिका की गुहा (lumen) में लगातार बनता है, जो आसानी से नहीं टूटता है।
डिक्सन तथा जौली ने निष्कर्ष निकाला कि –
(a) पौधों में पत्तियों द्वारा निरन्तर वाष्पोत्सर्जन (transpiration) होता रहता है जिससे वाष्पोत्सर्जन खिंचाव (transpiration pull) उत्पन्न होता है।
(b) पानी में अणुओं को अत्यन्त बल के साथ जकड़े रहने का गुण होता है जिसे संसजन शक्ति कहते हैं। इसी गुण के कारण पानी यूकेलिप्टस जैसे ऊँचे वृक्षों में 120 फीट तक चढ़ सकता है।
प्रश्न 6.
वाष्पोत्सर्जन से आप क्या समझते हैं ? वाष्पोत्सर्जन के प्रदर्शन के लिए बेलजार प्रयोग को समझाइए। वाष्पोत्सर्जन को कौन-कौन से कारक प्रभावित करते हैं ?
उत्तर:
वाष्योत्सर्जन (Transpiration) – पौधों के वायवीय भागों से जल का वाष्प के रूप में उड़ना वाष्योत्सर्जन (Transpiration) कहलाता है। पोधे जितना जल मृदा (soil) से प्रहण करते हैं, उसका केवल 1% भाग ही पौधे की उपापचयी क्रियाओं में प्रयक्त होता है। शेष जल वाष्पोत्सर्जन की क्रिया में उड़ जाता है। वाष्पोत्सर्जन (transpiration) पौधों का आवश्यक दुर्गुण (necessary evil) है।
वाष्पोत्सर्जन तीन प्रकार का होता है-
(i) रन्ध्रीय वाष्पोत्सर्जन (Stomatal Transpiration)-यह रन्ध्रों द्वारा एवं कुल वाष्पोत्सर्जन का लगभग $98 \%$ होता है।
(ii) उपत्वचीय वाष्पोत्रर्जन (cuticular Trans- piration)-यह पौधे की वायवीय उपत्वचा (cuticle) द्वारा होता है। यह केवल 1.8% होता है।
(iii) लेन्टीकुलर वाष्पोत्सर्जन (Lenticular Trans- piration)-यह लेन्ओसेल्स (lenticells) द्वारा होता है। यह केवल 0.2% होता है।
प्रयोग : बेलजार प्रयोग द्वारा वाप्योत्सर्जन क्रिया का प्रदर्शन –
गमले में लगे एक स्वस्थ पौधे को लेकर इसमें पर्याप्त मात्रा में जल डालते हैं। अब गमले को मिट्टी की सतह के ऊपर पॉलीधिन से इस प्रकार बाँधते हैं कि पौधे का प्ररोह बाहर रहे जैसा कि चित्र में दिखाया गया है। अब गमले को काँच की प्लेट पर रखकर इसके ऊपर काँच का
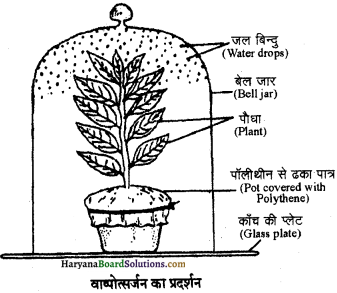
वाष्पोत्सर्जन को प्रभावित करने वाले कारक (Factors affecting Transpiration)
(अ) बाह्य कारक (External factors):
1. वायुमण्डलीय आपेक्षिक आर्द्रता (Relative humidity of atmosphere)वायुमण्डल में आर्द्रता कम होने पर वाष्पोत्सर्जन (transpiration) अधिक होता है। नम वातावरण होने पर वाष्पोत्सर्जन की दर घट जाती है।
2. प्रकाश (Light)-प्रकाश की उपस्थिति में रन्ध्र (stomata) खुलते हैं जिससे वाष्पोत्सर्जन (transpiration) अंधिक होता है। रन्ध्र बन्द होने की स्थिति में वाष्पोत्सर्जन कम होता है।
3. वायु (Wind) – तीव्र वायु वेंग की स्थिति में वाष्पोत्सर्जन (transpiration) बढ़ जाता है ।
4. तापक्रम (Temperature) – ताप बढ़ने से आपेक्षिक आर्द्रता कम हो जाती है तथा वायुमण्डल अधिक नमी ग्रहण कर सकता है। इससे वाष्पोत्सर्जन की दर बढ़ जाती है।
5. मृदा जल (Soil water) – मृदा में जल की कमी होने पर वाष्पोत्सर्जन (transpiration) कम हो जाता है।

(ब) आन्तरिक कारक (Internal factors) – पत्तियों की संरचना, रन्ध्रों की संरचना एवं प्रकार, रन्ध्रों (Stomata) की संख्या, जाइलम एवं मूलरोम की संरचना आन्तरिक कारक हैं। ये वाष्पोत्सर्जन को प्रभावित करते हैं।
वाप्योत्सर्जन की उपयोगिता (Importance of Transpiration):
1. जल एवं खनिजों के अवशोषण के लिए वाष्पोत्सर्जन एक खिंचाव (pull) उत्पन्न करता है
2. इससे मृदा जल विभिन्न पादप अंगों में खनिजों का वितरण करता है।
3. इसके द्वारा पत्तियों का ताप अपेक्षाकृत कम रहता है।
4. अतिरिक्त जल पौधों से बाहर निकलता है।
5 कोशिकाओं की स्फीति बनी रहती है।
प्रश्न 7.
रन्धों के खुलने तथा बन्द होने की मण्ड शर्करा परिकल्पना को समझाइए।
उत्तर:
रन्ध्रों के खुलने तथा बन्द होने की क्रियाविधि (Mechanism of Stomatal Opening and Closing):
द्वार कोशिकाओं की स्फीति अवस्था (turgidity) तथा श्लथ अवस्था (flaccidity) पर रन्द्रों का खुलना एवं बन्द होना निर्भर करता है। द्वार कोशिकाओं (guard cells) की परासरण सान्द्रता अधिक होने पर इनमें पानी प्रवेश करता है और कोशिका में स्फीति दाब (TP) बढ़ जाता है जिससे बाहर की भित्ति पर दबाव पड़ने से रन्ध्र खुल जाते हैं। इसके विपरीत जब द्वार कोशिका से पानी निकल जाता है तो कोशिकाएँ श्लथ (flaccid) हो जाती हैं और रन्ध्र बन्द हो जाते हैं। रन्ध्र के बंद होने तथा खुलने की क्रिया पर प्रकाश तथा अन्धकार का बहुत प्रभाव पड़ता है। इसके अतिरिक्त पानी की उपस्थिति, कोशिका रस की सान्द्रता, CO2 सान्द्रता, आदि भी इस क्रिया को प्रभावित करते हैं।
वॉन मोल (Von Mohl) ने 1856 में देखा कि यदि द्वार कोशिका (guard cells) की बाब्य त्वचा को जल के सम्पर्क में रखा जाता है तो रन्धु (stomata) खुल जाते हैं और यदि इसे शर्करा के घोल के सम्पर्क में रखा जाए तो रन्ध्र बन्द हो जाते हैं। हीथ (Heath) ने 1958 में बताया कि एक ओर की द्वारक कोशिका में एक बारीक छिद्र कर दिया जाए तो रन्ध्र एक तरफ से बन्द हो जाता है। अत: इससे सिद्ध होता है कि रन्ध्र केवल स्फीति दिशा में ही खुलते हैं। CO2 की सान्द्रता बढ़ने से रन्ध्र बन्द हो जाते हैं तथा कम होने पर एवं पानी की मात्रा बढ़ने पर रन्ध्र खुलते हैं। लगभग 30 C तापमान पर रन्ध्र खुलते हैं।
मण्ड शर्करा ⇔ अन्तरा परिवर्तन संकल्पना
(Starch ⇔ Sugar Interconversion Hypothesis)
यह संकल्पना जे. डी. सायरे (1923) ने प्रस्तुत की थी तथा इसे स्टीवार्ड ने 1964 में रूपान्तरित किया था। इस संकल्पना के प्रमुख बिन्दु निम्नवत् हैंप्रकाश में (In Light)
(i) दिन (प्रकाश) में प्रकाश-संश्लेषण की क्रिया होती है, जिसमें अन्तराकोशिकीय स्थानों में उपलब्ध श्वसनीय CO2 का उपभोग होता है।
(ii) इसके परिणामस्वरूप कोशिका रस में H+ सान्द्रता कम हो जाता है तथा रक्षक कोशिकाओं में pH मान बढ़ जाता है।
(iii) उच्च pH (7 cdot 0) फॉस्फोरिलेस एन्जाइम की क्रियाशीलता बढ़ाता है जो कि स्टॉर्च को ग्लूकोस-1-फॉस्फेट में बदलता है।
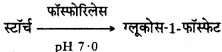
(iv) ग्लूकेस-1-फॉस्फेट, फॉस्फोग्लूकोम्यूटेस एन्जाइम की उपिस्थिति में ग्लूकोस-6-फॉस्फेट में बदल जाता है।
ग्लूकोस-6-फॉस्फेट → ग्लूकोस + फॉस्फेट
(v) ग्लूकोस-6-फॉस्फेट फॉस्फेटेस एन्जाइम की सहायता से ग्लूकोस तथा फॉस्फेट में बदल जाता है।
(vi) ग्लूकोस तथा फॉस्फेट माध्यम में घुलकर कोशिका रस की सान्द्रता बढ़ा देते हैं।
(vii) सान्द्रता बढ़ने से रक्षक कोशिकाओं का OP बढ़ जाता है तथा जल विभव कम हो जाता है। इसके परिणामस्वरूप रक्षक कोशिकाओं में परिवेश की कोशिकाओं से जल आ जाता है तथा रक्षक कोशिकाएँ स्फीति दशा में आकर फल जाती है एवं रन्ध खल जाते हैं।

अन्धकार में (In dark):
(i) अन्धकार में प्रकाश संश्लेषण नहीं होता है। उपरन्द्रीय गुहा (substomatal cavity) में श्वसनीय CO2 का स्तर बढ़ जाता है। इसके परिणामस्वरूप रक्षक कोशिकाओं में pH मान घट जाता है।
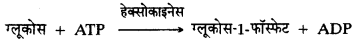
(ii) निम्न pH पर ग्लूकोस अणु हेक्सोकाइनेस एन्जाइम की उपस्थिति में ATP का प्रयोग करके ग्लूकोस-1-फॉस्फेट में परिवर्तित हो जाते हैं।
ग्लूकोस + ATP हेक्सोकाइनेस ग्लूकोस-1-फॉस्फेट + ADP
(iii) ग्लूकोस-1-फॉस्फेट अणु फॉस्फोरिलेज एन्जाइम की उपस्थिति में स्टॉर्च में बदल जाता है।
ग्लूकोस-1-फॉस्फेट → स्टॉर्च
(iv) स्टॉर्च के संश्लेषण से कोशिका रस तनु हो जाता है क्योंकि घुलित ग्लूकोस अणुओं की खपत हो जाती है। इसके फलस्वरूप कोशिका रस का OP घट जाता है तथां जल विभव बढ़ जाता है। रक्षक कोशिकाएँ समीपस्थ कोशिकाओं को जल देकर स्लथ (flaccid) हो जाती हैं एवं स्टोमेटा रन्ध्र बन्द हो जाते हैं।
सीमाएँ (Limitations) –
(i) शर्करा, स्टॉर्च अन्तरा परिवर्तन एक मन्द प्रक्रम है जो तीव्र स्टोमेटा गति को नहीं समझाता।
(ii) स्टॉर्च या अन्य बहुलीकृत पॉलीसैकेराइड प्याज के पौधों में नहीं पाए जाते हैं जबकि इनमें स्टोमेटा खुलते तथा बन्द होते हैं।
(iii) जब स्टोमेटा खुलते हैं तब रक्षक कोशिकाओं में ग्लूकोस की पहचान नहीं होती है।
(iv) स्टोमेटा के खुलते समय नीले प्रकाश की अत्यधिक प्रभाविता (extra effectiveness) को यह सिद्धान्त नहीं समझाता है।
2. प्रोटॉन स्थानान्तरण अवधारणा (स्टोमेटा की गति में K+की भूमिका) (Proton Transport Concept (Role of K+ in Stomatal Movement) इस सिद्धान्त को लेविट (1974) ने प्रस्तावित किया था तथा रॉसके (1975) तथा बाउलिल (1976) ने परिमार्जित किया था।
इस सिद्धान्त का विवरण निम्नवत् है –
प्रकाश में (In Light):
(i) प्रकाश में स्टॉर्च लुप्त हो जाता है। सर्वप्रथम समस्त स्टॉर्च विशेषतः फॉस्फोईनोल पाइरूबिक अम्ल में परिवर्तित हो जाता है। फॉस्फोईनोल पाइरूबिक अम्ल CO2 से संयुक्त होकर ऑक्सेलोऐसीटिक अम्ल तत्पश्चात् मैलिक अम्ल बनाता है।
(ii) रक्षक कोशिकाओं में कार्बनिक अम्ल यथा मैलिक अम्ल मैलेट आयन तथा H+ में वियोजित हो जाते हैं।
(iii) H+ एपीडर्मल कोशिकाओं तथा समीपस्थ कोशिकाओं में स्थानान्तरित हो जाते हैं तथा इनके विनिमय के फलस्वरूप H + आयन रक्षक कोशिकाओं में आ जाते हैं। इस प्रक्रम को आयन विनिमय (ion-exchange) कहते हैं।
(iv) K+ आयन मैलेट ऋणायनों से सन्तुलित होते हैं। K+ आयनों के लघु सान्द्रण को उदासीन करने के लिए कुछ Cl– आयन भी म्रहण किए जाते हैं ।
(v) H+ -K +विनिमय एक सक्रिय प्रक्रम है, जिसके लिए ऊर्जा (ATP) की आवश्यकता होती है तथा ATP की आपूर्ति श्वसन या फोटोफॉस्फोरिलेशन से होती है।
(vi) रक्षक कोशिकाओं की रिक्तिका में K+ तथा मैलेट आयनों का बढ़ा सान्द्रण पर्याप्त परासरण दाब उत्पन्न करता है जिससे परिवेश की कोशिकाओं से जल अवशोषित हो सके।
(vii) जल के प्रवेश करने से रक्षक कोशिकाओं का स्फीति दाब बढ़ता है तथा रन्ध्र खुल जाते हैं।

अन्धकार में (In dark)
(i) अन्धकार में उपरन्ध्रीय गुहा में CO2 सान्द्रण बढ़ जाता है क्योंकि प्रकाश संश्लेषण की क्रिया रुक जाती है तथा श्वसन लगातार होता रहता है।
(ii) उपरन्ध्रीय गुहा में CO2 के उच्च सान्द्रण से रक्षक कोशिकाओं की जीवद्रव्य कला के आधार प्रोटॉन प्रवणता (proton gradient) का रक्षण होता है। इसके परिणामस्वरूप रक्षक कोशिकाओं में K+का सक्रिय स्थानान्तरण रुक जाता है।
(iii) रन्द्रों के बन्द होने की क्रिया में निरोधक हॉमोंन ऐब्सीसिक हॉमोंन भाग लेता है जो निम्न pH पर कार्य करता है। जैसे ही रक्षक कोशिकाओं का pH घटता है वैसे ही ऐब्सीसिक हॉमोंन रक्षक कोशिकाओं के विसरण तथा पारणम्यता को परिवर्तित करके K+प्रहण करने को रोकता है।
(iv) रक्षक कोशिकाओं में उपस्थित मैलेट आयन H+ से संयोग करके मैलिक अम्ल बनाते हैं। मैलिक अम्ल का आधिक्य PEP-कार्बोक्सिलेस की क्रियाशीलता घटाकर स्वयं के और अधिक संश्लेषण को रोकता है।
(v) इन परिवर्तनों के कारण आयनों की गति व्युक्कमित (reversed) हो जाती है, अतः रक्षक कोशिकाओं से K+आयन समीपस्थ कोशिकाओं में स्थानान्तरित हो जाते हैं।
(vi) रक्षक कोशिकाओं का परासरण दाब (OP) घट जाता है एवं जल रक्षक कोशिकाओं से परिवेश की कोशिकाओं में चला जाता है।
(vii) रक्षक कोशिकाएँ श्लथ (flaccid) हो जाती हैं तथा रन्ध्र बन्द हो जाते हैं।
प्रश्न 8.
जल अवशोषण की क्रियाविधि को समझाइए।
अथवा
जड़ों द्वारा अवशोषण का सचित्र वर्णन कीजिए।
उत्तर:
जल अवशोषण (Water Absorption):
प्राय: पादपों में जल अवशोषण मूल पर उपस्थित मूलरोमों (root hairs) द्वारा होता है किन्तु कुछ पौधों में जल का अवशोषण पत्तियों तथा तनों द्वारा भी होता है। जलोद्भिदों (hydrophytes) में जल अवशोषण प्राय: सामान्य सतह द्वारा होता है। वुड (Wood; 1925) के अनुसार कुछ पौधे, जैसे-कोचिया, रेगोडिया आदि में जल का अवशोषण वायुमण्डल से होता है।
पौधौं में जल अवशोषण ज़ड़ की सम्पूर्ण सतह से नहीं होता, अपितु मूल के सिरे (root tips) के समीप मूलरोमों द्वारा होता है। मूल के सिरों को चार प्रदेशों में बाँटा जा सकता है-
1. मूल गोप प्रदेश (Root Cap Zone) – यह मूल के सिरे पर एक आवरण के रूप में उपस्थित होता है। यह मूल के विभज्योतकी क्षेत्र (Meristematic zone) की मृदा की रगड़ से रक्षा करता है।
2. प्रविभाजी प्रदेश (Meristematic Zone)-यह मूल गोप के ठीक पीछे स्थित होता है, इसकी कोशिकाओं में विभाजन के कारण ही मूल की वृद्धि होती है।
3. दीर्घन प्रद्देश (Zone of Elongation)-इस प्रदेश की कोशिकाएँ लम्बाई में वृद्धि करती हैं।
4. मूलरोम प्रदेश (Root hair zone) – यह दीर्घन प्रदेश के ठीक पीछे का क्षेत्र होता है। इस पर अनेक एककोशिकीय मूलरोम (unicellular root hairs) पाये जाते हैं। इसी प्रदेश में मूल रोमों का सबसे अधिक जल का अवशोषण होता है। इस प्रदेश के पीछे परिपक्वन (maturation zone) प्रदेश होता है।

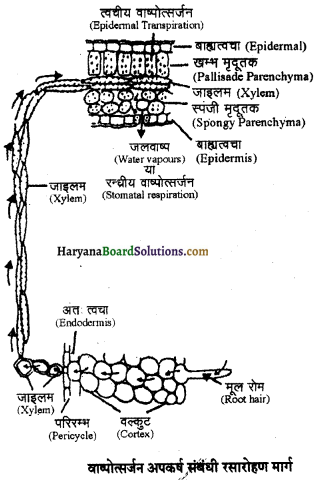
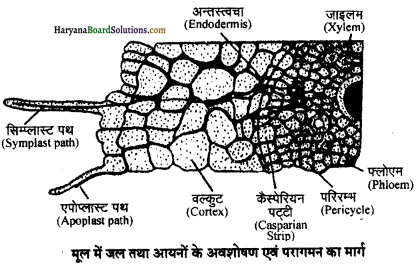
पादपों में जल का पथ (Pathway of water in Plants) – मूलरोमों द्वारा अवशोषित जल को जड़ में आन्तरिक संवहनी उतक तक पहुँचाने के लिए पौधों में निम्नलिखित दो पथ पाये जाते हैं –
1. एपोप्लास्ट पथ (Apoplast pathway) – जल मृदा से मूलरोम कोशिकाओं की कोशिका भित्तियों, वल्कुटी कोशिकाओं, (cortical cells) अन्तः़्वचा (endodermis), परिरम्भ, (pericycle) जाइलम मुदतक (xylem parenchyma) तथा जाइलम मार्गों तक पहुँचता है। चूँकि जाइलम मारों में जल पर अत्यांजक ऋणात्मक दाब होता है। अतः यह एपोप्लास्ट के मध्य से गुजरता हुआ मृदा से जल प्राप्त कर लेता है, यद्यपि अन्त:स्वचा (endodermis) की भुत्ति पूर्णतया पारगम्य नहीं होती है, क्योंकि इन पर अपारगम्य स्थूलन होता है जिन्हें कैस्पेरियन पट्टियाँ (casparian strips) कहते हैं। ये पट्टियाँ मोम सदूश सुबेरिन तथा लिग्निन युक्त होती हैं। अतः एपोप्लास्ट अन्तस्त्वचा (endodermis) तक ही क्रियाकारी होता है। अन्तस्वचा से होकर गुजरने के लिए जल को कोशिकाओं के एक किनारे से प्रविष्ट होकर दूसरे किनारे से निकलना होता है।
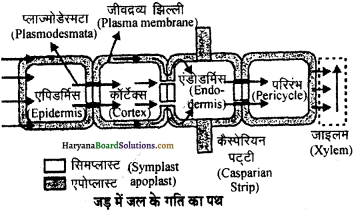
2. सिम्लास्ट पथ (Symplast Pathway) – युवा मूल रोम प्रदेश में जाइलम वाहनियाँ पूर्णkूपेण खाली नहीं होती हैं वरन् इनमें जीवित कोशिकाद्रव्य की एक पतली परत पायी जाती है। यह परत एक केन्द्रीय गुहा के चारों ओर होती है जिसमें जल भरा होता है। कोशिकाद्रव्य की यह स्तरित परत जाइलम मृदूतक, परिम्भ, अन्तस्वचा, बल्कुट तथा मूलरोम कोशिकाओं से जीवद्रव्य तन्तुओं द्वारा जुड़ी रहती है। वाष्पोत्सर्जन (transpiration) के कारण जाइलम में उत्पन्न तनाव से जल निक्रिय रूप से इन कोशिकाओं के कोशिकाद्रव्य की ओर गति करता है। कोशिकार्रव्यी प्रवाह (cytoplasmic flow) जल की गति को बढ़ाने में सहायक होता है ताकि यह प्रत्येक कोशिका से होता हुआ सुगमतापूर्वक गुजर सके। मृदा जल सिम्लास्ट में मूल रोम कोशाओं या अन्नस्वचा द्वारा प्रविष्ट होता है।
प्रश्न 9.
एक ऐसे प्रयोग का वर्णन कीजिए जिससे यह स्पष्ट किया जा सके कि वाष्पोत्सर्जन की क्रिया वातावरणीय कारकों द्वारा प्रभावित होती है. –
उत्तर:
वातावरणीय कारकों का अध्ययन (Study of environmental factors)
(i) यदि उपकरण को छायादार एवं नम स्थान पर रखा जाय तो वहाँ नमी की अधिकता के कारण वाष्तोर्सर्जन (transpiration) कम होगा और बुलबुला कम दूरी खिसकेगा।
(ii) यदि उपकरण को धूप में रखा जाय तो यहाँ वाष्पोत्सर्जन (transpiration) अधिक होता है।
(iii) यदि उपकरण को तीव वायु एवं धूप में रखा जाता है तो वाष्पोत्सर्जन (Transpiration) बहुत तीव्र होता है और बुलबुला तेजी से गति करता है।
(iv) यदि उपकरण को अन्दें स्थान पर रखते हैं तो बुलबुला बिल्कुल गति नहीं करता है। रन्ध्र की संरचना (Structure of Stomata)
रन्ध्र (Stomata) पत्ती की सतह पर पाये जाने वाले छोटे-छोटे छिद्र होते हैं। ये पत्ती के अतिरिक्त, फलों, कोमल तनों आदि वायवीय भागों पर भी पाये जाते हैं। प्रत्येक रन््ध दो वृक्काकार (kidney shaped) द्वार कोशिकाओं (guard cells) से घिरा हुआ छिद्र है। यह अत्यन्त सूक्ष्म संरचना है तथा छिद्र अण्डाकार होता है। द्वारकोशिका (guard cells) बाह्म त्वचा की अन्य कोशिकाओं से भिन्न होती हैं। इसकी बाह्य सतह पतली परन्तु भीतरी सतह मोटी होती है। कभी-कभी द्वार कोशिकाओं के बाहर सहायक कोशिकाएँ (subsidiary cells) भी मिलती हैं। जब द्वार कोशिकाएँ स्फीत (turgid) होती हैं तो छिद्र खुला होता है तथा इनकी श्लथ (flaccid) अवस्था में ये बन्द होते हैं।
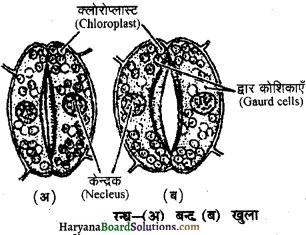
द्वार कोशिकाओं में केन्द्रक तथा क्लोरोप्लास्ट (chloroplast) पाए जाते हैं। द्वार कोशिकाओं में केन्द्रक तथा क्लोरोप्लास्ट मीसोफिल के क्लोरोप्लास्ट से भिन्न होता है। इसमें दोनों प्रकाशीय तंत्र PSI तथा PSII तन्त मिलते हैं। अतः फोटोफास्पोरिलेशन (photophosphorylation) की क्रिया प्रकाश में पूर्ण होती है परन्तु रिबुलोज डाइफास्फेट कार्बोंक्सिलेज एन्जाइम (ribulose biphosphate carboxylase enzyme) के न मिलने से भोजन नहीं बनता है। आसपास की कोशिकाओं से मिलने वाली शर्करा मण्ड (starch) में बदलती है। रात के समय मण्ड (starch) की मात्रा अधिक होने से रन्ध्र (stomata) बन्द हो जाते हैं तथा दिन में मण्ड के शर्करा में बदलने से ये खुल जाते हैं।
![]()


![]()
![]()







![]()
![]()

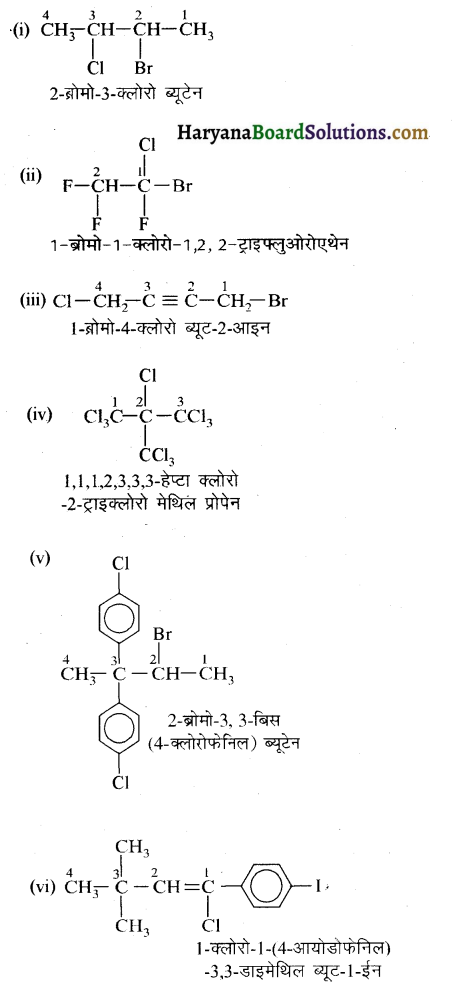
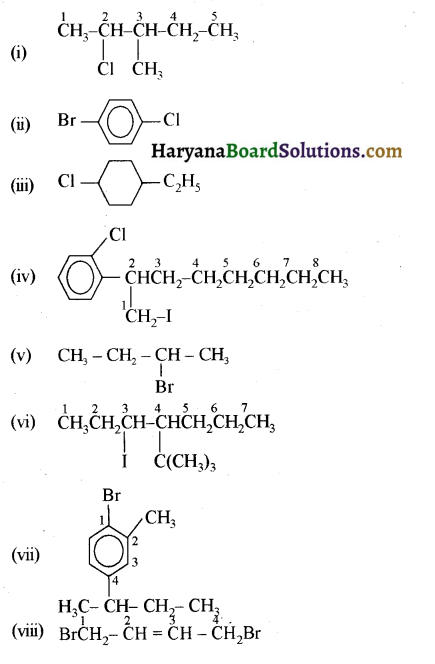
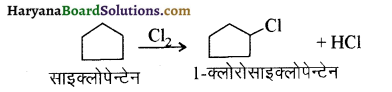
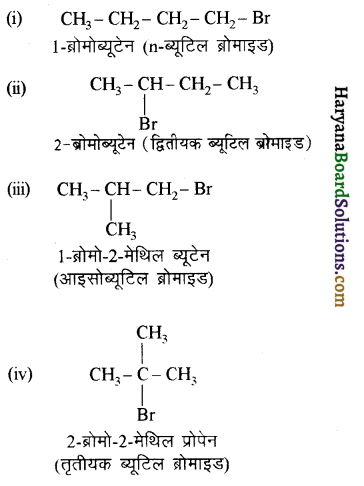
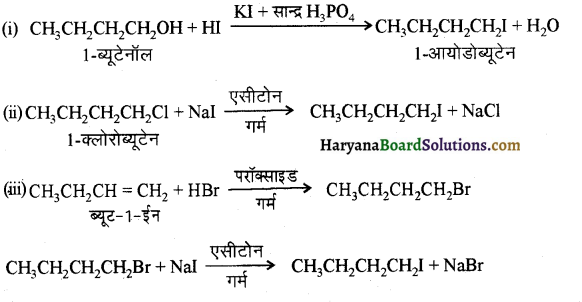
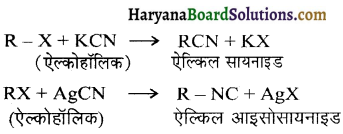
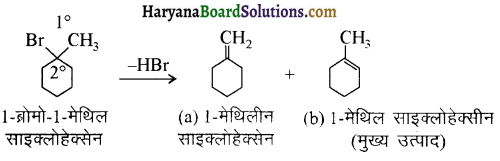
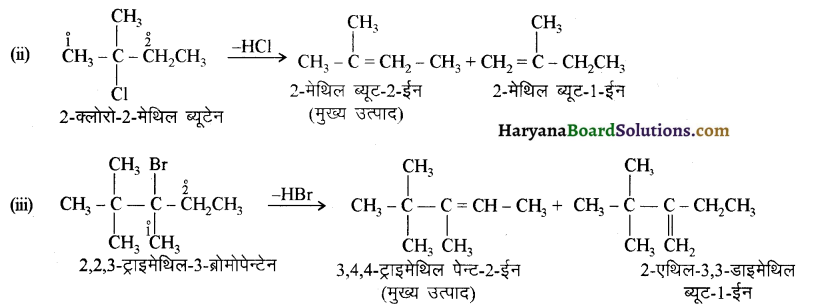
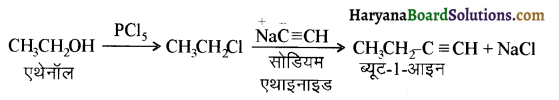
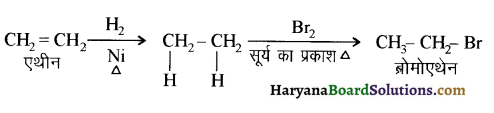

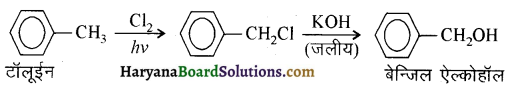
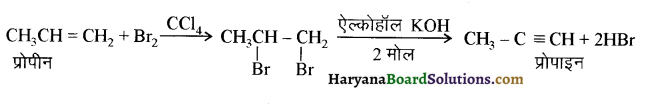
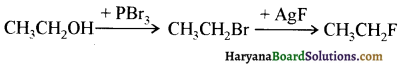
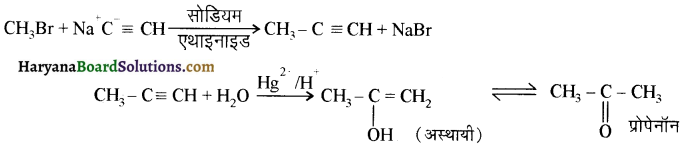
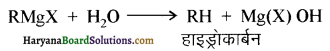
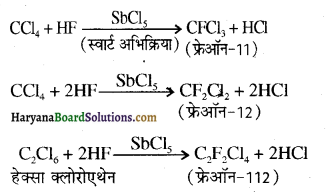
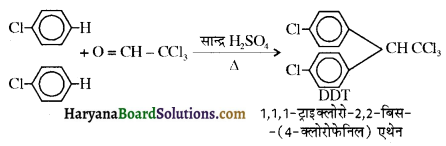
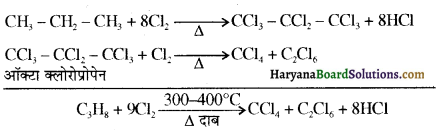
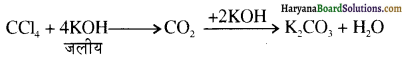
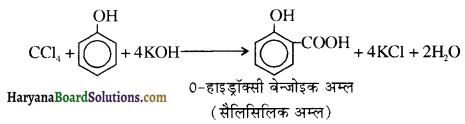
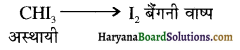
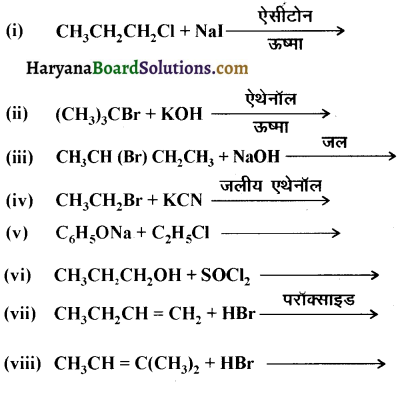
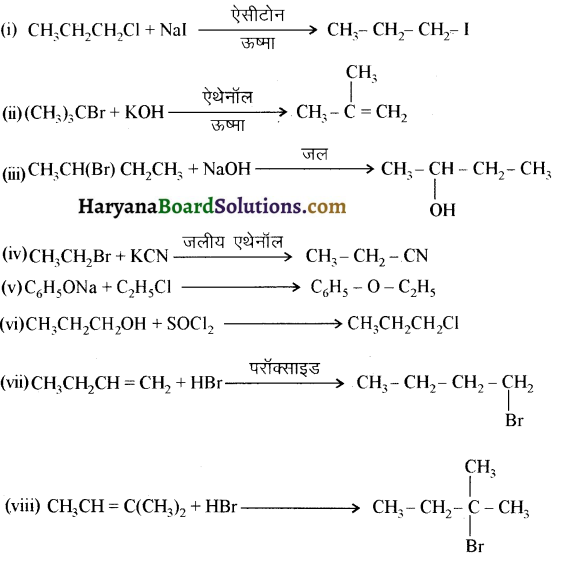


 में से
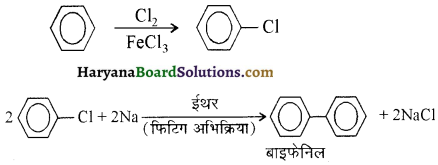
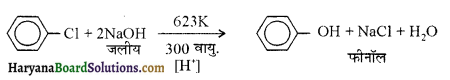
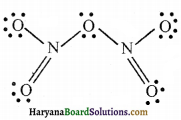
में से  का जलीय KOH से शीघ्रता से जल अपघटन होगा क्योंकि इसके जल अपघटन में बनने वाला मध्यवर्ती कार्बधनायन अधिक स्थायी होता है, क्योंकि इसमें दो बेन्जीन वलय के कारण अनुनाद अधिक होगा जबकि C6H5CH2Cl से बने कार्बधनायन में केवल एक बेन्जीनवलय ही अनुनाद में भाग लेती है।
का जलीय KOH से शीघ्रता से जल अपघटन होगा क्योंकि इसके जल अपघटन में बनने वाला मध्यवर्ती कार्बधनायन अधिक स्थायी होता है, क्योंकि इसमें दो बेन्जीन वलय के कारण अनुनाद अधिक होगा जबकि C6H5CH2Cl से बने कार्बधनायन में केवल एक बेन्जीनवलय ही अनुनाद में भाग लेती है।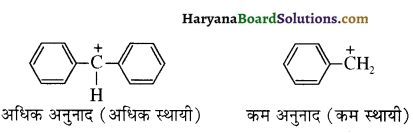
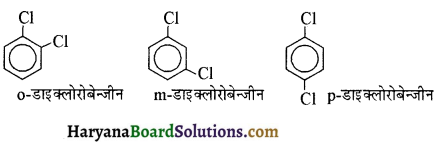
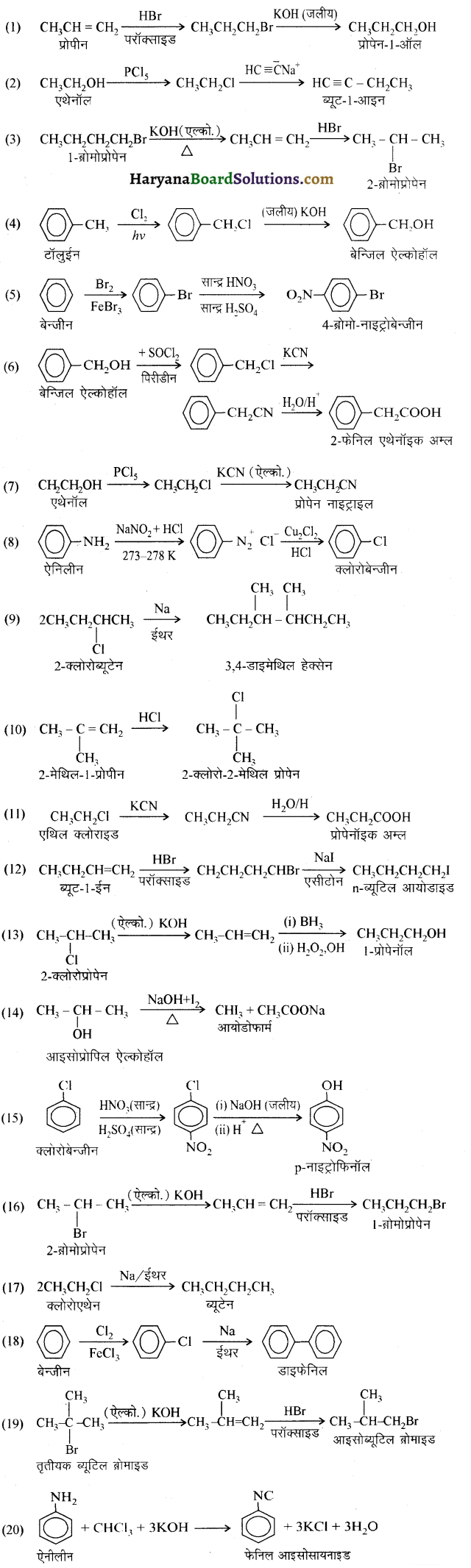
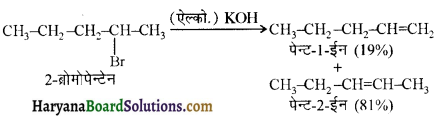
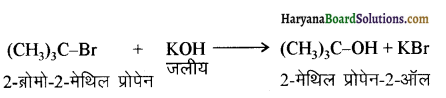
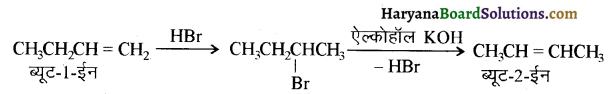
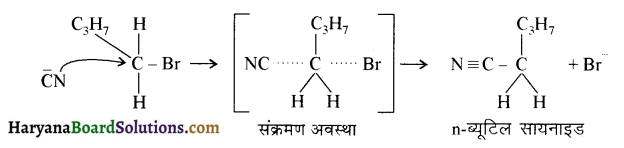
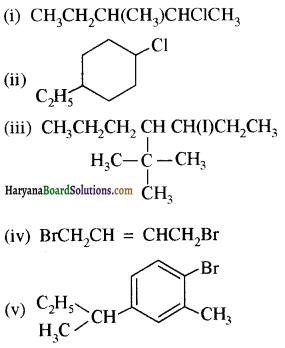
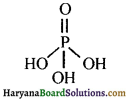
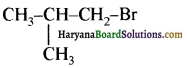 (आइसोब्यूटिल ब्रोमाइड)। प्रश्नानुसार, यौगिक ‘क’ n – ब्यूटिल ब्रोमाइड नहीं है अतः यह आइसोब्यूटिल ब्रोमाइड होगा।
(आइसोब्यूटिल ब्रोमाइड)। प्रश्नानुसार, यौगिक ‘क’ n – ब्यूटिल ब्रोमाइड नहीं है अतः यह आइसोब्यूटिल ब्रोमाइड होगा।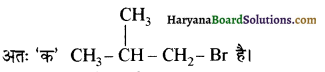

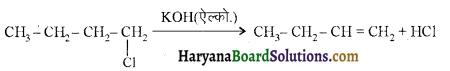
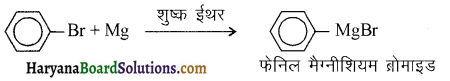


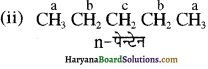

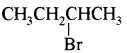
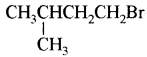




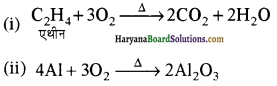
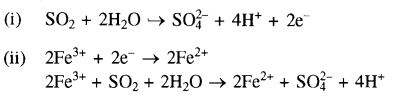

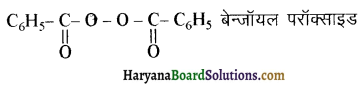
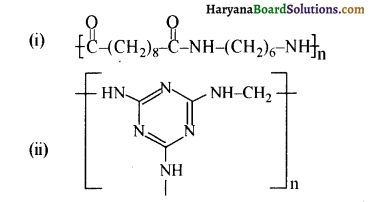
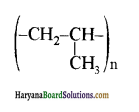 का बनना संकलन बहुलकन है जबकि हैक्सा मेथिलीन डाइऐमीन (NH2-(CH2)6NH2) तथा ऐडिपिक अम्ल (HOOC- (CH2)4COOH) के बहुलकन से नाइलॉन 6,6 का बनना संघनन बहुलकन है। इसमें H2O का विलोपन होता है।
का बनना संकलन बहुलकन है जबकि हैक्सा मेथिलीन डाइऐमीन (NH2-(CH2)6NH2) तथा ऐडिपिक अम्ल (HOOC- (CH2)4COOH) के बहुलकन से नाइलॉन 6,6 का बनना संघनन बहुलकन है। इसमें H2O का विलोपन होता है।
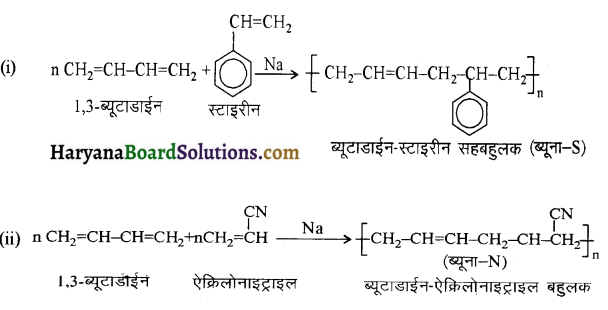
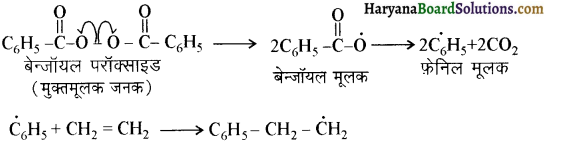
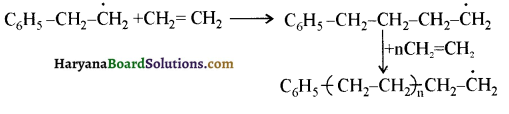
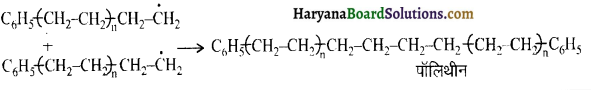
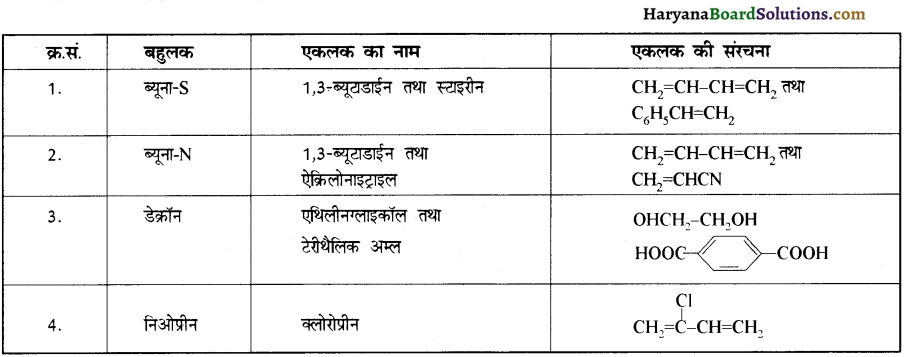
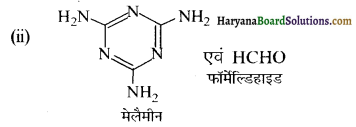
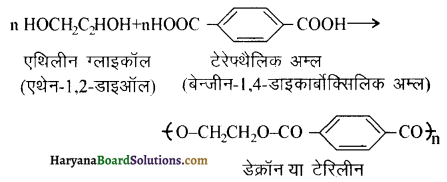
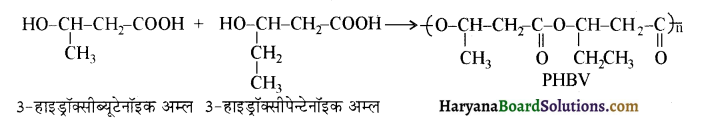
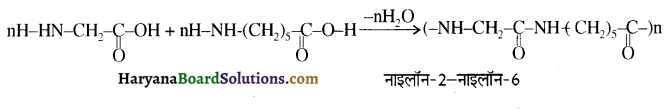
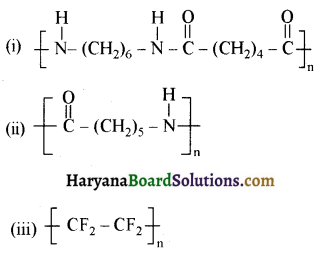
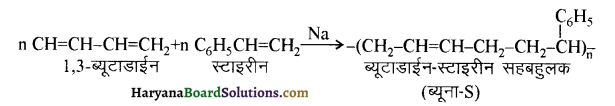
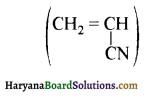 का सहबहुलक है जबकि ब्यूना-S, 1,3-ब्यूटाडाईन तथा स्टाइरीन
का सहबहुलक है जबकि ब्यूना-S, 1,3-ब्यूटाडाईन तथा स्टाइरीन 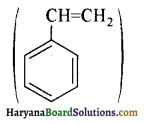 का सहबहुलक है।
का सहबहुलक है।

















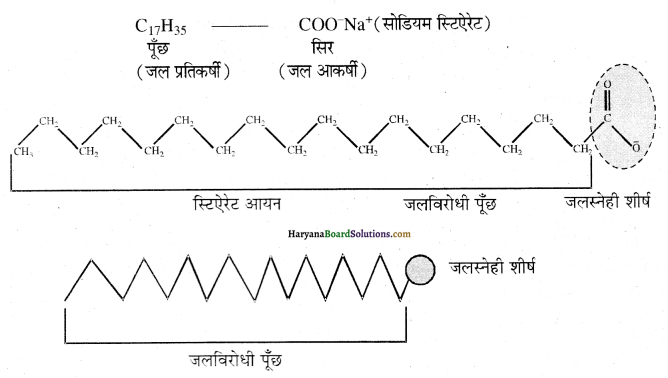
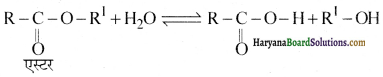



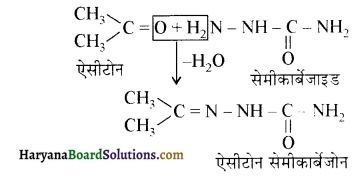
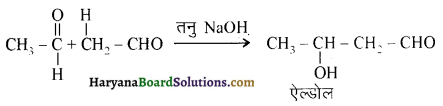
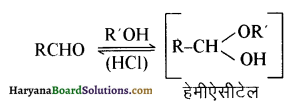
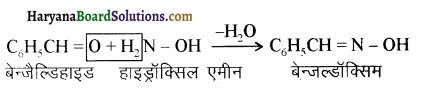
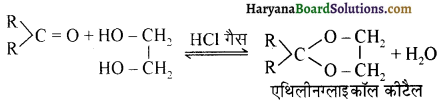
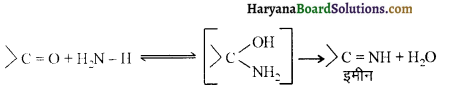
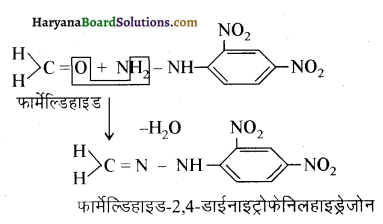
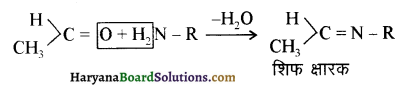
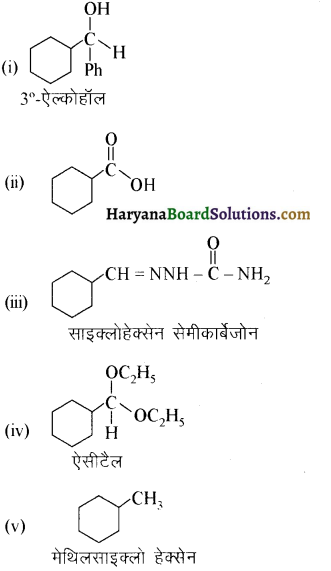
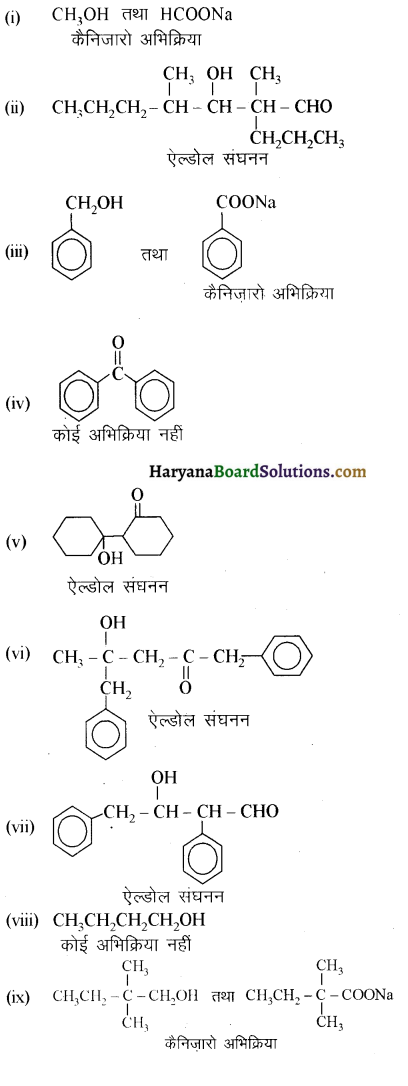
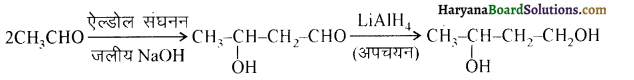
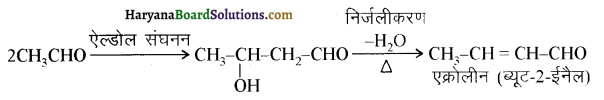

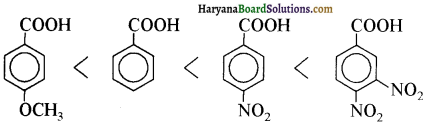
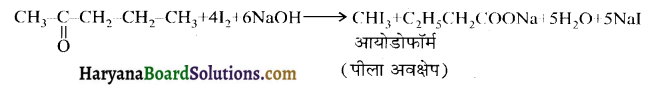
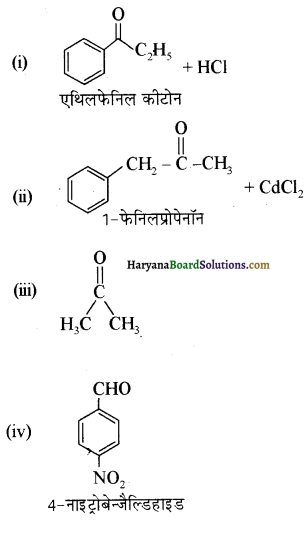
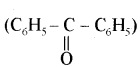 यह परीक्षण नहीं देता।
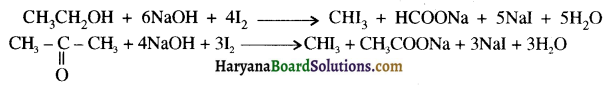
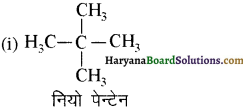
यह परीक्षण नहीं देता। एक मैथिल कीटोन है अतः यह आयोडोफॉर्म परीक्षण देता है जबकि पेन्टेन 3 ऑन
एक मैथिल कीटोन है अतः यह आयोडोफॉर्म परीक्षण देता है जबकि पेन्टेन 3 ऑन 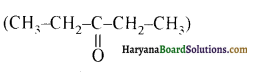 में यह परीक्षण नहीं होता।
में यह परीक्षण नहीं होता। एक मैथिल कीटोन है अतः ऐसीटोफ़ीनॉन, आयोडोफॉर्म परीक्षण देता है जबकि बेन्जेल्डिहाइड यह परीक्षण नहीं देता है।
एक मैथिल कीटोन है अतः ऐसीटोफ़ीनॉन, आयोडोफॉर्म परीक्षण देता है जबकि बेन्जेल्डिहाइड यह परीक्षण नहीं देता है।
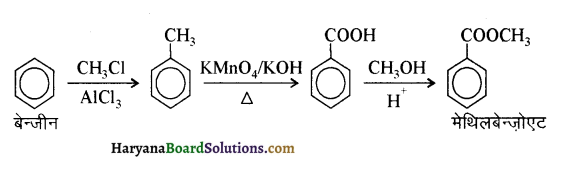
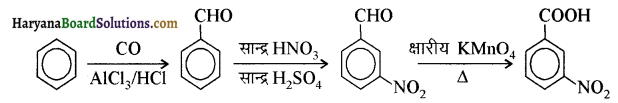
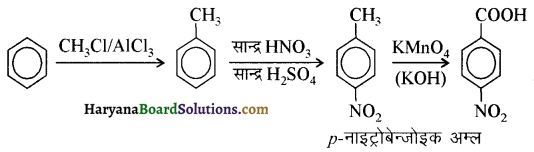
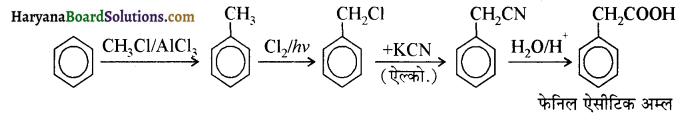
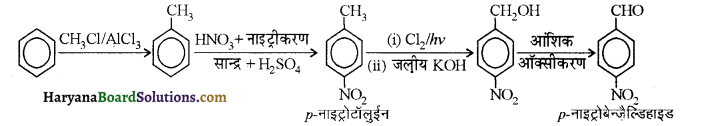
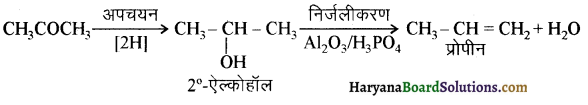
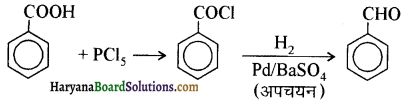

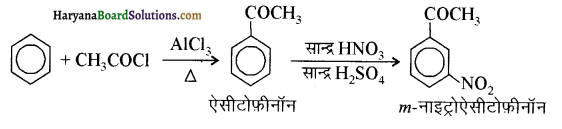
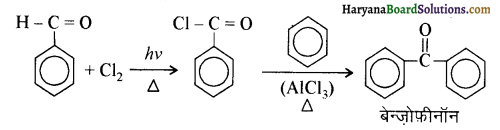
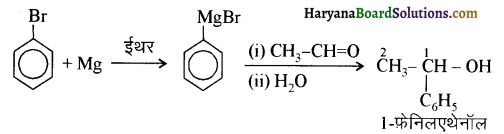

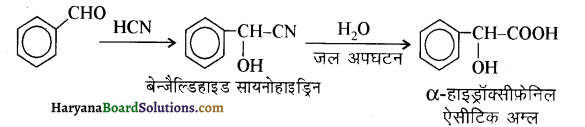
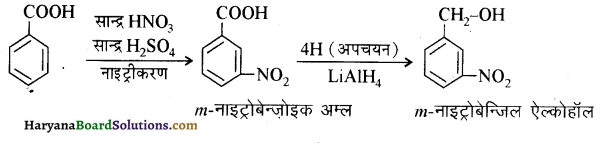

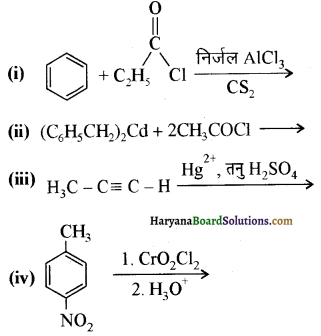
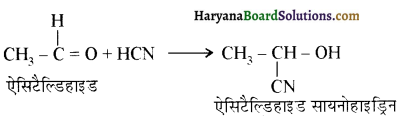
 आ जाता है। इसे ऐसीटिलन अभिक्रिया कहते हैं।
आ जाता है। इसे ऐसीटिलन अभिक्रिया कहते हैं।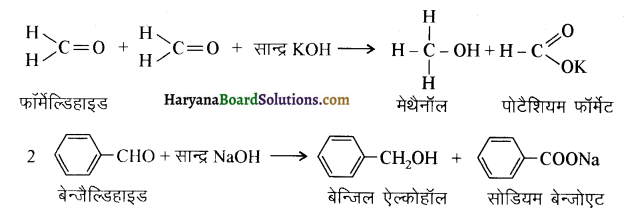
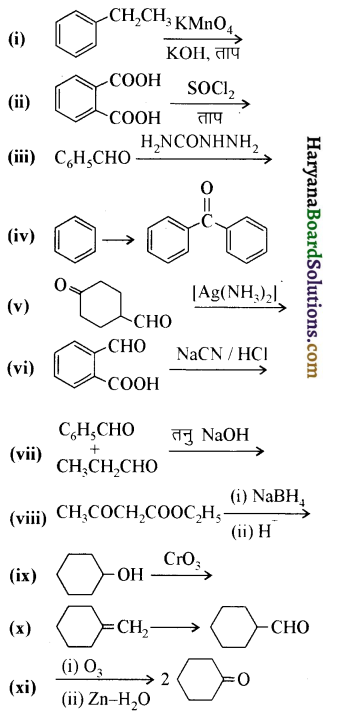
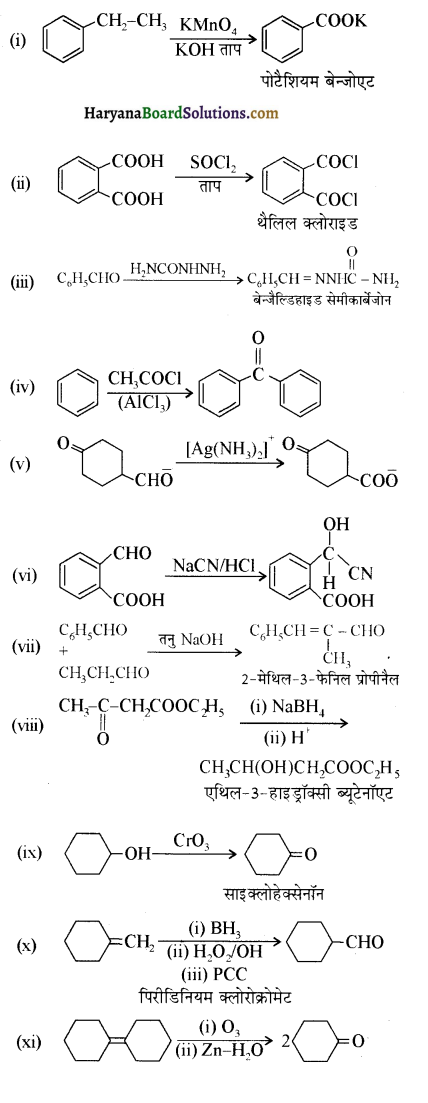

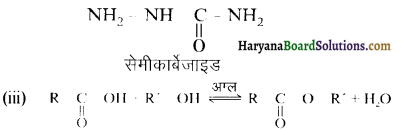
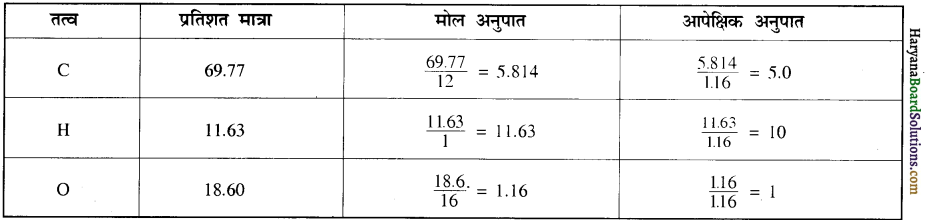
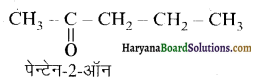 होगा ।
होगा ।