Haryana State Board HBSE 9th Class Science Important Questions Chapter 3 परमाणु एवं अणु Important Questions and Answers.
Haryana Board 9th Class Science Important Questions Chapter 3 परमाणु एवं अणु
अति लघूत्तरात्मक प्रश्न
प्रश्न 1.
आंतवाँ लॉरेन लवोइजिए (Antonie L. Lavoisier) वैज्ञानिक ने रसायन विज्ञान को आधार प्रदान करने वाले किन दो नियमों को स्थापित किया?
उत्तर:
- द्रव्यमान संरक्षण का नियम।
- स्थिर अनुपात का नियम।
प्रश्न 2.
द्रव्यमान का संरक्षण नियम क्या है?
उत्तर:
द्रव्यमान के संरक्षण नियम के अनुसार रासायनिक अभिक्रिया में द्रव्यमान का न सृजन होता है और न ही विनाश।
प्रश्न 3.
निश्चित (स्थिर) अनुपात का नियम क्या है?
उत्तर:
निश्चित (स्थिर) अनुपात के नियमानुसार शुद्ध रासायनिक पदार्थ में तत्त्व हमेशा द्रव्यमान के निश्चित अनुपात में विद्यमान होते हैं।
प्रश्न 4.
अमोनिया (NH3) में द्रव्यमान के अनुसार नाइट्रोजन और हाइड्रोजन में क्या अनुपात है?
उत्तर:
अमोनिया में द्रव्यमान के अनुसार नाइट्रोजन व हाइड्रोजन का अनुपात 14 : 3 है।
प्रश्न 5.
जल (H2O) में द्रव्यमान के अनुसार हाइड्रोजन और ऑक्सीजन में क्या अनुपात होता है?
उत्तर:
जल में द्रव्यमान के अनुसार हाइड्रोजन और ऑक्सीजन में 1 : 8 का अनुपात होता है।
प्रश्न 6.
परमाणु (Atom) किसे कहते हैं?
उत्तर:
परमाणु किसी तत्त्व का वह सूक्ष्मतम कण है जिसमें उस तत्त्व के सभी रासायनिक गुणधर्म विद्यमान होते हैं और वह उन गुणधर्मों को बनाए भी रखता है।
![]()
प्रश्न 7.
जॉन डाल्टन ने पदार्थ की प्रकृति के बारे में क्या सिद्धांत दिया?
उत्तर:
उनके अनुसार सभी पदार्थ चाहे तत्त्व, यौगिक या मिश्रण हों सूक्ष्मकणों से बने होते हैं, जिन्हें परमाणु कहते हैं।
प्रश्न 8.
परमाणु के मूल कण कौन-कौन से हैं?
उत्तर:
परमाणु के मूल कण प्रोटॉन, न्यूट्रॉन तथा इलेक्ट्रॉन हैं।
प्रश्न 9.
परमाणुओं के फोटोग्राफ लेने के लिए किस सूक्ष्मदर्शी का उपयोग किया जाता है?
उत्तर:
स्केनिंग टनैलिंग सूक्ष्मदर्शी (Scanning Tunneling Microscope-STM)।
प्रश्न 10.
अणु किसे कहते हैं?
उत्तर:
अणु किसी तत्त्व या यौगिक का वह सूक्ष्मतम कण है जिसका सामान्य अवस्था में अकेला या स्वतंत्र अस्तित्व होता है और वह इस पदार्थ (तत्त्व या यौगिक) के सभी गुणों को दर्शाता है।
प्रश्न 11.
किन्हीं दो एक-परमाणुक अणुओं के नाम व प्रतीक लिखो।
उत्तर:
ऑर्गन (Ar) तथा हीलियम (He)।
प्रश्न 12.
दो द्वि-परमाणुक तथा दो त्रि-परमाणुक अणुओं के सूत्र लिखो।
उत्तर:
- द्वि-परमाणुक अणु-H2, N2, HCl
- त्रि-परमाणुक अणु-H2O, CO2
प्रश्न 13.
बहु-परमाणुक अणु से क्या अभिप्राय है?
उत्तर:
जिस अणु में चार से अधिक परमाणु होते हैं, वह अणु बहु-परमाणुक कहलाता है; जैसे S8 तथा C2H5OH
प्रश्न 14.
किसी पदार्थ का अणुसूत्र हमें क्या जानकारी देता है?
उत्तर:
किसी पदार्थ का अणुसूत्र हमें बताता है कि प्रत्येक प्रकार के कितने परमाणु उसके एक अणु में विद्यमान हैं।
प्रश्न 15.
नेनोमीटर और मीटर में क्या संबंध होता है?
उत्तर:
1 नेनोमीटर (nm) = 10-9 मीटर होती है।
प्रश्न 16.
परमाणु की त्रिज्या को किस इकाई में मापा जाता है?
उत्तर:
परमाणु की त्रिज्या को नेनोमीटर (nm) इकाई में मापा जाता है।
प्रश्न 17.
हाइड्रोजन परमाणु की त्रिज्या कितनी होती है?
उत्तर:
हाइड्रोजन परमाणु की त्रिज्या 10-10 मीटर होती है।
प्रश्न 18.
IUPAC का क्या अर्थ है?
उत्तर:
IUPAC का अर्थ है- इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड केमिस्ट्री।
प्रश्न 19.
लोहे का प्रतीक क्या है तथा यह कहाँ से व्युत्पन्न हुआ?
उत्तर:
लोहे का प्रतीक Fe है जो इसके लैटिन नाम फेरम से व्युत्पन्न हुआ।
प्रश्न 20.
सोडियम तथा पोटैशियम का प्रतीक किन-किन लैटिन नामों से व्युत्पन्न हुआ?
उत्तर:
सोडियम (Na) तथा पोटैशियम (K) का प्रतीक क्रमशः नैट्रियम एवं केलियम से व्युत्पन्न हुए हैं।
प्रश्न 21.
N2 एवं 2N में क्या अंतर है?
उत्तर:
N2 नाइट्रोजन का एक अणु है जबकि 2N नाइट्रोजन के दो परमाणु हैं।
प्रश्न 22.
संरचना सूत्र से क्या अभिप्राय है?
उत्तर:
संरचना सूत्र एक रासायनिक सूत्र है जो दर्शाता है कि अणु में परमाणु एक-दूसरे से किस प्रकार आबंधित होते हैं।
प्रश्न 23.
जल का संरचना सूत्र क्या है?
उत्तर:
जल का संरचना सूत्र H-O-H है।
प्रश्न 24.
कार्बन मोनोक्साइड का सूत्र क्या है?
उत्तर:
कार्बन मोनोक्साइड का सूत्र CO है।
प्रश्न 25.
परमाणु द्रव्यमान इकाई को परिभाषित करें।
उत्तर:
परमाणु द्रव्यमान इकाई को कार्बन के विशिष्ट समस्थानिक (C-12) के एक परमाणु के द्रव्यमान के \(\frac { 1 }{ 2 }\) भाग के रूप में परिभाषित किया जाता है।
प्रश्न 26.
अणु द्रव्यमान से क्या अभिप्राय है?
उत्तर:
किसी पदार्थ का अणु द्रव्यमान उस पदार्थ के एक अणु में विद्यमान सभी परमाणुओं के परमाणु द्रव्यमानों का कुल योग होता है।
प्रश्न 27.
सूत्र द्रव्यमान से क्या अभिप्राय है?
उत्तर:
किसी पदार्थ का सूत्र द्रव्यमान उस यौगिक के सूत्र इकाई में विद्यमान सभी परमाणुओं के परमाणु द्रव्यमानों का कुल योग होता है, चाहे वह अणु है या नहीं।
प्रश्न 28.
CH3OH का अणु द्रव्यमान कितना है?
उत्तर:
CH3OH का अणु द्रव्यमान = (12 + 3 x 1 + 16 + 1)u
= (12 + 3 + 16 + 1)u
= 32u
![]()
प्रश्न 29.
परमाणुओं और अणुओं की गणक इकाई क्या है?
उत्तर:
परमाणुओं और अणुओं की गणक इकाई मोल (mole) है।
प्रश्न 30.
अणु किन सूक्ष्मकणों से मिलकर बनते हैं?
उत्तर:
परमाणुओं से।
प्रश्न 31.
परमाणु के विषय में कब और किसने जानकारी दी?
उत्तर:
सन् 1808 में जॉन डाल्टन ने।
प्रश्न 32.
किसी तत्त्व को संक्षिप्त रूप में लिखना क्या कहलाता है?
उत्तर:
प्रतीक।
प्रश्न 33.
कॉपर का प्रतीक क्या है?
उत्तर:
Cu
प्रश्न 34.
ऐलुमिनियम का प्रतीक क्या है?
उत्तर:
AI
प्रश्न 35.
सोने व चाँदी के प्रतीक लिखें।
उत्तर:
सोना = Au व चाँदी = Ag
प्रश्न 36.
रासायनिक सूत्र से क्या अभिप्राय है?
उत्तर:
किसी यौगिक के अणु की रचना को रासायनिक प्रतीकों द्वारा प्रकट करने को रासायनिक सूत्र कहते हैं।
प्रश्न 37.
परमाणुकता से क्या अभिप्राय है?
उत्तर:
किसी तत्त्व के एक अणु में उपस्थित परमाणुओं की संख्या उसकी परमाणुकता कहलाती है।
प्रश्न 38.
उत्कृष्ट गैसों की परमाणुकता क्या होती है?
उत्तर:
एक।
प्रश्न 39.
तीन परमाणुकता वाले एक अणु का नाम लिखें।
उत्तर:
ओज़ोन (O3)।
प्रश्न 40.
दो परमाणु वाले अणु क्या कहलाते हैं?
उत्तर:
द्वि-परमाणुक।
प्रश्न 41.
फास्फोरस एवं सल्फर की परमाणुकता कितनी है?
उत्तर:
फास्फोरस की परमाणुकता चार तथा सल्फर की परमाणुकता आठ है।
प्रश्न 42.
कॉपर क्लोराइड का रासायनिक सूत्र लिखें।
उत्तर:
CuCl2
प्रश्न 43.
रासायनिक समीकरण से क्या अभिप्राय है?
उत्तर:
किसी रासायनिक अभिक्रिया का प्रतीकात्मक निरूपण रासायनिक समीकरण कहलाता है।
प्रश्न 44.
मोल क्या है?
उत्तर:
मोल पदार्थ की वह मात्रा है जिसमें C-12 के 12 ग्राम में परमाणुओं की संख्या के बराबर के कण (परमाणु, अणु अथवा आयन) होते हैं।
प्रश्न 45.
आवोगाद्रो स्थिरांक (Avogadro’s Constant) क्या है?
उत्तर:
आवोगाद्रो स्थिरांक (6.022 x 1023 mol-1) को 12C के 12 ग्राम में उपस्थित परमाणुओं की संख्या द्वारा परिभाषित किया है।
प्रश्न 46.
मोलर द्रव्यमान को परिभाषित करें।
उत्तर:
पदार्थ के एक मोल अणुओं का द्रव्यमान इसका मोलर द्रव्यमान कहलाता है।
प्रश्न 47.
मोलर द्रव्यमान का प्रतीक व इकाई क्या है?
उत्तर:
मोलर द्रव्यमान का प्रतीक : M व इकाई : ग्राम प्रति मोल (g/mol)
प्रश्न 48.
जल व ऑक्सीजन का मोलर द्रव्यमान लिखें।
उत्तर:
M(H2O) = 18 g/mol व M (O2) = 32 g/mol
प्रश्न 49.
आवेशित कणों को क्या कहते हैं?
उत्तर:
आवेशित कणों को आयन कहते हैं।
प्रश्न 50.
ऋणायन तथा धनायन से क्या अभिप्राय है?
उत्तर:
ऋण आवेशित कणों को ऋणायन तथा धन आवेशित कणों को धनायन कहते हैं।
प्रश्न 51.
आयन किसे कहते हैं? उदाहरण सहित लिखिए।
उत्तर:
धातु एवं अधातु युक्त यौगिक आवेशित कणों से बने होते हैं। इन आवेशित कणों को आयन कहते हैं; जैसे सोडियम, मैग्नीशियम।
लघूत्तरात्मक प्रश्न
प्रश्न 1.
पदार्थ की प्रकृति के बारे में जॉन डाल्टन द्वारा दिए गए सिद्धांत की विवेचना कीजिए।
उत्तर:
जॉन डाल्टन द्वारा पदार्थ की प्रकृति के बारे में दिया गया मूल सिद्धांत कहता है कि सभी पदार्थ चाहे तत्त्व, यौगिक या मिश्रण हों सूक्ष्मकणों से बने होते हैं जिन्हें परमाणु कहते हैं। इसकी विवेचना अग्रलिखित प्रकार से की जा सकती है-
- तत्त्व अति सूक्ष्म अविभाज्य कणों से मिलकर बनता है, जिन्हें परमाणु कहते हैं।
- दिए गए तत्त्व के सभी परमाणु द्रव्यमान और गुणधर्म दोनों में समान होते हैं। विभिन्न तत्त्वों के परमाणुओं के विभिन्न द्रव्यमान और गुणधर्म होते हैं।
- किसी तत्त्व के परमाणुओं का सृजन या विनाश दूसरे तत्त्व के परमाणुओं में रूपांतरण नहीं हो सकता है।
- जब विभिन्न तत्त्वों के परमाणु आपस में छोटी पूर्ण संख्या अनुपात में संयोग करते हैं तो यौगिक बनते हैं।
- दिए गए यौगिक में परमाणुओं की आपेक्षिक संख्या और प्रकार निश्चित रहते हैं।
संक्षेप में, परमाणु किसी तत्त्व का सूक्ष्मतम कण है जो सभी रासायनिक और भौतिक परिवर्तनों में अपनी रासायनिक पहचान .. ‘ बनाए रखता है। एक तत्त्व के परमाणु दूसरे तत्त्व के परमाणुओं से अलग होते हैं।
प्रश्न 2.
परमाणु के बारे में आधुनिक मत डॉल्टन के सिद्धांत से किस प्रकार भिन्न है?
उत्तर:
डॉल्टन के मतानुसार, परमाणु पदार्थ का अति सूक्ष्म अविभाज्य कण है तथा परमाणु को न तो उत्पन्न किया जा सकता है और न ही नष्ट किया जा सकता है, परंतु आधुनिक मतानुसार परमाणु को अधिक सूक्ष्मकणों-इलेक्ट्रॉन, प्रोटॉन व न्यूट्रॉन में तोड़ा जा सकता है। आजकल परमाणु के नाभिक के विखंडन से परमाणु बम भी बनाया जाता है जो परमाणु की अविनाशिता के नियम से भिन्नता प्रकट करता है।
प्रश्न 3.
डॉल्टन के परमाणु सिद्धांत में क्या-क्या त्रुटियाँ थीं? उदाहरण द्वारा स्पष्ट करें।
उत्तर:
डॉल्टन का परमाणु सिद्धांत कुछ तथ्यों की व्याख्या नहीं कर सका, जो निम्नलिखित हैं-
(1) हीरा तथा ग्रेफाइट एक ही तत्त्व के बने हैं, तब भी इनके गुणों में इतनी विभिन्नता क्यों है? हीरा प्रकृति में प्राप्त सबसे कठोर तथा चमकदार है तथा ग्रेफाइट मुलायम तथा काले रंग का है।
(2) डॉल्टन के परमाणु सिद्धांत के अनुसार परमाणु अविभाजित कण है, परन्तु आधुनिक खोजों के अनुसार परमाणु प्रोटॉन, इलेक्ट्रॉन तथा न्यूट्रॉन से मिलकर बना है।
(3) एक ही तत्त्व के दो परमाणुओं का द्रव्यमान अलग-अलग भी होता है; जैसे यूरेनियम के दो समस्थानिक होते हैं \({ }_{92} \mathrm{U}^{235}\) तथा \({ }_{92} \mathrm{U}^{238}\) जिनका परमाणु द्रव्यमान क्रमशः 235u तथा 238u होता है।
प्रश्न 4.
व्याख्या कीजिए कि परमाणु अविभाज्य न होकर भाज्य हैं।
उत्तर:
विस्तृत अध्ययन से यह प्रमाणित हो चुका है कि कुछ तत्त्वों के परमाणु विकिरणें उत्सर्जित करते हैं जो कागज़ जैसे कई पदार्थों में से गुज़र सकती हैं। परमाणुओं में से विकिरण अथवा कणों का उत्सर्जित होना यह सिद्ध करता है कि परमाणु अविभाज्य न होकर भाज्य हैं।
प्रश्न 5.
परमाणु कितने बड़े होते हैं?
उत्तर:
परमाणु बहुत छोटे होते हैं। ये किसी भी वस्तु, जिसकी हम कल्पना या तुलना कर सकते हैं, से भी छोटे होते हैं। लाखों परमाणुओं को जब एक के ऊपर एक चट्टे के रूप में रखें, तो बड़ी कठिनाई से कागज की एक शीट जितनी मोटी परत बन पाएगी।
परमाणु त्रिज्या को नेनोमीटर (nm) में मापा जाता है। 10-9m = 1nm.
![]()
प्रश्न 6.
निम्नलिखित पदार्थों की त्रिज्या मीटरों में प्रदर्शित करें।
(1) हाइड्रोजन परमाणु
(2) जल अणु
(3) हीमोग्लोबिन अणु
(4) रेत कण।
उत्तर:
| पदार्थ का नाम | त्रिज्या (मीटर में) |
| (1) हाइड्रोजन परमाणु | 10-10 |
| (2) जल अणु | 10-9 |
| (3) हीमोग्लोबिन अणु | 10-8 |
| (4) रेत कण | 10-4 |
प्रश्न 7.
रिक्त स्थान भरिए-
(1) तत्त्व केवल एक ही प्रकार के ………………… से मिलकर बना होता है।
(2) हाइड्रोजन के अणु में हाइड्रोजन के ………………… परमाणु होते हैं।
(3) यौगिक कम-से-कम ………………… तत्त्वों के संयोग से बनता है।
उत्तर:
(1) परमाणुओं
(2) दो
(3) दो।
प्रश्न 8.
निम्नलिखित तत्त्वों के प्रतीक लिखिए-
ऐलुमिनियम, कैल्शियम, कोबाल्ट, आयोडीन एवं मर्करी।
उत्तर:
| तत्त | प्रतीक |
| 1. ऐलुमिनियम | Al |
| 2. कैल्शियम | Ca |
| 3. कोबाल्ट | Co |
| 4. आयोडीन | I |
| 5. मर्करी | Hg |
प्रश्न 9.
निम्नलिखित प्रतीक किन तत्त्वों के हैं?
Na, K, P, Pb, Ca, Zn, Br और Sn
उत्तर:
| प्रतीक | तत्त्व |
| 1. Na | सोडियम |
| 2. K | पोटैशियम |
| 3. P | फॉस्फोरस |
| 4. Pb | लेड (सीसा) |
| 5. Ca | कैल्शियम |
| 6. Zn | जिंक (जस्त) |
| 7. Br | ब्रोमीन |
| 8. Sn | टिन |
प्रश्न 10.
कॉलम A में दिए गए वक्तव्यों को कॉलम B में दिए गए प्रतीकों से संबंध स्थापित कीजिए-
| कॉलम A | कॉलम B |
| (1) नाइट्रोजन का एक अणु | Na |
| (2) किसी यौगिक का एक अणु | N |
| (3) किसी धातु का एक परमाणु | N2 |
| (4) नाइट्रोजन का एक परमाणु | NH3 |
उत्तर:
| कॉलम A | कॉलम B |
| (1) नाइट्रोजन का एक अणु | N2 |
| (2) किसी यौगिक का एक अणु | NH3 |
| (3) किसी धातु का एक परमाणु | Na |
| (4) नाइट्रोजन का एक परमाणु | N |
प्रश्न 11.
लैटिन नामों पर आधारित कुछ तत्त्वों के नाम व प्रतीक लिखें।
उत्तर:
लैटिन नामों पर आधारित कुछ तत्त्वों के नाम व प्रतीक निम्नलिखित हैं-
| तत्त्व | लैटिन नाम | प्रतीक |
| सोडियम | नैट्रियम | Na |
| कॉपर | साइप्रस | Cu |
| आयरन | फेरम | Fe |
| पोटैशियम | केलियम | K |
| सिल्वर | अर्जेंटम | Ag |
| टिन | स्टेनम | Sn |
| गोल्ड | ऑरम | Au |
| मर्करी | हाइड्रेरजिरम | Hg |
| लेड | प्लॅमूब्ब | Pb |
प्रश्न 12.
निम्नलिखित यौगिकों में उपस्थित तत्त्वों के नाम लिखिए-
बिना बुझा हुआ चूना (CaO), सल्फर डाइऑक्साइड (SO2), पोटैशियम नाइट्रेट (KNO3), मरक्यूरिक ऑक्साइड (HgO) तथा बोरेक्स (Na2B4O7)।
उत्तर:
दिए गए यौगिकों में उपस्थित तत्त्वों के नाम निम्नलिखित सारणी में दर्शाए गए हैं-
| यौगिक | उपस्थित तत्त्व |
| 1. बिना बुझा हुआ चूना CaO | कैल्शियम (Ca) ऑक्सीजन (O) |
| 2. सल्फर डाइऑक्साइड (SO2) | सल्फर (S); ऑक्सीजन (O) |
| 3. पोटैशियम नाइट्रेट (KNO3) | पोटैशियम (K); नाइट्रोजन (N); ऑक्सीजन (O) |
| 4. मरक्यूरिक ऑक्साइड (HgO) | मर्करी (Hg); ऑक्सीजन (O) |
| 5. बोरेक्स (Na2B4O7) | सोडियम (Na); बोरॉन (B); ऑक्सीजन (O) |
प्रश्न 13.
ऑक्सीजन परमाणु के द्रव्यमान 1/16 के भाग को इकाई के रूप में क्यों नहीं लिया जाता है?
उत्तर:
ऑक्सीजन परमाणु के द्रव्यमान के 1/16 भाग को इकाई के रूप में नहीं लिया जाता, क्योंकि-
- ऑक्सीजन अनेक तत्त्वों के साथ अभिक्रिया करके यौगिक बनाता है।
- इस परमाणु द्रव्यमान इकाई द्वारा अधिकांश तत्त्वों के परमाणु द्रव्यमान पूर्णांक में प्राप्त होते हैं।
प्रश्न 14.
परमाणु किस प्रकार अस्तित्व में रहते हैं?
उत्तर:
अधिकांश तत्त्वों के परमाणु स्वतंत्र रूप से अस्तित्व में नहीं रह पाते। परमाणु अणु एवं आयन बनाते हैं। ये अणु अथवा आयन अत्यधिक संख्या में पुंजित होकर वह द्रव्य बनाते हैं, जिसे हम देख सकते हैं, अनुभव कर सकते हैं अथवा छू सकते हैं।
प्रश्न 15.
निम्नलिखित सरल यौगिकों को आण्विक मॉडल द्वारा दर्शाएँ-
(1) जल
(2) अमोनिया
(3) एथिल ऐल्कोहॉल
(4) क्लोरीन
(5) फास्फोरस
(6) सल्फर।
उत्तर:
दिए गए यौगिकों के आण्विक सूत्र निम्नांकित है-
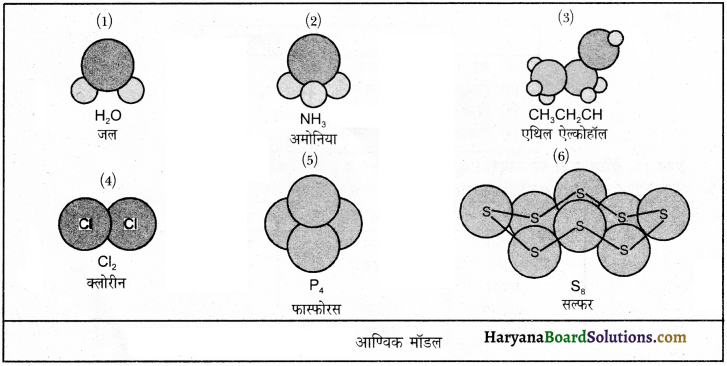
प्रश्न 16.
निम्नलिखित में परस्पर अंतर बताइए-
(1) हाइड्रोजन के परमाणु तथा उसके अणु।
(2) ऑक्सीजन के अणु तथा जल के अणु।
(3) चीनी के अणु तथा जल के अणु।
(4) कैल्शियम ऑक्साइड के अणु तथा मैग्नीशियम ऑक्साइड के अणु।
उत्तर:
(1) हाइड्रोजन की सबसे छोटी इकाई (H) हाइड्रोजन का एक परमाणु है, परंतु हाइड्रोजन का एक अणु हाइड्रोजन के दो परमाणुओं से मिलकर बनता है (H2)।
(2) ऑक्सीजन के एक अणु में ऑक्सीजन के दो परमाणु होते हैं (O2), परंतु जल के एक अणु में हाइड्रोजन के दो परमाणु तथा ऑक्सीजन का एक परमाणु होता है (H2O)।
(3) चीनी के एक अणु में कार्बन के 12 परमाणु, हाइड्रोजन के 22 परमाणु तथा ऑक्सीजन के 11 परमाणु होते हैं (C12H22O11), परंतु जल के एक अणु में हाइड्रोजन के दो परमाणु तथा ऑक्सीजन का एक परमाणु होता है (H2O)।
(4) कैल्शियम ऑक्साइड के एक अणु में कैल्शियम का एक परमाणु तथा ऑक्सीजन का एक परमाणु होता है (CaO), परंतु मैग्नीशियम ऑक्साइड के एक अणु में मैग्नीशियम का एक परमाणु तथा ऑक्सीजन का एक परमाणु होता है (MgO)।
प्रश्न 17.
निम्नलिखित यौगिकों में उपस्थित तत्त्वों के नाम एवं प्रत्येक तत्त्व के उपस्थित परमाणुओं की संख्या लिखिए-
खाने का सोडा (NaHCO3), सोडियम कार्बोनेट (Na2CO3), कॉपर सल्फेट (CuSO4), रेत (SiO2), ऐलुमिनियम क्लोराइड (AlCl3)।
उत्तर:
दिए गए यौगिकों में उपस्थित तत्त्वों के नाम एवं प्रत्येक तत्त्व में उपस्थित परमाणुओं की संख्या निम्नांकित सारणी में दी गई है-
| यौगिक | उपस्थित तत्त्व | परमाणुओं की संख्या |
| (1) खाने का सोडा (NaHCO3) | सोडियम (Na) हाइड्रोजन (H) कार्बन (C) ऑक्सीजन (O) | 1 1 1 3 |
| (2) सोडियम कार्बोनेट (Na2CO3) | सोडियम (Na) कार्बन (C) ऑक्सीजन (O) | 2 1 3 |
| (3) कॉपर सल्फेट (CuSO4) | कॉपर (Cu) सल्फर (S) ऑक्सीजन (O) | 1 1 4 |
| (4) रेत (SiO2) | सिलीकॉन (Si) ऑक्सीजन (O) | 1 2 |
| (5) ऐलुमिनियम क्लोराइड (AlCl3) | ऐलुमिनियम (Al) क्लोरीन (Cl) | 1 3 |
प्रश्न 18.
एक-परमाणुक, द्वि-परमाणुक तथा बहु-परमाणुक से क्या अभिप्राय है?
उत्तर:
- एक-परमाणुक-जो तत्त्व एकल परमाणु के रूप में पाए जाते हैं, उन्हें ‘एक-परमाणुक’ कहते हैं; जैसे हीलियम (He) व निऑन (Ne)।
- द्वि-परमाणुक-जिन तत्त्वों के एक अणु में दो परमाणु होते हैं, उन्हें द्वि-परमाणुक कहते हैं; जैसे हाइड्रोजन (H2), ऑक्सीजन (O2) व नाइट्रोजन (N2)।
- बहु-परमाणुक-जिन तत्त्वों के एक अणु में दो से अधिक परमाणु होते हैं, उन्हें बहु-परमाणु कहते हैं; जैसे फॉस्फोरस (P4) एवं सल्फर (S8)।
प्रश्न 19.
परमाणुकता से क्या अभिप्राय है? कुछ तत्त्वों के सूत्र एवं परमाणुकता लिखें।
उत्तर:
किसी तत्त्व के एक अणु में उपस्थित परमाणुओं की संख्या उसकी परमाणुकता कहलाती है। कुछ तत्त्वों के सूत्र एवं परमाणुकता निम्नलिखित हैं-
| तत्त्व | सूत्र | परमाणुकता |
| हाइड्रोजन | H2 | 2 |
| हीलियम | He | 1 |
| नाइट्रोजन | N2 | 2 |
| ऑक्सीजन | O2 | 2 |
| निऑन | Ne | 1 |
| फॉस्फोरस | P4 | 4 |
| सल्फर | S8 | 8 |
| क्लोरीन | Cl2 | 2 |
| ब्रोमीन | Br2 | 2 |
प्रश्न 20.
किसी यौगिक का रासायनिक सूत्र लिखते समय किन बातों को ध्यान में रखना चाहिए?
उत्तर:
किसी यौगिक का रासायनिक सूत्र लिखते समय निम्नलिखित बातों को ध्यान में रखना चाहिए-
(1) आयन की संयोजकता अथवा आवेश संतुलित होना चाहिए।
(2) जब एक यौगिक किसी धातु एवं अधातु के संयोग से बना होता है तो धातु के नाम अथवा उसके प्रतीक को रासायनिक सूत्र में पहले लिखते हैं। उदाहरणस्वरूप कैल्शियम ऑक्साइड (CaO), सोडियम क्लोराइड (NaCl), आयरन सल्फाइड (FeS), कॉपर ऑक्साइड (CuO) इत्यादि, जहाँ पर ऑक्सीजन, क्लोरीन, सल्फर अधातुएँ हैं तथा उन्हें दायीं तरफ लिखते हैं, जबकि कैल्शियम, सोडियम, आयरन एवं कॉपर धातुएँ हैं तथा उन्हें बायीं तरफ लिखते हैं।
(3) बहु-परमाणुक आयनों द्वारा निर्मित यौगिकों में आयन को पहले कोष्ठक में रखते हैं। तत्पश्चात अनुपातों को दर्शाने वाली संख्या को लिखते हैं।
प्रश्न 21.
पानी का रासायनिक सूत्र H2O है। इससे हमें क्या जानकारी मिलती है?
उत्तर:
पानी के रासायनिक सूत्र H2O से हमें निम्नलिखित जानकारी मिलती है-
(1) रासायनिक सूत्र से हमें यह पता चलता है कि दिया गया यौगिक H2O हाइड्रोजन तथा ऑक्सीजन से मिलकर बना है।
(2) रासायनिक सूत्र से हमें दिए गए पदार्थ के एक अणु में उपस्थित प्रत्येक तत्त्व के परमाणुओं की संख्या का भी पता चलता है अर्थात् H2O में दो हाइड्रोजन परमाणु तथा एक ऑक्सीजन परमाणु है।
(3) रासायनिक सूत्र द्वारा पदार्थ में उपस्थित प्रत्येक तत्त्व की संयोजकता का पता चल जाता है अर्थात् H2O में ऑक्सीजन की संयोजकता 2 तथा हाइड्रोजन की संयोजकता 1 है।
(4) रासायनिक सूत्र द्वारा हमें दिए गए पदार्थ के अणु द्रव्यमान का ज्ञान हो जाता है अर्थात् H2O का अणु द्रव्यमान 1×2 + 16 = 18 u है।
(5) रासायनिक सूत्र से हमें पता चलता है कि दिए गए पदार्थ में उसके अवयव तत्त्वों के परमाणुओं की संख्या का अनुपात तथा द्रव्यमान की दृष्टि से अनुपात क्या है अर्थात् H2O में H : O = 2 : 1 तथा द्रव्यमान की दृष्टि से H : 0 = 2 : 16 या = 1 : 8 है।
(6) रासायनिक अणु सूत्र यह दर्शाता है कि दिया गया यौगिक विद्युत दृष्टि से उदासीन है अर्थात् H2O पर कोई आवेश नहीं है।
![]()
प्रश्न 22.
सूत्र की सहायता से अणु द्रव्यमान या अणु भार कैसे निकाला जाता है?
उत्तर:
सूत्र की सहायता से अणु द्रव्यमान निम्नलिखित प्रकार से निकाला जाता है-
- सबसे पहले यौगिक का रासायनिक सूत्र लिखो।
- अब प्रत्येक तत्त्व को पृथक्-पृथक् लिखो।
- फिर सभी तत्त्वों के परमाणुओं की संख्या लिखो।
- फिर तत्त्वों के परमाणु द्रव्यमान को लिखो।
- अब तत्त्वों के परमाणुओं की संख्या को उनके परमाणु द्रव्यमानों से गुणा करो।
- अब सभी गुणनफलों को जोड़ो। यह यौगिक का शुद्ध द्रव्यमान होता है।
उदाहरण-
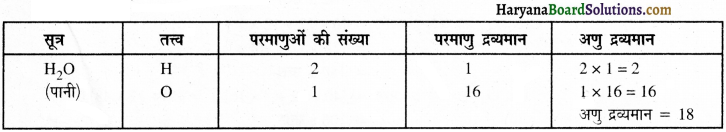
प्रश्न 23.
निम्नलिखित यौगिकों के एक-एक मोल में क्लोरीन परमाणु के कितने मोल विद्यमान हैं?
(क) Cl2O7
(ख) HCl
(ग) BaCl2
(घ) AlCl3
(ङ) FeCl3
(च) CCl4
हल-
| यौगिक | क्लोरीन परमाणुओं के मोल |
| (क) Cl2O7 | 2 |
| (ख) HCl | 1 |
| (ग) BaCl2 | 2 |
| (घ) AlCl3 | 3 |
| (ङ) FeCl3 | 3 |
| (च) CCl4 | 4 |
प्रश्न 24.
दिए गए यौगिक AB में तत्त्व A तथा तत्त्व B की द्रव्यमान प्रतिशतता कैसे ज्ञात की जाती है?
उत्तर:
AB एक यौगिक है जिसका एक तत्त्व A है तथा B दूसरा तत्त्व है। हम A की द्रव्यमान प्रतिशतता द्रव्यमान के अनुसार AB के सौ भागों में A के भाग के रूप में देते हैं।

प्रश्न 25.
परमाणु, अणु तथा आयन को परिभाषित कीजिए।
उत्तर:
- परमाणु-तत्त्व का सूक्ष्मतम कण परमाणु होता है, जो स्वतंत्र रूप से रह सकता है तथा उसके सभी रासायनिक गुणधर्मों को प्रदर्शित करता है।
- अणु-अणु, किसी तत्त्व अथवा यौगिक का वह सूक्ष्मतम कण होता है जो सामान्य दशाओं में स्वतंत्र रह सकता है। यह उस यौगिक के सभी गुणधर्मों को प्रदर्शित करता है।
- आयन-धातु एवं अधातु युक्त यौगिक आवेशित कणों से बने होते हैं। इन आवेशित कणों को आयन कहते हैं।
गणनात्मक प्रश्न
प्रश्न 1.
निम्नलिखित यौगिकों का अणु द्रव्यमान ज्ञात कीजिए-
(1) NH3
(2) NaCl
(3) (NH4), SO4
(4) Al2 (SO4)3
(5) C6H12O6
(6) CaCO3
[N = 14, H = 1, Na = 23, Cl = 35.5, S = 32, O = 16, Al = 27, C = 12, Ca = 40]
हल:
(1) NH3, का अणु द्रव्यमान = [14 + 3 x 1] u
= [14 + 3] u
= 17 u उत्तर
(2) NaCl का अणु द्रव्यमान = [23 + 35.5] u
= 58.5 u उत्तर
(3) (NH4)2, SO4 का अणु द्रव्यमान = [2 (14 + 4 x 1) + 32 + 4 x 16] u
= [2 (18) + 32 + 64] u
= [36 + 32 + 64] u
= 132 u उत्तर
(4) Al2(SO4)3 का अणु द्रव्यमान = [2 x 27 + 3 (32 + 4 x 16)] u
= [54 + 3 (32 + 64)] u = [54 + 3 (96)] u
= [54 + 288] u
= 342 u उत्तर
(5) C6H12O6 का अणु द्रव्यमान = [6 x 12 + 12 x 1 + 6 x 16] u
= [72 + 12 + 96] u
= 180 u उत्तर
(6) CaCO3 का अणु द्रव्यमान = [40 + 12 + 3 x 16] u = [40 + 12 + 48] u
= 100 u उत्तर
प्रश्न 2.
निम्न में अणुओं की संख्या का परिकलन कीजिए
(1) 0.25 mole ऑक्सीजन गैस
(2) 66 g कार्बन डाइऑक्साइड।
हल:
(1) ∵ ऑक्सीजन के 1 मोल में होते हैं = 6.022 x 1023
∴ अणु . ऑक्सीजन के 0.25 मोल में होंगे = 6.022 x 1023 x 0.25 अणु
= 1.505 x 1023 अणु उत्तर
(2) CO2 का 1 मोल = ग्रामों में CO2 का आण्विक द्रव्यमान
= C का द्रव्यमान + O का द्रव्यमान x 2
= 12 + 16 x 2 = 12 + 32 = 44g
अब 44g कार्बन डाइऑक्साइड = 6.022 x 1023 अणु
∴ 66g कार्बन डाइऑक्साइड =\(\frac{6.022 \times 10^{23}}{44}\) x 66 अणु = 9.033 x 1023 अणु उत्तर
प्रश्न 3.
2.8 ग्राम द्रव्यमान वाले लोहे (Fe) के टुकड़े में लोहे के कितने परमाणु होंगे? (Fe = 56 ग्राम)
हल:
लोहे के परमाणुओं का एक मोल = 6.022 x 1023 परमाणु
= 56 ग्राम
56 ग्राम लोहे में परमाणुओं की संख्या = 6.022 x 1023
2.8 ग्राम लोहे में परमाणुओं की संख्या = \(\frac{6.022 \times 10^{23}}{56}\) x 2.8 = 3.011 x 1022 परमाणु उत्तर
प्रश्न 4.
निम्नलिखित का द्रव्यमान ग्रामों में ज्ञात करें-
(1) सल्फ्यूरिक अम्ल (H2SO4) का एक मोल
(2) ऐलुमिनियम सल्फेट [Al2(SO4) का 0.5 मोल।
हल:
(1) H2SO4 के एक मोल का ग्रामों में द्रव्यमान = 1 x 2 + 32 + 16 x 4
= 2 + 32 + 64
= 98 ग्राम उत्तर
(2) Al2 (SO4)3 के एक मोल का ग्रामों में द्रव्यमान = 27 x 2 + 3 (32 + 16 x 4)
= 54+ 3(32 + 64)
= 54 + 3 x 96
54 + 288 = 342 ग्राम उत्तर
∴ Al2(SO4)3 के 0.5 मोल का ग्रामों में द्रव्यमान = 342 x 0.5
= 342 x \(\frac { 5 }{ 10 }\)
= 171 ग्राम उत्तर
प्रश्न 5.
20 ग्राम कैल्शियम कार्बोनेट (CaCO3) में CaCO3 के मोलों की संख्या ज्ञात कीजिए।
हल:
CaCO3 का एक मोल = 40 x 1 + 12 x 1 + 16 x 3
= 40 + 12 + 48
= 100 ग्राम
अतः 100 ग्राम CaCO3 में मोलों की संख्या = 1
20 ग्राम CaCO3 में मोलों की संख्या = \(\frac { 1 }{ 100 }\) x 20
= 0.2 मोल उत्तर
प्रश्न 6.
ऐलुमिनियम सल्फेट [Al2 (SO4)3] के 34.2 ग्राम लवण में प्रत्येक तत्त्व के कितने-कितने मोल होंगे?
हल:
Al2(SO4)3) का 1 मोल = 2 x 27 + 3 x 32 + 12 x 16
= 54 + 96 + 192
= 342 ग्राम
(1) 342 ग्राम Al2 (SO4)3 में Al मोलों की संख्या = 2 मोल
∴ 34.2 ग्राम Al2 (SO4), में Al मोलों की संख्या = \(\frac { 2 }{ 342 }\) = 34.2
= 0.2 मोल उत्तर
(2) 342 ग्राम Al2 (SO4)3 में S मोलों की संख्या = 3 मोल
∴ 34.2 ग्राम Al2 (SO4)3 में S मोलों की संख्या = \(\frac { 3 }{ 342 }\) x 34.2
0.3 मोल उत्तर
(3) 342 ग्राम Al2 (SO4)3 में O मोलों की संख्या = 12 मोल
∴ 34.2 ग्राम Al2 (SO4)3 में O मोलों की संख्या = \(\frac { 12 }{ 342 }\) x 34.2
= 1.2 मोल उत्तर
प्रश्न 7.
H2O के एक ग्राम में जल के कितने अणु हैं?
हल:
H2O का 1 मोल = 1 x 2 + 16 x 1
= 2 + 16 = 18 ग्राम
अतः 18 ग्राम (एक मोल) H2O में अणु = 6.022 x 1023
1 ग्राम H2O में अणु =\(
= 3.346 x 1022 उत्तर
प्रश्न 8.
निम्नलिखित को मोल में परिवर्तित कीजिए
(1) 3.012 x 1023 सोडियम परमाणु, (2) 180 g जल।
हल:
(1) ∵ 6.022 x 1023 सोडियम परमाणु = 1 मोल सोडियम
∴ 3.012 x 1023 सोडियम परमाणु = [latex}\frac{1}{6.022 \times 10^{23}}\) x 3.012 x 1023 = \(\frac { 1 }{ 2 }\) = मोल सोडियम
∵ 18g जल = 1 मोल जल
∴ 180g जल = \(\frac { 1 }{ 18 }\) x 180 मोल जल = 10 मोल जल उत्तर
![]()
प्रश्न 9.
6.022 x 1023 N2 अणुओं की संख्या का द्रव्यमान ज्ञात कीजिए।
हल:
1 मोल N= 2 x 14 = 28g
= 6.022 x 1023 अणु
अतः 6.022 x 1023 अणु N2 अणु का द्रव्यमान = 28g उत्तर
प्रश्न 10.
निम्नलिखित के मोलर द्रव्यमान की गणना कीजिए तथा उनकी उपयुक्त मात्रक इकाइयाँ दीजिए-
C2H5OH, S8, PCl5
हल:
हम जानते हैं कि पदार्थ के एक मोल अणुओं का द्रव्यमान उसका मोलर द्रव्यमान कहलाता है।
(1) C2H5OH का मोलर द्रव्यमान = (2 x 12 + 5 x 1 + 16 + 1) g/mol
= (24+5+ 16 + 1) g/mol
= 46 g/mol उत्तर
(2) S8 का मोलर द्रव्यमान = (8 x 32 = 256) g/mol उत्तर
(3) PCl5 का मोलर द्रव्यमान = (31 +5 x 35.5) g/mol
= (31 + 177.5) g/mol
= 208.5 g/mol उत्तर
प्रश्न 11.
0.1 मोल कार्बन परमाणु में कणों की संख्या का परिकलन कीजिए।
हल:
1 मोल कार्बन = 6.022 x 1023 कण
0.1 मोल कार्बन = 0.1 x 6.022 x 1023 कण
= 6.022 x 1022 कण उत्तर
प्रश्न 12.
निम्नलिखित के अणु द्रव्यमान का परिकलन कीजिए।
(1) PCIL (2) NH3 (3) CH2 Cl2, (4) H2O2 (5) S8 (6) HCl
जबकि-P = 31, Cl = 35.5, N = 14, H = 1, C = 12, 0 = 16, S = 32
हल:
(1) PCl5, का अणु द्रव्यमान = [31 + 5 x 35.5] u
= [31 + 177.5] u
= 208.5 u उत्तर
(2) NH3 का अणु द्रव्यमान = [14 + 3 x 1] u
= 17 u उत्तर
(3) CH2Cl2 का अणु द्रव्यमान
= [12 + 2 x 1 + 2 x 35.5] u
= [12 + 2 +71] u
= 85 u उत्तर
(4) H2O2 का अणु द्रव्यमान = [2 x 1 + 2 x 16] u
= [2 + 32] u
= 34u उत्तर
(5) S8 का अणु द्रव्यमान = 8 x 32 u = 256 u
HCl का अणु द्रव्यमान = [1 + 35.5] u
= 36.5 u उत्तर
प्रश्न 13.
नीचे दिए गए यौगिकों के सूत्र द्रव्यमान का परिकलन कीजिए-
(1) Mg0, (2) CaCl2 (3) CaCO3, (4) AlCI3
हल:
(1) MgO का सूत्र द्रव्यमान = [24 + 16] ग्राम
= 40 ग्राम उत्तर
(2) CaCl2 का सूत्र द्रव्यमान = [40 + 2 x 35.5] ग्राम
= [40 + 71] ग्राम = 111 ग्राम उत्तर
(3) CaCO53 का सूत्र द्रव्यमान = [40 + 12 + 3 x 16] ग्राम
= [40 + 12+ 48] ग्राम
= 100 ग्राम उत्तर
(4) AlCl3 का सूत्र द्रव्यमान = [27 + 3 x 35.5] ग्राम
= [27 + 106.5] ग्राम
= 133.5 ग्राम उत्तर
प्रश्न 14.
1 मोल फॉर्मेल्डिहाइड (CH2O) में प्रत्येक तत्त्व की प्रतिशतता का परिकलन कीजिए।
हल:
CH2O का मोलर द्रव्यमान = [12 + 2 x 1 + 16] g/mol
= 30g/mol
CH2O में C की प्रतिशतता = \(\frac { 12 }{ 30 }\) x 100 = 40% उत्तर
CH2O में H की प्रतिशतता = \(\frac { 2×1 }{ 30 }\) x 100 = 6.7% उत्तर
CH2O में O की प्रतिशतता = x 100 = 53.3% उत्तर
प्रश्न 15.
6.3g नाइट्रिक अम्ल (HNO3) में प्रत्येक तत्त्व के कितने परमाणु होते हैं?
हल:
HNO3 का अणु द्रव्यमान = 1 x 1 + 14 x 1 + 16 x 3
= 1 + 14 + 48
= 63 u
1 मोल HNO3 का द्रव्यमान = 63 ग्राम
63 ग्राम HNO3 = 1 मोल
∴ 6.3 ग्राम HNO3 = \(\frac { 1×6.3 }{ 63 }\) मोल
= 0.1 मोल
(1) 1 मोल HNO3 में H-परमाणुओं की संख्या = 1 मोल H-परमाणु अथवा
= 6.022 x 1023 H-परमाणु (आवोगाद्रो संख्या)
∴ 0.1 मोल HNO3, में H-परमाणुओं की संख्या = \(\frac{6.022 \times 10^{23} \times 0.1}{1}\)
= 6.022 x 1022 H-परमाणु उत्तर
(2) 1 मोल HNO3 में N-परमाणुओं की संख्या = 1 मोल N-परमाणु
= 6.022 x 1023 N-परमाणु
∴ 0.1 मोल HNO3 में N-परमाणुओं की संख्या = \(\frac{6.022 \times 10^{23} \times 0.1}{1}\)
= 6.022 x 1022 N-परमाणु उत्तर
(3) 1 मोल HNO3 में O-परमाणुओं की संख्या = 3 मोल O-परमाणु
= 3 x 6.022 x 1023 O-परमाणु
= 18.066 x 1023 O-परमाणु
∴ 0.1 मोल HNO3 में 0-परमाणओं की संख्या = \(\frac{18.066 \times 10^{23} \times 0.1}{1}\)
= 18.066 x 1023 O-परमाणु उत्तर
प्रश्न 16.
9.5 g मैग्नीशियम क्लोराइड में क्लोराइड आयन की संख्या का परिकलन कीजिए। (परमाणु संहति : Mg = 24,Cl = 35.5)
हल:
मैग्नीशियम क्लोराइड (MgCl2) का 1 मोल = Mg का द्रव्यमान + Cl का द्रव्यमान x 2
= 24 + 35.5 x 2
= 24 + 71 = 95 g
∵ 95g मैग्नीशियम क्लोराइड = 1 मोल
∴ 9.5 g मैग्नीशियम क्लोराइड = \(\frac { 1 }{ 95 }\) x 9.5 मोल
= 0.1 मोल
1 मोल मैग्नीशियम क्लोराइड = 2 x 6.022 x 1023 क्लोराइड आयन
अतः 0.1 मोल मैग्नीशियम क्लोराइड = 0.1 x 2 x 6.022 x 1023 क्लोराइड आयन
= 1.2044 x 1023 क्लोराइड आयन उत्तर
प्रश्न 17.
निम्न यौगिकों के सूत्र इकाई द्रव्यमान का परिकलन कीजिए।
Na2SO4, ZnCO3, CaSO4, H2SO3, HNO2 तथा N2O5
(परमाणु द्रव्यमान : Na = 23.0u, S = 32.0u, O = 16.0u, Zn = 65.0u, C = 12.0u, Ca = 40.0u, H = 1.0u, N = 14.0u)
हल:
(i) Na2SO4 का सूत्र इकाई द्रव्यमान = [2 x 23 + 1 x 32 + 4 x 16] u
= [46 + 32 + 64]u
= 142u
(ii) ZnCO3 का सूत्र इकाई द्रव्यमान = [1 x 65 + 1 x 12 + 3 x 16] u
= [65 + 12 + 48] u
= 125u
(iii) CaSO4 का सूत्र इकाई द्रव्यमान = [1 x 40 + 1 x 32 + 4 x 16] u
= [40+ 32 + 64] u
= 136u
(iv) H2SO4 का सूत्र इकाई द्रव्यमान = [2 x 1 + 1 x 32 + 3 x 16] u
= [2+ 32+ 48] u
= 82u
(v) HNO2 का सूत्र इकाई द्रव्यमान = [1 x 1 + 1 x 14 + 2 x 16] u
= [1 + 14 + 32] u
= 47u
(vi) NO2 का सूत्र इकाई द्रव्यमान = [2 x 14 + 5 x 16] u
= [28 + 80] u
= 108u
निबंधात्मक प्रश्न
प्रश्न 1.
किसी यौगिक का अणु सूत्र ज्ञात करने की विधि का वर्णन करें।
उत्तर:
अज्ञात यौगिक के विषय में निम्नलिखित महत्त्वपूर्ण जानकारी प्राप्त करके यौगिक का अणु सूत्र ज्ञात किया जा सकता है-
- सबसे पहले यौगिक की प्रतिशत संख्या ज्ञात होनी चाहिए। इसके लिए यौगिक में उपस्थित विभिन्न तत्त्वों का प्रतिशत ज्ञात करो।
- आवर्त सारणी में तत्त्वों के परमाणु द्रव्यमान ज्ञात करो।
- तत्त्व की प्रतिशत मात्रा को परमाणु द्रव्यमान से भाग देकर तत्त्वों का परमाणु अनुपात ज्ञात करो।
- तत्त्वों का सरलतम अनुपात ज्ञात करने के लिए तत्त्वों के अनुपात को उनमें से सबसे छोटी अनुपात द्वारा भाग करो।
- तत्त्वों के संकेत साथ-साथ लिखो। उनके नीचे दाईं ओर संबंधित परमाणु अनुपात लिखो। इस प्रकार यौगिक का मूलानुपाती सूत्र ज्ञात हो जाएगा।
- मूलानुपाती सूत्र में तत्त्वों का द्रव्यमान लिखकर मूलानुपाती सूत्र का द्रव्यमान ज्ञात करो।
- अणु द्रव्यमान को मूलानुपाती सूत्र द्रव्यमान से भाग देकर अनुपाती संख्या ‘n’ का मान ज्ञात करो।

- मूलानुपाती सूत्र को n से गुणा करके अणु सूत्र ज्ञात किया जा सकता है।
अणुसूत्र = मूलानुपाती सूत्र x n
प्रश्न 2.
निम्न यौगिकों के सूत्र लिखिए
(1) हाइड्रोजन क्लोराइड, (2) हाइड्रोजन सल्फाइड, (3) कार्बन टेट्राक्लोराइड, (4) मैग्नीशियम क्लोराइड, (5) कैल्शियम ऑक्साइड, (6) ऐलुमिनियम ऑक्साइड।
उत्तर:
आण्विक यौगिकों के रासायनिक सूत्र लिखते समय हम पहले संघटक तत्त्वों के प्रतीक लिखकर उनकी संयोजकताएं लिखते हैं। तत्पश्चात् संयोजित परमाणुओं की संयोजकताओं को क्रॉस करके (cross over) अणु सूत्र लिखते हैं।
(1) हाइड्रोजन क्लोराइड का सूत्र

अतः हाइड्रोजन क्लोराइड का रासायनिक सूत्र = HCl
(2) हाइड्रोजन सल्फाइड के सूत्र

अतः हाइड्रोजन सल्फाइड का सूत्र = H2
(3) कार्बन टेट्राक्लोराइड का सूत्र

अतः कार्बन टेट्राक्लोराइड का सूत्र = CCl4
(4) मैग्नीशियम क्लोराइड का सूत्र

अतः मैग्नीशियम क्लोराइड का सूत्र = MgCl2
(5) कैल्शियम ऑक्साइड का सूत्र

यहाँ पर दोनों तत्त्वों की संयोजकताएँ समान हैं। अतः इसका सूत्र Ca2O2 प्राप्त होगा, किंतु हम इस सूत्र को Ca0 के रूप में सरलीकृत करते हैं।
(6) ऐलुमिनियम ऑक्साइड का सूत्र

अतः ऐलुमिनियम ऑक्साइड का सूत्र = Al2O3
प्रश्न 3.
निम्नलिखित बहु-परमाणुक आयनों वाले यौगिकों के सूत्र लिखें
(1) सोडियम नाइट्रेट, (2) कैल्शियम हाइड्रॉक्साइड, (3) अमोनियम सल्फेट, (4) सोडियम कार्बोनेट।
उत्तर:
(1) सोडियम नाइट्रेट का सूत्र

अतः सूत्र = NaNO3
(2) कैल्शियम हाइड्रॉक्साइड का सूत्र

अतः सूत्र = Ca (OH)2
(3) अमोनियम सल्फेट का सूत्र-
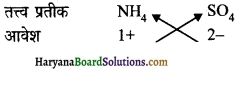
अतः सूत्र = (NH4)2SO4
(4) सोडियम कार्बोनेट का सूत्र-

अतः सूत्र = Na2CO3
प्रयोगात्मक कार्य
क्रियाकलाप 1.
द्रव्यमान संरक्षण नियम को एक प्रयोग द्वारा सिद्ध कीजिए।
कार्य-विधि-कॉपर सल्फेट तथा सोडियम कार्बोनेट के 5% विलयन जल में तैयार कीजिए। अब सोडियम कार्बोनेट के विलयन की कुछ मात्रा को एक शंक्वाकार फ्लास्क में लीजिए तथा कॉपर सल्फेट की कुछ मात्रा को एक परखनली में लेकर शंक्वाकार फ्लास्क
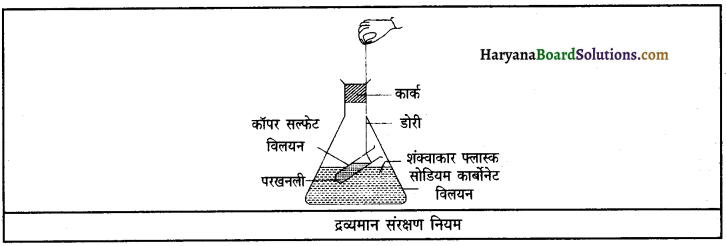
में इस प्रकार लटकाइए कि दोनों विलयन परस्पर मिश्रित न हों जैसा कि चित्र में दिखाया गया है। तत्पश्चात फ्लास्क के मुख पर कार्क लगाकर उसका द्रव्यमान ज्ञात कीजिए।
अब फ्लास्क को झुकाकर इस प्रकार घुमाएँ कि दोनों विलयन परस्पर मिश्रित हो जाए। अब पुनः फ्लास्क का द्रव्यमान नोट कीजिए। आप देखेंगे कि क्रिया से पहले तथा क्रिया के बाद शंक्वाकार फ्लास्क द्रव्यमान समान आता है। इससे द्रव्यमान संरक्षण का नियम सिद्ध हो जाता है।
क्रियाकलाप 2.
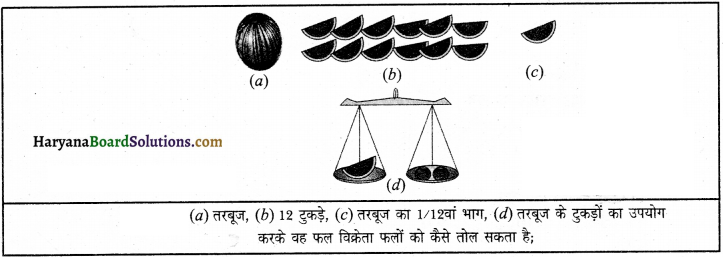
मानक परमाणु द्रव्यमान इकाई को समझाने के लिए एक क्रियाकलाप का वर्णन करें।
कार्य-विधि-माना एक फल विक्रेता बिना मानक भार के फल बेच रहा है। वह एक तरबूज लेकर कहता है कि “इसका द्रव्यमान 12 इकाई है।” वह तरबूज के 12 बराबर टुकड़े करता है तथा पाता है कि उसके द्वारा बेचे जा रहे प्रत्येक फल का द्रव्यमान तरबूज के एक टुकड़े के द्रव्यमान के सापेक्ष है। जैसे चित्र में दिखाया गया है। अब वह फलों को सापेक्ष फल द्रव्यमान इकाई (fmu) में बेचता है।
इस प्रकार किसी तत्त्व के सापेक्षिक परमाणु द्रव्यमान को उसके परमाणुओं के औसत द्रव्यमान का कार्बन-12 परमाणु के द्रव्यमान के 1/12वें भाग के अनुपात द्वारा परिभाषित किया जाता है।
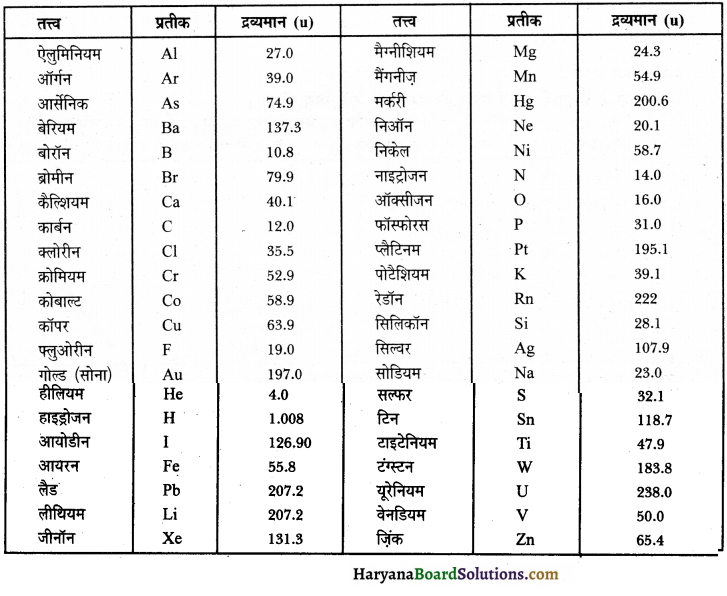
विशेष जानकारियाँ एवं सारणियाँ
सारणी-I कुछ सामान्य तत्त्वों के प्रतीक व परमाणु द्रव्यमानों की सूची
सारणी-II कुछ सामान्य, सरल एवं बहु-परमाणुक आयन आयन
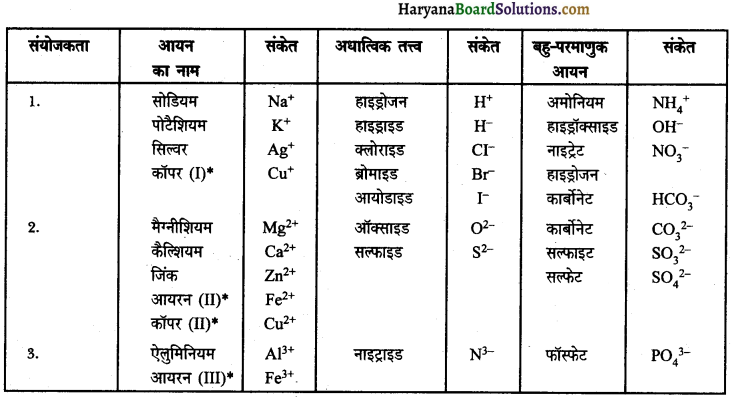
कुछ तत्त्व एक से अधिक संयोजकता दर्शाते हैं। संयोजकता को कोष्ठकों में रोमन संख्यांक द्वारा प्रदर्शित करते हैं।
अध्याय कास्ताव अध्ययन
1. किस भारतीय दार्शनिक ने पदार्थ के सूक्ष्मतम अविभाज्य कण को परमाणु की संज्ञा दी?
(A) महर्षि कनाड
(B) पकुधा
(C) डॉ० राधाकृष्णन
(D) डॉ० रमन
उत्तर:
(A) महर्षि कनाड
2. द्रव्यमान संरक्षण का नियम किस वैज्ञानिक की देन है?
(A) डेमोक्रिटस
(B) लियुसीपस
(C) लवाइजिए एवं जोजफ एल० प्राउस्ट
(D) जॉन डॉल्टन
उत्तर:
(C) लवाइजिए एवं जोजफ एल० प्राउस्ट
3. स्थिर अनुपात के नियम का जनक कौन है?
(A) जॉन डाल्टन
(B) लवाइजिए
(C) लियुसीपस
(D) डेमोक्रिटस
उत्तर:
(B) लवाइजिए
4. जॉन डाल्टन का परमाणु सिद्धांत है-
(A) सभी द्रव्य परमाणुओं से निर्मित होता है
(B) परमाणु अविभाज्य सूक्ष्मतम कण होते हैं
(C) एक तत्त्व के परमाणुओं के गुणधर्म एक समान होते हैं
(D) उपर्युक्त सभी
उत्तर:
(D) उपर्युक्त सभी
5. डाल्टन द्वारा सुझाया हाइड्रोजन का प्रतीक था-
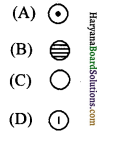
उत्तर:

6. डाल्टन के अनुसार फॉस्फोरस का प्रतीक था-
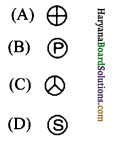
उत्तर:

7. IUPAC के अनुसार कोबाल्ट का प्रतीक है-
(A) K
(B) Co
(C) CO
(D) C
उत्तर:
(B) Co
8. IUPAC के अनुसार ऐलुमिनियम का सही प्रतीक है-
(A) AL
(B) aL
(C) al
(D) Al
उत्तर:
(D) Al
9. IUPAC के अनुसार सिलिकॉन का प्रतीक है-
(A) si
(B) sl
(C) Si
(D) Cl
उत्तर:
(C) Si
10. हाइड्रोजन का परमाणु द्रव्यमान है-
(A) 1
(B) 2
(C) 4
(D) 6
उत्तर:
(A) 1
11. कार्बन का परमाणु द्रव्यमान कितना है?
(A) 4
(B) 6
(C) 12
(D) 16
उत्तर:
(C) 12
![]()
12. ओजोन में उपस्थित ऑक्सीजन के परमाणुओं की संख्या होती है-
(A) 2
(B) 3
(C) 4
(D) 5
उत्तर:
(B) 3
13. सोडियम का परमाणु द्रव्यमान कितना है?
(A) 11
(B) 23
(C) 46
(D) इनमें से कोई नहीं
उत्तर:
(B) 23
14. सल्फर की परमाणुकता कितनी होती है?
(A) 8
(B) 7
(C) 5
(D) 3
उत्तर:
(A) 8
15. क्लोरीन का परमाणु द्रव्यमान है-
(A) 17
(B) 35
(C) 35.5
(D) 34
उत्तर:
(C) 35.5
16. जल में हाइड्रोजन व ऑक्सीजन का द्रव्यमान अनुपात कितना है?
(A) 1:4
(B) 1:8
(C) 8:1
(D) 1:16
उत्तर:
(B) 1:8
17. अमोनिया में नाइट्रोजन और हाइड्रोजन का द्रव्यमान अनुपात है-
(A) 7:1
(B) 14:1
(C) 14:3
(D) 7:14
उत्तर:
(C) 14:3
18. कार्बन डाइऑक्साइड में कार्बन और ऑक्सीजन का द्रव्यमान अनुपात है-
(A) 3:8
(B) 16:3
(C) 8:3
(D) 2:7
उत्तर:
(A) 3:8
19. ऐलुमिनियम आयन का सही संकेत है-
(A) Al+
(B) Al1+
(C) Al2+
(D) Al2+
उत्तर:
(D) Al2+
20. लौह तत्त्व का लैटिन नाम क्या है?
(A) फेरम
(B) क्यूप्रम
(C) केलियम
(D) नैट्रियम
उत्तर:
(A) फेरम
21. हाइड्रोजन क्लोराइड का रासायनिक सूत्र क्या है?
(A) HCl
(B) HCl2
(C) HCl3
(D) H2Cl
उत्तर:
(A) HCl
22. हाइड्रोजन सल्फाइड का रासायनिक सूत्र है-
(A) HS
(B) H2S
(C) H2S2
(D) H2S3
उत्तर:
(B) H2S
23. कार्बन टेट्राक्लोराइड का सूत्र क्या है?
(A) C4Cl
(B) CCl
(C) CCl4
(D) C4C4
उत्तर:
(C) CCl4
24. सोडियम कार्बोनेट का सूत्र है
(A) NaCO3
(B) NaCO2
(C) Na2CO3
(D) Na3CO3
उत्तर:
(C) Na2CO3
25. साधारण नमक का रासायनिक सूत्र है-
(A) Nacl
(B) MgCl
(C) CaCl2
(D) Ca(OH)2
उत्तर:
(A) NaCl
26. HNO3 का आण्विक द्रव्यमान होता है-
(A) 53u
(B) 63 u
(C) 73u
(D) 58.5 u
उत्तर:
(B) 63 u
27. NaCl का आण्विक द्रव्यमान कितना होता है?
(A) 36.5u
(B) 35.5u
(C) 58.5 u
(D) 63 u
उत्तर:
(C) 58.5 u
28. CaCl2 का आण्विक द्रव्यमान कितना होता है?
(A) 98.2 u
(B) 112 u
(C) 112 u
(D) 114.2 u
उत्तर:
(B) 111 u
29. HCI का मोलर द्रव्यमान होता है-
(A) 35.5 g/mol
(B) 36.5 g/mol
(C) 63 g/mol
(D) 73 g/mol
उत्तर:
(B) 36.5 g/mol
30. HNO3 का मोलर द्रव्यमान होता है-
(A) 63 g/mol
(B) 635 g/mol
(C) 26 g/mol
(D) 124 g/mol
उत्तर:
(A) 63 g/mol
31. पोटैशियम का प्रतीक है-
(A) Pt
(B) K
(C) P
(D) Pm
उत्तर:
(B) K
32. सोडियम का प्रतीक है-
(A) S
(B) So
(C) Na
(D) Sd
उत्तर:
(C) Na
33. 3g हाइड्रोजन गैस के साथ पूर्ण रूप से संयोग करने के लिए ऑक्सीजन गैस के कितने द्रव्यमान की आवश्यकता होगी?
(A) 3g
(B) 8g
(C) 11g
(D) 24g
उत्तर:
(D) 24g
34. ऐलुमिनियम क्लोराइड का सूत्र क्या है?
(A) AlCl
(B) Al3Cl
(C) AlCl3
(D) AlCl2
उत्तर:
(C)AlCl3
35. सोडियम सल्फाइड का सूत्र है-
(A) NaS
(B) Na2S
(C) NaS2
(D) Na2 S2
उत्तर:
(B) Na2S
36. 4 मोल ऐलुमिनियम परमाणु का द्रव्यमान होगा?
(A) 27g
(B) 4g
(C) 108g
(D) 31g
उत्तर:
(C) 108 g
37. 12g ऑक्सीजन में मोल ज्ञात करो-
(A) 0.375 mol
(B) 3.75 mol
(C) 37.5 mol
(D) 375 mol
उत्तर:
(A) 0.375 mol
38. धन आवेशित आयन को क्या कहा जाता है?
(A) ऋणायन
(B) ऐनायन
(C) धनायन
(D) उदासीन आयन
उत्तर:
(C) धनायन
39. क्लोरीन आयन (Cl–) में इलेक्ट्रानों की संख्या क्या होती है?
(A) 35
(B) 36
(C) 17
(D) 18
उत्तर:
(D) 18