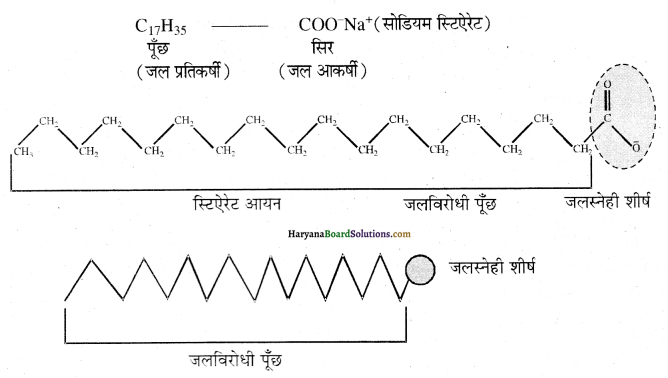
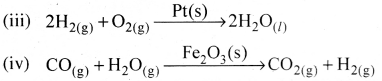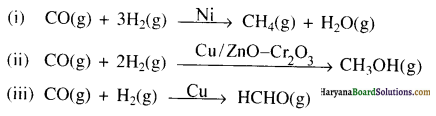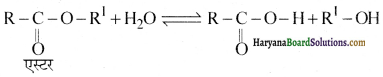Haryana State Board HBSE 12th Class Economics Important Questions Chapter 6 प्रतिस्पर्धारहित बाज़ार Important Questions and Answers.
Haryana Board 12th Class Economics Important Questions Chapter 6 प्रतिस्पर्धारहित बाज़ार
वस्तुनिष्ठ प्रश्न
A. नीचे दिए गए चार विकल्पों में से सही विकल्प चुनिए
1. एकाधिकार में-
(A) वस्तु के कई निकट स्थानापन्न होते हैं
(B) वस्तु का कोई निकट स्थानापन्न नहीं होता
(C) वस्तु विभेद पाया जाता है
(D) कीमत विभेद नहीं होता
उत्तर:
(B) वस्तु का कोई निकट स्थानापन्न नहीं होता
2. एकाधिकारी फर्म को अल्पकाल संतुलन में-
(A) न्यूनतम हानि हो सकती है
(B) असामान्य लाभ हो सकते हैं
(C) सामान्य लाभ हो सकते हैं ।
(D) उपर्युक्त सभी
उत्तर:
(D) उपर्युक्त सभी

3. दीर्घकाल में एकाधिकार फर्म को-
(A) हानि होती है
(B) असामान्य लाभ मिलते हैं
(C) सामान्य लाभ मिलते हैं
(D) पूर्ण प्रतिस्पर्धा की तुलना में कम हानि होती है
उत्तर:
(B) असामान्य लाभ मिलते हैं
4. एकाधिकारी प्रतिस्पर्धा की अवस्था में फर्म को अल्पकाल में संतुलन की स्थिति में-
(A) अधिकतम लाभ प्राप्त होते हैं
(B) न्यूनतम हानि होती है
(C) सामान्य लाभ प्राप्त होते हैं
(D) उपर्युक्त सभी
उत्तर:
(D) उपर्युक्त सभी
5. एकाधिकारी प्रतिस्पर्धा में दीर्घकाल में फर्म को संतुलन की अवस्था में केवल-
(A) सामान्य लाभ प्राप्त होते हैं
(B) असामान्य लाभ प्राप्त होते हैं
(C) न्यूनतम हानि प्राप्त होती है
(D) उपर्युक्त सभी
उत्तर:
(A) सामान्य लाभ प्राप्त होते हैं
6. एकाधिकार में कीमत-
(A) सीमांत लागत से अधिक होती है
(B) सीमांत लागत के बराबर होती है
(C) सीमांत लागत से कम होती है
(D) सीमांत लागत से कम या अधिक होती रहती है
उत्तर:
(A) सीमांत लागत से अधिक होती है
7. एकाधिकार में किस समय अवधि में फर्म को केवल असामान्य लाभ प्राप्त होते हैं?
(A) अति अल्पकाल में
(B) अल्पकाल में
(C) दीर्घकाल में
(D) इनमें से कोई नहीं
उत्तर:
(C) दीर्घकाल में
8. एकाधिकार के अंतर्गत फर्म के माँग वक्र का स्वरूप क्या है?
(A) पूर्ण लोचदार
(B) पूर्ण बेलोचदार
(C) कम लोचदार
(D) अधिक लोचदार
उत्तर:
(C) कम लोचदार
9. एकाधिकारी प्रतियोगिता में किस समय-अवधि में फर्म को केवल असामान्य लाभ प्राप्त होते हैं?
(A) अल्पकाल में
(B) अति-अल्पकाल में
(C) दीर्घकाल में
(D) अति-दीर्घकाल में
उत्तर:
(A) अल्पकाल में
10. निम्नलिखित में से एकाधिकारी बाज़ार की विशेषता नहीं है
(A) फर्मों के प्रवेश व निकासी की स्वतंत्रता
(B) निकटतम स्थानापन्न का अभाव
(C) एक विक्रेता
(D) कीमत विभेद की संभावना
उत्तर:
(A) फर्मों के प्रवेश व निकासी की स्वतंत्रता
11. वस्तु विभेद किस बाज़ार की प्रमुख विशेषता है?
(A) एकाधिकार की
(B) पूर्ण प्रतिस्पर्धा की
(C) एकाधिकारी प्रतिस्पर्धा की
(D) इनमें से कोई नहीं
उत्तर:
(C) एकाधिकारी प्रतिस्पर्धा की

12. गैर-कीमत प्रतियोगिता सर्वाधिक पाई जाती है
(A) एकाधिकार में
(B) पूर्ण प्रतिस्पर्धा में
(C) एकाधिकारी प्रतिस्पर्धा में ..
(D) इनमें से कोई नहीं
उत्तर:
(C) एकाधिकारी प्रतिस्पर्धा में
13. अपूर्ण प्रतिस्पर्धा में बाज़ार की कौन-सी अवस्था हो सकती है?
(A) एकाधिकारी प्रतिस्पर्धा
(B) अल्पाधिकार
(C) द्वि-अधिकार
(D) उपर्युक्त सभी
उत्तर:
(D) उपर्युक्त सभी
14. किस बाज़ार के लिए फर्म के लिए कीमत रेखा क्षैतिज सरल रेखा होती है?
(A) एकाधिकारी
(B) पूर्ण प्रतिस्पर्धा
(C) एकाधिकारी प्रतियोगिता
(D) अल्पाधिकार
उत्तर:
(B) पूर्ण प्रतिस्पर्धा
15. किस बाज़ार में विक्रय लागतों का बहुत अधिक महत्त्व होता है?
(A) पूर्ण प्रतियोगी बाज़ार में
(B) अल्पाधिकार बाज़ार में
(C) अपूर्ण प्रतियोगिता बाज़ार में
(D) इनमें से कोई नहीं
उत्तर:
(C) अपूर्ण प्रतियोगिता बाज़ार में
16. एकाधिकार में सीमांत संप्राप्ति वक्र का आकार कैसा होता है?
(A) धनात्मक ढलान वाला
(B) OX-अक्ष के समानांतर
(C) OY-अक्ष के समानांतर
(D) ऋणात्मक ढलान वाला
उत्तर:
(D) ऋणात्मक ढलान वाला
17. अल्पकाल में एकाधिकार के संतुलन की अवस्था में निम्नलिखित में से कौन-सी अवस्था हो सकती है?
(A) असामान्य लाभ
(B) सामान्य लाभ
(C) न्यूनतम हानि
(D) उपर्युक्त सभी
उत्तर:
(D) उपर्युक्त सभी
18. एकाधिकार होता है
(A) कीमत-निर्धारक
(B) कीमत स्वीकार करने वाला
(C) (A) तथा (B) दोनों
(D) इनमें से कोई नहीं
उत्तर:
(A) कीमत-निर्धारक
B. रिक्त स्थानों की पूर्ति कीजिए
1. पूर्ण प्रतियोगिता में वस्तुएँ ……………… होती हैं। (भिन्न, समरूप)
उत्तर:
समरूप
2. एकाधिकारी बाज़ार में एकाधिकारी कीमत …………… होता है। (निर्धारक, स्वीकारक)
उत्तर:
निर्धारक
3. विज्ञापन लागते ……………. में अधिक महत्त्वपूर्ण होती हैं। (एकाधिकार, एकाधिकारी प्रतियोगिता)
उत्तर:
एकाधिकारी प्रतियोगिता
4. ……………… एकाधिकार बाज़ार की मुख्य विशेषता होती है। (वस्तु विभेद, कीमत विभेद)
उत्तर:
कीमत विभेद
5. ‘अल्पाधिकार’ में ………………… विक्रेता पाए जाते हैं। (बहुत अधिक, कुछ)
उत्तर:
कुछ
6. ‘एकाधिकार’ की तुलना में ‘एकाधिकारी प्रतियोगिता’ में AR तथा MR वक्र सापेक्षिक ……………… लोचदार होते हैं। (कम, अधिक)
उत्तर:
अधिक
7. एकाधिकारी प्रतियोगिता (प्रतिस्पर्धा) में AR तथा MR वक्र एक-दूसरे के ……………….. होते हैं। (बराबर, भिन्न)
उत्तर:
भिन्न
8. द्वयाधिकार बाज़ार में वस्तु के ……………. विक्रेता पाए जाते हैं। (एक, दो)
उत्तर:
दो
9. विक्रय लागते ……………. बाज़ार में अधिक उपयोगी होती हैं। (एकाधिकार, एकाधिकारी प्रतियोगिता)
उत्तर:
एकाधिकारी प्रतियोगिता
10. गैर-कीमत प्रतियोगिता सर्वाधिक ………………. में पाई जाती है। (पूर्ण प्रतियोगिता, एकाधिकारी प्रतियोगिता)
उत्तर:
एकाधिकारी प्रतियोगिता
11. एकाधिकारी प्रतियोगिता में एक फर्म दीर्घकाल में …………. लाभ प्राप्त करती है। (सामान्य, असामान्य)
उत्तर:
सामान्य

C. बताइए कि निम्नलिखित कथन सही हैं या गलत-
- सर्वाधिक गैर कीमत प्रतियोगिता एकाधिकारी प्रतियोगिता में पाई जाती है।
- एकाधिकारी कीमत सदैव ऊँची होती है।
- एकाधिकार के अंतर्गत कीमत 10 रु० होगी यदि सीमांत लागत 10 रु० है।
- एकाधिकारी प्रतियोगिता में फर्मों के आने व छोड़कर जाने की स्वतंत्रता नहीं होती।
- एकाधिकार में कीमत, सीमान्त लागत के समान होती है।
- एक एकाधिकारी प्रतियोगी फर्म को दीर्घकाल में असामान्य लाभ प्राप्त होंगे।
- एकाधिकारी दीर्घकाल में असामान्य लाभ प्राप्त नहीं कर सकता।
- एकाधिकार में औसत आगम (AR) वक्र तथा सीमांत आगम (MR) वक्र एक-समान होते हैं।
- पूर्ण प्रतियोगिता में औसत आगम (AR) वक्र तथा सीमांत आगम (MR) वक्र एक-दूसरे के बराबर नहीं होते।
- एकाधिकारी बाजार में एकाधिकारी कीमत निर्धारक होता है।
- एकाधिकार में कीमत विभेद संभव होता है।
- एकाधिकारी प्रतियोगिता में AR तथा MR वक्र एक-दूसरे के भिन्न होते हैं।
- अल्पाधिकार में दो विक्रेता पाए जाते हैं।
- द्वयाधिकार बाज़ार में वस्तु के दो विक्रेता पाए जाते हैं।
- विज्ञापन लागतें एकाधिकारी प्रतियोगिता में अधिक महत्त्वपूर्ण होती हैं।
उत्तर:
- सही
- गलत
- गलत
- गलत
- गलत
- गलत
- गलत
- गलत
- गलत
- सही
- गलत
- सही
- गलत
- सही
- सही।
अति-लघूत्तरात्मक प्रश्न
प्रश्न 1.
बाज़ार किसे कहते हैं?
उत्तर:
बाज़ार का अर्थ किसी विशेष स्थान से नहीं है बल्कि किसी वस्तु की मात्रा के क्रय-विक्रय से है।

प्रश्न 2.
बाज़ार के मुख्य रूप कौन-कौन से हैं?
उत्तर:
- पूर्ण प्रतियोगिता
- एकाधिकार
- एकाधिकारी प्रतियोगिता
- अल्पाधिकार।
प्रश्न 3.
एकाधिकार (Monopoly) क्या है?
उत्तर:
एकाधिकार बाज़ार की वह स्थिति है जिसमें वस्तु का एक ही विक्रेता होता है और उस वस्तु का कोई निकट स्थानापन्न नहीं होता।
प्रश्न 4.
एकाधिकारी प्रतिस्पर्धा (Monopolistic Competition) क्या है?
उत्तर:
एकाधिकारी प्रतिस्पर्धा बाज़ार की वह स्थिति है जिसमें वस्तु के बहुत-से विक्रेता लगभग एक-जैसी विभेदीकृत वस्तुओं (Differentiated Goods) के रूप में बेचने की प्रतिस्पर्धा करते हैं।
प्रश्न 5.
गठबंधन प्रतियोगिता और गैर-गठबंधन प्रतियोगिता में अंतर बताहए।
अथवा
गठबंधन अल्पाधिकार तथा गैर-गठबंधन अल्पाधिकार से आपका क्या अभिप्राय है?
उत्तर:
गठबंधन प्रतियोगिता या अल्पाधिकार-गठबंधन प्रतियोगिता अल्पाधिकार बाजार की वह स्थिति है जिसमें सभी फर्मे एक-दूसरे के सहयोग से अपनी वस्तुओं की कीमतों को निर्धारित करती हैं। ये एक-दूसरे से किसी भी प्रकार की कोई प्रतिस्पर्धा नहीं करतीं। गैर-गठबंधन प्रतियोगिता या अल्पाधिकार-गैर-गठबंधन प्रतियोगिता अल्पाधिकार बाजार की वह स्थिति है जिसमें सभी फर्मे स्वतंत्र रूप से अपनी वस्तुओं की कीमतों को निर्धारित करती हैं और इनमें प्रतिस्पर्धा होती है।
प्रश्न 6.
अल्पाधिकार की परिभाषा दीजिए।
उत्तर:
अल्पाधिकार बाज़ार की वह स्थिति है जिसमें वस्तु के कुछ उत्पादक होते हैं। वाटसन के अनुसार, “अल्पाधिकार वह बाजार अवस्था है जिसमें समरूप अथवा विभेदीकृत वस्तुएँ बेचने वाली थोड़ी-सी फर्मे होती हैं।”
प्रश्न 7.
कीमत विभेद किसे कहते हैं?
उत्तर:
एक ही वस्तु को विभिन्न क्रेताओं को भिन्न-भिन्न कीमतों पर बेचना कीमत विभेद कहलाता है।
प्रश्न 8.
विभेदीकृत उत्पादों (Differentiated Products) से क्या अभिप्राय है?
उत्तर:
विभेदीकृत उत्पादों से अभिप्राय उन उत्पादों से है जिनकी प्रकृति एक-समान होती है, परंतु जिन्हें ब्रांड नाम, आकार, रंग, डिज़ाइन, गुण, सेवा आदि के आधार पर अन्य वस्तुओं से विभेदित किया जाता है।
प्रश्न 9.
वस्तु विभेद (Product Differentiation) से आप क्या समझते हैं?
उत्तर:
वस्तु विभेद से अभिप्राय उस प्रक्रिया से है जिसके अंतर्गत एक-समान स्वभाव वाली वस्तुओं को विज्ञापन, पैकिंग, ब्रांड आदि के आधार पर अन्य वस्तुओं से भिन्न बनाया जाता है।
प्रश्न 10.
विक्रय लागते (Selling Costs) क्या होती हैं?
उत्तर:
विक्रय लागतों से अभिप्राय उन लागतों से है जिन्हें फर्म की बिक्री बढ़ाने के लिए व्यय किया जाता है।
प्रश्न 11.
विज्ञापन लागतें क्या होती हैं?
उत्तर:
विज्ञापन लागतें वे लागतें होती हैं जो एकाधिकारी प्रतिस्पर्धा फर्मे अपनी-अपनी वस्तुओं के प्रचार पर बिक्री बढ़ाने के उद्देश्य से व्यय करती हैं।
प्रश्न 12.
पेटेंट अधिकार क्या होते हैं?
उत्तर:
पेटेंट अधिकार वे अधिकार हैं जिनमें धारक को ही एक विशेष उत्पादन विधि या नए उत्पाद का प्रयोग करने का अधिकार होता है और अन्य किसी भी उत्पादक को धारक से लाइसेंस पाए बिना इसके उत्पादन या प्रयोग करने का अधिकार नहीं होता।
प्रश्न 13.
संगुट विरोधी (Anti Trust) कानून क्या होते हैं?
उत्तर:
संगुट विरोधी कानून ऐसे कानून हैं जो उन सभी प्रकार के विलय (Merger), अधिग्रहण (Acquisition) और व्यावसायिक गतिविधियों को सीमित करते हैं जिनके कारण दक्षता में नाममात्र की वृद्धि परंतु बाज़ार पर नियंत्रण की संभावना अधिक होती है।
प्रश्न 14.
एकाधिकारी प्रतिस्पर्धा में दीर्घकाल में फर्म असामान्य लाभ अर्जित क्यों नहीं कर पाती?
उत्तर:
क्योंकि दीर्घकाल में अन्य फळं बाजार में प्रवेश करके असामान्य लाभ को सामान्य लाभ में बदल देती हैं।
लघूत्तरात्मक प्रश्न
प्रश्न 1.
एकाधिकार बाज़ार की कोई चार विशेषताएँ बताएँ।
उत्तर:
एकाधिकार बाज़ार की मुख्य विशेषताएँ निम्नलिखित हैं-
- एक विक्रेता-एकाधिकार बाज़ार में वस्तु का केवल एक ही विक्रेता होता है। अतः इस बाज़ार में फर्म तथा उद्योग का अंतर समाप्त हो जाता है।
- निकट स्थानापन्न का न होना-एकाधिकार बाजार जिस वस्तु का उत्पादन या विक्रय करता है, उसका कोई निकट स्थानापन्न नहीं होता।
- प्रवेश पर प्रतिबंध-एकाधिकार बाजार में नई फर्मों के प्रवेश पर प्रतिबंध होता है। इसलिए एकाधिकारी का कोई प्रतियोगी नहीं होता।
- पूर्ति पर प्रभावी नियंत्रण वस्तु की पूर्ति पर एकाधिकारी बाज़ार का पूर्ण नियंत्रण होता है।

प्रश्न 2.
एकाधिकारी प्रतिस्पर्धा की कोई चार विशेषताएँ बताएँ।
उत्तर:
एकाधिकारी प्रतिस्पर्धा की मुख्य विशेषताएँ निम्नलिखित हैं
1. फर्मों की अधिक संख्या एकाधिकारी प्रतिस्पर्धा में फर्मों की संख्या अधिक होती है। इस प्रकार विक्रेताओं में प्रतिस्पर्धा पाई जाती है।
2. वस्तु विभेद-एकाधिकारी प्रतिस्पर्धा में अनेक फर्मे मिलती-जुलती वस्तुओं का उत्पादन करती हैं। उन वस्तुओं में रंग, रूप, आकार, डिज़ाइन, पैकिंग, ब्रांड, ट्रेडमार्क, सुगंध आदि के आधार पर वस्तु विभेद (Product Variation) किया जाता है; जैसे पेप्सोडेंट, कोलगेट, फोरहन्स, क्लोज़अप आदि टूथपेस्ट। इन पदार्थों में एकरूपता तो नहीं होती, लेकिन वे एक-दूसरे के निकट स्थानापन्न (Close Substitutes) होते हैं।
3. फर्मों के निर्बाध प्रवेश और बहिर्गमन-एकाधिकारी प्रतिस्पर्धा बाज़ार में नई फर्मों के बाज़ार में प्रवेश करने और पुरानी फर्मों को बाजार छोडने की पूर्ण स्वतन्त्रता होती है।
4. विक्रय लागतें-एकाधिकारी प्रतिस्पर्धा बाज़ार में प्रत्येक फर्म को अपनी वस्तु का प्रचार करने के लिए विज्ञापनों पर बहुत व्यय करना पड़ता है। अतः एकाधिकारी प्रतिस्पर्धा में फर्मों में अपनी-अपनी बिक्री बढ़ाने के लिए कीमत प्रतियोगिता तो नहीं पाई जाती, बल्कि गैर-कीमत प्रतिस्पर्धा (Non-Price Competition) पाई जाती है।
प्रश्न 3.
उन कारकों की व्याख्या करें जिनके कारण एकाधिकार बाज़ार अस्तित्व में आया।
उत्तर:
एकाधिकार बाज़ार के अस्तित्व में आने के कारण निम्नलिखित हैं
1. सरकारी प्रतिबंध कई बार किसी क्षेत्र विशेष में अन्य किसी फर्म के प्रवेश करने पर सरकार प्रतिबंध लगा देती है। उदाहरण के लिए, रेल परिवहन के क्षेत्र में भारत सरकार ने अन्य किसी के प्रवेश पर प्रतिबंध लगाया हुआ है। अतः रेलवे परिवहन पर सरकार का एकाधिकार है।
2. लाइसेंस-सरकार द्वारा केवल एक कंपनी को किसी वस्तु या सेवा के उत्पादन का लाइसेंस देना किसी क्षेत्र या उद्योग में एकाधिकार फर्म को जन्म दे सकता है।
3. पेटेंट अधिकार-पेटेंट अधिकार के कारण भी एकाधिकार स्थापित हो सकता है। जब किसी एक फर्म अथवा उत्पादक को यह सरकारी मान्यता मिल जाती है कि उसके अलावा अन्य कोई भी फर्म उस वस्तु का उत्पादन अथवा उस तकनीक का प्रयोग नहीं कर सकती, जिसका विकास अथवा आविष्कार इस फर्म ने किया है तो इसे पेटेंट अधिकार कहते हैं। यह फर्मों को अन्वेषण एवं विकास के कार्य करते रहने हेतु प्रोत्साहित करने और जोखिम की पूर्ति के लिए दिया जाता है।
4. व्यापार गुट (कार्टेल) कभी-कभी किसी एक विशेष वस्तु के उत्पादक अपना स्वतंत्र अस्तित्व बनाए रखते हुए अधिकतम लाभ कमाने के लिए एकत्रित होकर एक संगठन बना लेते हैं, इसे व्यापार गुट (कार्टेल) कहा जाता है। वे इस संस्था के माध्यम से एकाधिकारी की तरह ही अपनी उत्पादन एवं कीमत नीति को लागू करते हैं।
प्रश्न 4.
एकाधिकारी प्रतिस्पर्धी फर्म का माँग वक्र अधिक लोचदार क्यों रहता है?
उत्तर:
एकाधिकारी प्रतिस्पर्धी फर्म द्वारा उत्पादित वस्तु की कई निकट प्रतिस्थापक वस्तुएँ बाज़ार में उपलब्ध होती हैं। जिस वस्तु की जितनी अधिक प्रतिस्थापक वस्तुएँ उपलब्ध होंगी उस वस्तु की माँग उतनी ही अधिक लोचदार होगी। इसलिए एक एकाधिकारी प्रतिस्पर्धी फर्म का माँग वक्र अधिक लोचदार रहता है। इसे हम संलग्न रेखाचित्र द्वारा दिखा सकते हैं।
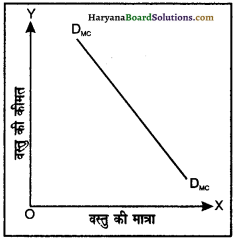
प्रश्न 5.
एकाधिकार और एकाधिकारी प्रतिस्पर्धा में से किस बाज़ार में फर्म का माँग वक्र अधिक लोचशील होता है और क्यों?
उत्तर:
एकाधिकारी प्रतिस्पर्धा और एकाधिकार दोनों ही अवस्थाओं में फर्मों का माँग वक्र अथवा औसत आगम वक्र दाईं ओर नीचे को झुका हुआ होता है। इसका अर्थ यह है कि दोनों प्रकार की फर्मों को अधिक मात्रा में वस्तु बेचने के लिए कीमत कम करनी पड़ती है। लेकिन एक एकाधिकारी फर्म का माँग वक्र कम लोचशील होता है क्योंकि इस अवस्था में वस्तु की कोई निकट स्थानापन्न वस्तु नहीं होती। इसके विपरीत, एकाधिकारी प्रतिस्पर्धा में एक फर्म का माँग वक्र अधिक लोचशील होता है क्योंकि उस वस्तु की कई निकट स्थानापन्न वस्तुएँ बाज़ार में उपलब्ध होती हैं। एकाधिकार और एकाधिकारी प्रतिस्पर्धा में फर्म के माँग वक्र को निम्नांकित रेखाचित्रों द्वारा दिखाया जाता है
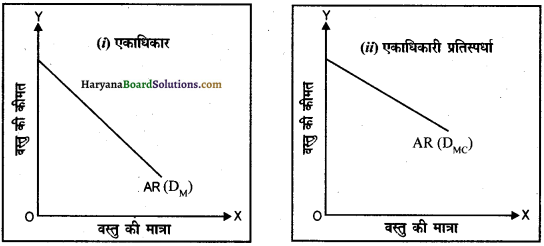
प्रश्न 6.
बताइए कि एकाधिकारी फर्म का सीमांत आगम औसत आगम से कम क्यों रहता है?
उत्तर:
एकाधिकारी फर्म पूरे बाज़ार में एकमात्र वस्तु का अकेला विक्रेता होता है। एकाधिकारी फर्म का वस्तु की पूर्ति पर पूर्ण नियंत्रण होता है। लेकिन उसका वस्तु की माँग पर कोई नियंत्रण नहीं होता। अतः एकाधिकारी फर्म अधिक लाभ कमाने के लिए वस्तु को अधिकतम मूल्य पर बेचने का प्रयास करेगी। विक्रेता को वस्तु की अधिकाधिक इकाइयाँ बेचने के लिए कीमत कम करनी पड़ती है। इसलिए फर्म का सीमांत आगम औसत आगम से कम रहता है। सीमांत आगम और औसत आगम दोनों वक्रों का ढाल ऊपर से नीचे की ओर होता है लेकिन सीमांत आगम औसत आगम से सदैव कम होता है। इसे हम संलग्न रेखाचित्र द्वारा दिखा सकते हैं।
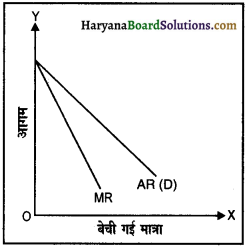
प्रश्न 7.
माँग की कीमत लोच और सीमांत आगम के बीच संबंध को एक | रेखाचित्र से स्पष्ट कीजिए।
उत्तर:
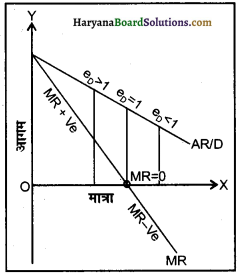
माँग की कीमत लोच (eD) और सीमांत संप्राप्ति (आगम) (MR) के बीच निकट संबंध रहता है। जैसे कि
(i) जब MR धनात्मक है तो कीमत लोच 1 से अधिक होती है।
(ii) जब MR शून्य होती है तो कीमत लोच 1 के बराबर होती है।
(iii) जब MR ऋणात्मक होता है तो कीमत लोच 1 से कम होती है। यह संबंध संलग्न रेखाचित्र द्वारा दर्शाया गया है।
प्रश्न 8.
द्वि-अधिकार बाज़ार की कोई चार विशेषताएँ बताएँ।
उत्तर:
द्वि-अधिकार बाज़ार की मुख्य विशेषताएँ निम्नलिखित हैं-
- यह एक ऐसी स्थिति है जिसमें केवल दो ही उत्पादक होते हैं।
- दोनों लगभग समान वस्तु का विक्रय करते हैं।
- दोनों ही अपने उत्पादन कार्य में स्वतंत्र होते हैं तथा दोनों ही वस्तुएँ एक-दूसरे से प्रतिस्पर्धा करती हैं।
- प्रत्येक प्रतिस्पर्धी को स्वयं अपनी नीति का निर्धारण करने में दूसरे प्रतिस्पर्धी की नीति को ध्यान में रखना आवश्यक होता है।
प्रश्न 9.
शून्य उत्पादन लागत वाली एकाधिकार फर्म के संतुलन को रेखाचित्र की सहायता से समझाइए।
उत्तर:
कभी-कभी एक एकाधिकारी फर्म की लागत शून्य होती है, क्योंकि उसे उत्पाद के लिए कोई कीमत नहीं चुकानी पड़ती। ऐसी स्थिति में फर्म का संतुलन उस बिंदु पर होगा जहाँ MC =MR है। एक फर्म की संतुलन स्थिति को हम संलग्न रेखाचित्र द्वारा दिखा सकते हैं
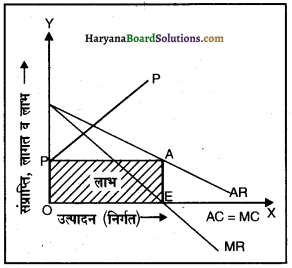
संलग्न रेखाचित्र में, X-अक्ष ही औसत व सीमांत लागत वक्र है, क्योंकि लागत शून्य है। E बिंदु पर MR=MC है इसलिए यह संतुलन बिंदु है, जहाँ फर्म को OPAE लाभ प्राप्त हो रहा है जो अधिकतम लाभ है। चूँकि हम जानते हैं कि जब MR = 0 होता है, तो TR अधिकतम होता है।

प्रश्न 10.
एकाधिकार फर्म के लिए माँग वक्र ही संरोध (Con-straint) कैसे बन जाता है?
उत्तर:
एकाधिकार फर्म पूरे बाज़ार में एकमात्र वस्तु का विक्रेता होता है। एकाधिकार फर्म का बाज़ार में वस्तु की पूर्ति पर पूरा नियंत्रण होता है। लेकिन कीमत प्रक्रिया के दूसरे पहलू माँग पर फर्म का कोई नियंत्रण नहीं होता क्योंकि माँग उपभोक्ताओं द्वारा की जाती है। एक फर्म अधिक लाभ कमाने के लिए वस्तु को अधिकतम कीमत पर बेचने का प्रयास करती है परंतु अधिकतम कीमत पर माँग कम होगी। अतः वस्तु की अधिक मात्रा बेचने के लिए फर्म को कीमत कम करनी पड़ती है। इस प्रकार फर्म के लिए माँग वक्र ही संरोध बन जाता है। इसे हम संलग्न रेखाचित्र द्वारा दिखा सकते हैं।
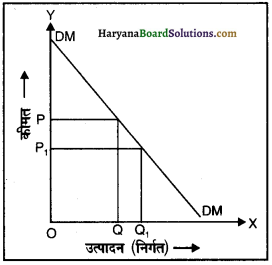
संलग्न रेखाचित्र में हम देखते हैं कि OP कीमत पर वस्तु की माँग केवल OQ है। OQ1 मात्रा बेचने के लिए फर्म को वस्तु की कीमत OP से कम करके OP1 करनी पड़ेगी।
प्रश्न 11.
एकाधिकारी प्रतिस्पर्धा क्या होती है? क्या ऐसे बाज़ार में एक विक्रेता कीमत को प्रभावित कर सकता है? समझाइए।
उत्तर:
एकाधिकारी प्रतिस्पर्धा बाज़ार की वह स्थिति है जिसमें एक बड़ी संख्या में फर्मे लगभग एक जैसी किंतु विभेदीकृत वस्तुओं को बेचने की प्रतिस्पर्धा करती हैं।
एकाधिकारी प्रतिस्पर्धा में यहाँ एक ओर फर्मों को प्रतिस्पर्धा का सामना करना पड़ता है वहीं दूसरी ओर फर्मों को वस्तु विभेद के कारण कुछ सीमा तक एकाधिकारी शक्ति भी प्राप्त होती है। इसलिए एक विक्रेता कीमत को प्रभावित कर सकता है। यहाँ एक विक्रेता कीमत निर्धारक होता है, कीमत स्वीकारक नहीं।
प्रश्न 12.
एकाधिकार व एकाधिकारी प्रतिस्पर्धा में औसत संप्राप्ति (AR) तथा सीमांत संप्राप्ति (MR) वक्र बनाइए।
उत्तर:
एकाधिकार तथा एकाधिकारी प्रतिस्पर्धा की अवस्थाओं में फर्म अपनी स्वतंत्र कीमत नीति अपना सकती है। फर्म कीमत को कम करके अधिक माल बेच सकती है तथा कीमत में वृद्धि करने पर फर्म का कम माल बिकेगा। अतः इन दोनों स्थितियों में औसत संप्राप्ति वक्र तथा सीमांत संप्राप्ति (आगम) वक्र गिरते हुए होते हैं और जब औसत संप्राप्ति गिर रही होती है तो सीमांत संप्राप्ति औसत संप्राप्ति से कम रहती है अर्थात् इन दोनों में मुख्य अंतर यह है कि एकाधिकार में आगम वक्र कम लोचदार (Less Elastic) और एकाधिकारी प्रतिस्पर्धा में अधिक लोचदार (More Elastic) होते हैं।
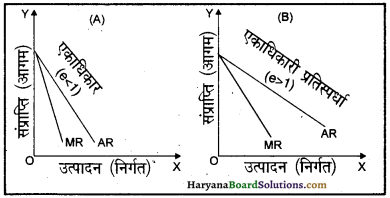
इसका अभिप्राय यह है कि यदि एकाधिकारी फर्म कीमत बढ़ा देती है, तो फर्म की कुल माँग पर कम प्रभाव पड़ता है क्योंकि एकाधिकार में वस्तु के स्थानापन्न (Substitutes) उपलब्ध नहीं होते जबकि एकाधिकारी प्रतिस्पर्धा वाली फर्म यदि वस्तु की कीमत बढ़ा देती है तो उसकी माँग पर अधिक प्रभाव पड़ता है, क्योंकि एकाधिकारी प्रतिस्पर्धा में वस्तु के स्थानापन्न उपलब्ध होते हैं।
प्रश्न 13.
एक प्रतिस्पर्धारहित बाज़ार में सीमांत संप्राप्ति (आगम) तथा कुल संप्राप्ति (आगम) का संबंध तालिका व रेखाचित्र की सहायता से समझाइए।
उत्तर:
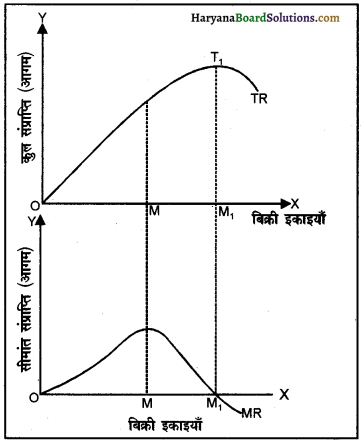
एक प्रतिस्पर्धारहित बाज़ार के कुल संप्राप्ति और सीमांत संप्राप्ति के संबंध को निम्न तालिका व रेखाचित्र से दिखा सकते हैं-
| बेची गई इकाइयाँ | प्रति इकाई कीसत | कुल आगम | सीमांत आगम |
| 1 | 10 | 10 | 10 |
| 2 | 9 | 18 | 8 |
| 3 | 8 | 24 | 6 |
| 4 | 7 | 28 | 4 |
| 5 | 6 | 30 | 2 |
| 6 | 5 | 30 | 0 |
| 7 | 4 | 28 | -2 |
| 8 | 3 | 24 | -4 |
तालिका तथा रेखाचित्रों से यह स्पष्ट होता है कि कुल आगम उस समय तक बढ़ता है जब तक कि सीमांत आगम धनात्मक अर्थात् शून्य से ऊपर है। कुल आगम वहाँ अधिकतम है जहाँ सीमांत आगम शून्य है। कुल आगम उस समय घटने लगता है जब सीमांत आगम ऋणात्मक अर्थात् शून्य से कम होता है। उपर्युक्त तालिका से यह स्पष्ट है कि सीमांत आगम पाँचवीं इकाई तक धनात्मक है।
अतः कुल आगम बढ़ रहा है। छठी इकाई पर कुल आगम अधिकतम है क्योंकि सीमांत आगम शून्य है। छठी इकाई के पश्चात् सीमांत आगम ऋणात्मक होने लगता है और कुल आगम घटने वाले होते हैं।
प्रश्न 14.
कुल संप्राप्ति (आगम) (TR) तथा सीमांत संप्राप्ति (MR) में संबंध तालिका एवं रेखाचित्र की सहायता से बताइए।
उत्तर:
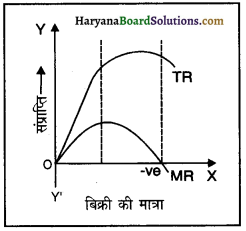
| बेची गई इकाइयाँ | TR | MR |
| 1 | 10 | – |
| 2 | 18 | 8 |
| 3 | 24 | 6 |
| 4 | 28 | 4 |
| 5 | 30 | 2 |
| 6 | 30 | 0 |
| 7 | 28 | – 2 |
(i) जब MR धनात्मक होता है तो TR बढ़ता है।
(ii) जब MR शून्य होता है, तो TR अधिकतम होता है।
(iii) जब MR ऋणात्मक होता है, तो TR गिरना शुरू कर देता है।
(iv) TR बढ़ती दर से बढ़ता है, जब तक MR बढ़ता है तथा TR घटती दर से बढ़ता है, जब तक MR गिरता है।
प्रश्न 15.
एकाधिकारी प्रतिस्पर्धा के अंतर्गत कुल संप्राप्ति, औसत संप्राप्ति और सीमांत संप्राप्ति के बीच संबंध बताइए। रेखाचित्र का प्रयोग कीजिए।
उत्तर:
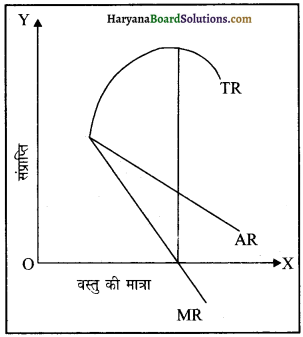
एकाधिकारी प्रतिस्पर्धा में एक फर्म कीमत निर्धारक होती है। एक फर्म अपनी वस्तु की बिक्री को तभी बढ़ा सकती है जब वह वस्तु की कीमत में कमी करे। इसलिए फर्म के AR और MR वक्र गिरते हुए सीधी रेखा के रूप में होते हैं। कुल संप्राप्ति वक्र का आकार उल्टे ‘U’ आकार का होता है, क्योंकि कुल संप्राप्ति पहले बढ़ती है, बाद में कम होती है। यह वस्तु की मात्रा संलग्न रेखाचित्र में दर्शाया गया है।
दीर्घ-उत्तरात्मक प्रश्न
प्रश्न 1.
द्वि-अधिकार (Duopoly) की परिभाषा दीजिए। इसकी विशेषताएँ बताइए।
उत्तर:
द्वि-अधिकार का अर्थ-द्वि-अधिकार से अभिप्राय बाजार की उस स्थिति से है जिसमें किसी एक ही सर्वथा समान अथवा लगभग समान वस्तु के दो उत्पादक होते हैं। दोनों ही अपने उत्पादन कार्य में स्वतंत्र होते हैं एवं दोनों की वस्तुएँ एक-दूसरे से पर्धा करती हैं। यदि एक विक्रेता अपनी उपज तथा कीमत संबंधी नीति में परिवर्तन करता है तो दूसरे की ओर से इसकी बलशाली प्रतिक्रिया होती है। इस प्रकार दोनों विक्रेताओं में से कोई भी बिना दूसरे की प्रतिक्रिया को ध्यान में रखे उत्पादन की मात्रा अथवा कीमत को निश्चित नहीं कर सकता।
द्वि-अधिकार बाजार की विशेषताएँ-द्वि-अधिकार बाजार की निम्नलिखित विशेषताएँ होती हैं-
- यह एक ऐसी स्थिति है जिसमें केवल दो ही उत्पादक होते हैं।
- दोनों सर्वथा समान अथवा लगभग समान वस्तु का विक्रय करते हैं।
- दोनों ही अपने उत्पादन कार्य में स्वतंत्र होते हैं तथा दोनों ही वस्तुएँ एक-दूसरे से प्रतिस्पर्धा करती हैं।
- अतः प्रत्येक प्रतिस्पर्धी को स्वयं अपनी नीति का निर्धारण करने में दूसरे प्रतिस्पर्धी की नीति को ध्यान में रखना आवश्यक होता है।
द्वि-अधिकार आवश्यक रूप से अपूर्ण प्रतिस्पर्धा की स्थिति नहीं होती, क्योंकि यदि दोनों विक्रेता परस्पर मिलकर उत्पादन करने लगे, तब द्वि-अधिकार की स्थिति समाप्त हो जाएगी। इसके विपरीत, यह भी संभव है कि कंठ-छेदी प्रतिस्पर्धा (Cut-throat competition) के कारण पूर्ण प्रतिस्पर्धा की सी दशाएँ उत्पन्न हो जाएँ।
प्रश्न 2.
कुल संप्राप्ति (TR) और कुल लागत (TC) वक्रों की सहायता से एक एकाधिकारी फर्म (Monopoly Firm) के संतुलन को समझाइए।
उत्तर:
कुल संप्राप्ति (आगम) तथा कुल लागत विधि द्वारा एकाधिकारी फर्म का संतुलन-एकाधिकार वस्तु की उस मात्रा को बेचकर अधिकतम लाभ प्राप्त कर सकता है जिस पर कुल संप्राप्ति (आगम) (Total Revenue) तथा कुल लागत (Total Cost) का अंतर अधिकतम होता है। एकाधिकार वस्तु की विभिन्न कीमतें निर्धारित करके अथवा वस्तु की पूर्ति में परिवर्तन लाकर यह जानने का प्रयास करता है कि उत्पादन के किस स्तर पर कुल संप्राप्ति (TR) तथा कुल लागत (TC) का अंतर अधिकतम है। उत्पादन की उस मात्रा पर जिसके उत्पादन से एकाधिकार को अधिकतम लाभ प्राप्त होंगे, एकाधिकार संतुलन की स्थिति में होगा। इसे संलग्न रेखाचित्र द्वारा स्पष्ट किया जा सकता है
रेखाचित्र में TC कुल लागत वक्र है, जो उत्पादन वृद्धि के साथ-साथ लागत में स्थिर दर से होने वाली वृद्धि को दर्शाता है। TR कुल संप्राप्ति वक्र है जो आरंभ में ऊपर की ओर बढ़ता है, बाद में चपटा (Flat) होता है और अंत में नीचे की ओर गिरता है जो एक निश्चित बिंदु के पश्चात कुल प्राप्तियों में गिरावट का प्रतीक है। TP कुल लाभ की रेखा है। यह Rबिंद से आरंभ होती है जो यह दर्शाती है कि प्रारंभिक स्थिति में फर्म को ऋणात्मक लाभ (Negative Profits) मिलते हैं। रेखाचित्र से यह स्पष्ट होता है कि जैसे-जैसे फर्म उत्पादन बढ़ाती है वैसे-वैसे कुल संप्राप्ति TR बढ़ती जाती है। आरंभ में TR < TC है। परिणामस्वरूप TR वक्र का RC भाग यह दिखाता है कि फर्म को हानि हो रही है। K बिंदु पर TR = TC है जो यह स्पष्ट करती है कि फर्म को न लाभ है और न ही हानि। जैसाकि TP के C बिंदु से स्पष्ट हो रहा है।
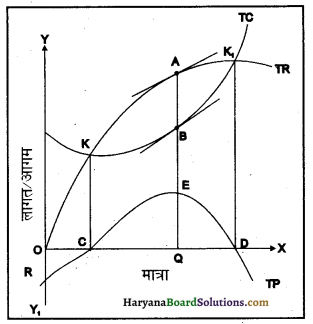
K बिंदु ‘समविच्छेद बिंदु’ (Break Even Point) कहलाता है। जब फर्म K बिंदु से अधिक उत्पादन करती है तो TR > TC है। C बिंदु के बाद TP वक्र भी दाएँ ऊपर की ओर बढ़ता है। यह इस बात का प्रतीक है कि फर्म लाभ प्राप्त कर रही है। जब TP वक्र अपने उच्चतम बिंदु E पर पहुँचता है तब फर्म अधिकतम लाभ कमा रही होती है। इसलिए OQ उत्पादन की मात्रा संतुलन मात्रा कहलाती है। यदि फर्म संतुलन मात्रा से अधिक उत्पादन करती है तो TR और TC वक्रों का अंतर कम होता जाता है जो कि दोबारा K1 बिंदु पर एक-दूसरे को काटते हैं। पुनः TR = TC हो जाते हैं। इसका अभिप्राय यह है कि फर्म के लाभ घटते जाते हैं और D बिंदु पर फर्म को न लाभ न हानि होती है। इस प्रकार बिंदु K1 भी ‘समविच्छेद बिंदु’ (Break Even Point) कहलाता है। यदि फर्म इससे भी अधिक मात्रा का उत्पादन करती है तो TR < TC हो जाता है और फर्म को हानि होने लगती है।
सारांश में फर्म E बिंदु पर अधिकतम लाभ प्राप्त करेगी। अधिकतम लाभ का अनुमान लगाने के लिए TR और TC वक्रों पर दो स्पर्श रेखाएँ (Tangents) खींची गई हैं। जिन बिंदुओं पर स्पर्श रेखाएँ समानांतर (Parallel) हैं, वहीं TR और TC का अंतर अधिकतम होता, है। जैसाकि रेखाचित्र में A और B बिंदुर चूँकि स्पर्श रेखाएँ परस्पर समानांतर हैं, इसलिए यहाँ TR और TC का अंतर अधिकतम है। इसी स्थिति में फर्म को अधिकतम लाभ प्राप्त होता है जो TP वक्र के E बिंदु से स्पष्ट है और E बिंदु ही फर्म का संतुलन बिंदु है।

प्रश्न 3.
सीमांत संप्राप्ति (MR) और सीमांत लागत (MC) विधि द्वारा एक एकाधिकारी फर्म की संतुलन स्थिति को समझाइए।
अथवा
एक एकाधिकारी किस प्रकार अपनी कीमत और मात्रा निर्धारित करता है? रेखाचित्र द्वारा समझाइए।
उत्तर:
सीमांत संप्राप्ति (आगम) तथा सीमांत लागत विधि द्वारा एकाधिकारी फर्म की संतुलन स्थिति-एकाधिकार की स्थिति उत्पादन तथा संतुलन स्थिति का निर्धारण सीमांत आगम और सीमांत लागत विधि द्वारा भी कर सकती है। इस विधि के अनुसार एकाधिकारी उस समय संतुलन स्थिति में होता है जहाँ निम्नलिखित दो शर्ते पूरी होंगी
- सीमांत संप्राप्ति (आगम) (MR) = सीमांत लागत (MC) हो
- सीमांत लागत (MC) वक्र सीमांत संप्राप्ति (MR) वक्र को नीचे से काटता हो।
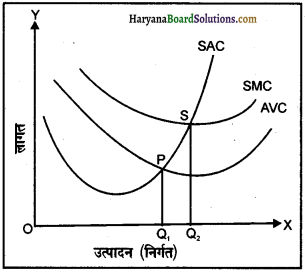
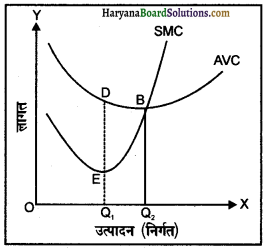
एकाधिकार में कीमत, उत्पादन तथा संतुलन निर्धारण दिए गए रेखाचित्र द्वारा स्पष्ट किया गया है रेखाचित्र में औसत लागत, तथा सीमांत लागत वक्र को माँग (औसत संप्राप्ति) वक्र तथा सीमांत संप्राप्ति वक्र के साथ दर्शाया गया है। रेखाचित्र से स्पष्ट है कि q0 के नीचे उत्पादन स्तर पर सीमांत संप्राप्ति स्तर सीमांत लागत स्तर से ऊँचा है। तात्पर्य यह है कि वस्तु की एक अतिरिक्त इकाई के विक्रय से प्राप्त कुल संप्राप्ति में वृद्धि उस अतिरिक्त इकाई की उत्पादन लागत में वृद्धि से अधिक होती है। इसका अर्थ यह है कि उत्पादन की एक अतिरिक्त इकाई से अतिरिक्त लाभ का सृजन होगा। चूँकि लाभ में परिवर्तन = कुल संप्राप्ति में परिवर्तन – कुल लागत में परिवर्तन। अतः यदि फर्म q0 से कम स्तर पर वस्तु का उत्पादन कर रही है, तो वह अपने उत्पादन में वृद्धि लाना चाहेगी, क्योंकि इससे उसके लाभ में बढ़ोतरी होगी। जब तक सीमांत संप्राप्ति (MR) वक्र सीमांत लागत (MC) वक्र के ऊपर स्थित है, तब तक उपर्युक्त D = AR तर्क का अनुप्रयोग होगा। अतः फर्म अपने उत्पादन में वृद्धि करेगी। इस प्रक्रम में तब रुकावट आएगी, जब उत्पादन का स्तर q0 पर प. प. पहुँचेगा, क्योंकि इस स्तर पर सीमांत संप्राप्ति (MR) और सीमांत उत्पादन (निर्गत) MR लागत (MC) दोनों समान होंगे और उत्पादन में वृद्धि से लाभ में किसी प्रकार की वृद्धि नहीं होगी।
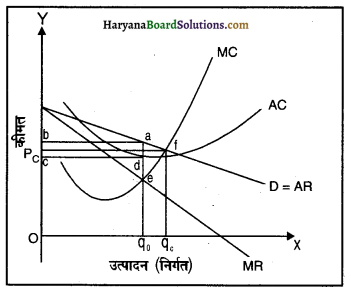
दूसरी ओर, यदि फर्म q0 से अधिक मात्रा में वस्तु का उत्पादन करती है तो सीमांत लागत (MC) सीमांत संप्राप्ति से अधिक होती है। अभिप्राय यह है कि उत्पादन की एक इकाई कम करने से कुल लागत में जो कमी होती है, वह इस कमी के कारण कल संप्राप्ति में हुई हानि से अधिक होती है। अतः फर्म के लिए यह उपयुक्त है कि वह उत्पादन में कमी लाए। यह तर्क तब तक ठीक साबित होगा जब तक सीमांत लागत (MC) वक्र सीमांत संप्राप्ति वक्र के ऊपर स्थित होगा और फर्म अपने उत्पादन में कमी को जारी रखेगी। एक बार उत्पादन स्तर के q0 पर पहुँचने पर सीमांत लागत (MC) और सीमांत संप्राप्ति (MR) के मूल्य समान हो जाएँगे और फर्म अपने उत्पादन में कमी को रोक देगी।
वार्य रूप से उत्पादन स्तर पर पहुँचती है, इसलिए इस स्तर को उत्पादन का संतुलन स्तर कहते हैं। चूंकि उत्पादन के उस संतुलन स्तर पर सीमांत संप्राप्ति (MR) सीमांत लागत के बराबर होती है तथा सीमांत लागत (MC) वक्र सीमांत संप्राप्ति वक्र को नीचे से काट रही है और इस बिंदु पर एकाधिकार फर्म की संतुलन की शर्ते पूरी हो रही हैं।
q0 उत्पादन के स्तर पर औसत लागत dq0 है। चूंकि कुल लागत, औसत लागत और उत्पादित मात्रा q0 के गुणनफल के बराबर होती है, इसलिए इसे आयंत Oq0dc के द्वारा दर्शाया गया है।
रेखाचित्र में कीमत बिंदु a द्वारा दर्शायी गई है जहाँ q0 से शुरू होकर उदग्र रेखा बाजार माँग वक्र D से मिलती है।। इससे aq0 की ऊँचाई द्वारा दर्शाई गई कीमत प्राप्त होती है। चूंकि फर्म द्वारा प्राप्त कीमत उत्पादन की प्रति इकाई संप्राप्ति होती है, अतः यह फर्म के लिए औसत संप्राप्ति है। कुल संप्राप्ति, औसत संप्राप्ति और उत्पादन q0 के स्तर का गुणनफल होती है, इसलिए इसे आयत Oq0ab के क्षेत्रफल के रूप में दर्शाया गया है। आरेख से स्पष्ट है कि आयत Oq0ab का क्षेत्रफल आयत Oq0dc के क्षेत्रफल से बड़ा है अर्थात् कुल संप्राप्ति कुल लागत से अधिक है। आयत cdab का क्षेत्रफल इनके बीच का अंतर है अतः लाभ = कुल संप्राप्ति – कुल लागत को cdab के क्षेत्रफल से प्रदर्शित किया जा सकता है।
प्रश्न 4.
शून्य लागत की स्थिति में एक एकाधिकारी फर्म के संतुलन स्थिति को रेखाचित्र की सहायता से सुस्पष्ट कीजिए।
उत्तर:
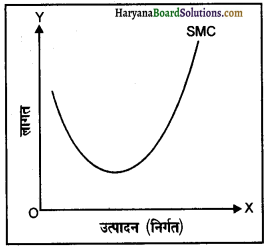
शून्य लागत की स्थिति में एकाधिकार फर्म का संतुलन कभी-कभी एक एकाधिकार फर्म की वस्तु की उत्पादन लागत शून्य होती है, क्योंकि उसे अपने उत्पाद के लिए कोई कीमत चुकानी नहीं पड़ती। ऐसी स्थिति में भी एक फर्म का संतुलन उस बिंदु पर होगा, जहाँ MC = MR है और चूँकि हमने माना है कि MC = 0 है तो संतुलन की शर्त होगी (MR = MC = 0)। हम यह भी जान चुके हैं कि जब MR = 0 होता है तो TR अधिकतम होता है। एक फर्म की संतुलन स्थिति को हम निम्नलिखित उदाहरण व संलग्न रेखाचित्र की सहायता से स्पष्ट कर सकते हैं
उदाहरण (Example) मान लीजिए कि कोई गाँव अन्य गाँवों से काफी दूरी पर स्थित है। इस गाँव में एक ही कुआँ है जिसमें पानी उपलब्ध होता है। सभी निवासी जल की आवश्यकता के लिए पूर्ण रूप से इसी कुएँ पर निर्भर हैं। कुएँ का स्वामी एक ऐसा व्यक्ति है जो अन्य लोगों को कुएँ से जल निकालने के लिए रोकने में समर्थ है सिवाय इसके कि कोई जल का क्रय करे। इस कुएँ से जल का क्रय करने वाले स्वयं ही जल निकालते हैं। हम इस एकाधिकार की स्थिति का विश्लेषण बिक्री जहाँ लागत शून्य है इस जल की मात्रा और उसकी कीमत जिस पर बेची जाती है, का निर्धारण करने के लिए करेंगे।
रेखाचित्र में कुल संप्राप्ति (TR), औसत संप्राप्ति (AR) और सीमांत संप्राप्ति (MR) वक्रों को दर्शाया गया है। फर्म का लाभ कुल संप्राप्ति – कुल लागत के बराबर होता है अर्थात
π = TR – TC.
रेखाचित्र से स्पष्ट है कि जब कुल उत्पादन OQ है, तो कुल लागत शून्य है। चूंकि इस स्थिति में कुल लागत शून्य है, जब कुल संप्राप्ति सर्वाधिक है। लाभ सर्वाधिक है तो जैसा कि हमने पहले देखा है कि यह स्थिति तब होती है, जब उत्पादन मात्रा OQ इकाइयाँ हों। यह स्तर तब प्राप्त होता है जब MR शून्य के बराबर होती है। लाभ का परिणाम ‘a’ से समस्तरीय अक्ष तक के उदग्र रेखा की लंबाई के द्वारा स्पष्ट है।
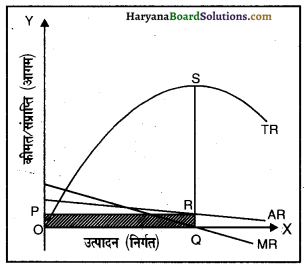
जिस कीमत पर उत्पाद की इस मात्रा का विक्रय होगा जिसे उपभोक्ता समग्र रूप से भुगतान करने को तैयार होंगे। इसे बाजार माँग वक्र D द्वारा दिया गया है। OQ इकाई के उत्पादन के स्तर पर कीमत P रु० है। चूँकि एकाधिकार फर्म के लिए बाजार माँग वक्र ही औसत संप्राप्ति (AR) वक्र है, इसलिए फर्म के द्वारा प्राप्त औसत संप्राप्ति P है। उत्पादन (निर्गत) Q MR कुल संप्राप्ति को औसत संप्राप्ति और बिक्री मात्रा के गुणनफल अर्थात् Px OQ इकाइयाँ = OQRP के द्वारा दिखाया गया है। यह छायांकित आयत के द्वारा चित्रित किया गया है।
पूर्ण प्रतिस्पर्धा से तुलना-उपरोक्त स्थिति में एकाधिकारी फर्म को अधिसामान्य लाभ प्राप्त होंगे। अब यदि हम यह मान लें कि बाजार में पूर्ण प्रतिस्पर्धा की स्थिति है और गाँव में जल के अनगिनत कुएँ हैं, जिनके स्वामी भी अलग-अलग हैं, तब उनमें परस्पर प्रतिस्पर्धा होगी। दूसरे स्वामी कीमत को कम करेंगे और कीमत असीमित रूप से नीचे की ओर गिरेगी और तब तक गिरेगी जब तक शन्य न हो जाए और लाभ भी शून्य न हो जाए। अतः इस प्रकार पूर्ण प्रतिस्पर्धा लाभ के कारण कम कीमत पर अधिक मात्रा की बिक्री होती है तथा लाभ AR सामान्य (शून्य) होते हैं।
प्रश्न 5.
एकाधिकारी प्रतिस्पर्धा में फर्म के अल्पकालीन संतुलन की स्थिति समझाइए। MC, MR विधि का प्रयोग करें।
उत्तर:
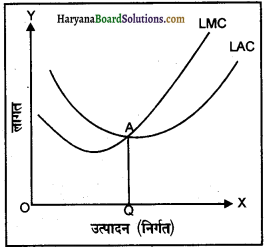
अल्पकालीन संतुलन (Short Run Equilibrium) अल्पकाल समय की वह अवधि है, जिसमें माँग के बढ़ने पर उत्पादन उत्पादन (निर्गत) को केवल वर्तमान क्षमता (Existing Capacity) तक ही बढ़ाया जा सकता है। उत्पादन के स्थिर साधनों; जैसे मशीनरी, प्लांट आदि में परिवर्तन नहीं किया जा सकता। इस समय अवधि में एकाधिकारी प्रतिस्पर्धा फर्म का संतुलन तो उसी बिंदु पर निर्धारित होता है, जिस पर MC = MR हो तथा MC, MR को नीचे से काटे, परंतु संतुलन की अवस्था में फर्म को उत्पादन करने में (i) असामान्य लाभ, (ii) सामान्य लाभ या (iii) हानि उठानी पड़ सकती है। इनका विवरण दिए गए रेखाचित्रों की सहायता से किया जा सकता है।
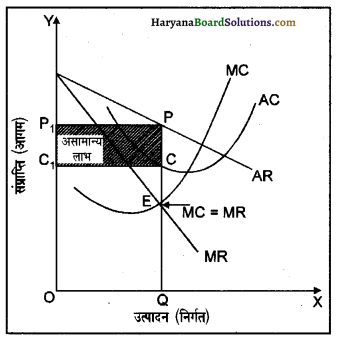
1. असामान्य लाभ-एकाधिकारी प्रतिस्पर्धा में फर्म को असामान्य लाभ (Supermormal Profit) उस समय होते हैं, जब फर्म की औसत संप्राप्ति (आगम) (AR) औसत लागत से अधिक होती है (AR > AC)। संलग्न रेखाचित्र में संतुलन बिंदु E है, जिस पर MC = MR है तथा MC वक्र, MR वक्र को नीचे से काट रहा है। इस स्थिति में संतुलन उत्पादन OQ है तथा संतुलन कीमत QP = OP1 है। OQ उत्पादन की प्रति इकाई कीमत (QP) औसत लागत (OC) से अधिक है। इसलिए फर्म को PP1C1C छाया वाले भाग के बराबर असामान्य लाभ प्राप्त होते हैं।
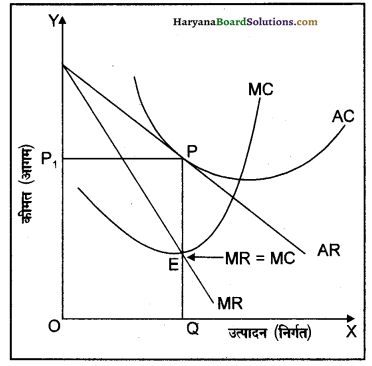
2. सामान्य लाभ-अल्पकाल में एकाधिकारी प्रतिस्पर्धा में फर्म को सामान्य लाभ उस समय प्राप्त होते हैं, जब औसत संप्राप्ति (आगम) (AR) तथा औसत लागत (AC) एक-दूसरे के बराबर होती है। (AR = AC)। संलग्न रेखाचित्र में संतुलन बिंदु .E है, जिस पर MC = MR है तथा MC वक्र, MR वक्र को नीचे से काट रहा है। अतः संतुलन उत्पादन OQ है तथा संतुलन कीमत qP = OP1 निर्धारित होती है। OQ संतुलन उत्पादन की औसत संप्राप्ति (AR) तथा औसत लागत (AC) बराबर है (OP = QP1)। अतः फर्म को केवल सामान्य लाभ (Normal Profit) प्राप्त हो रहे हैं।
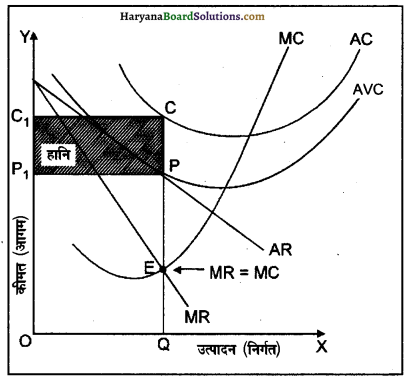
3. न्यूनतम हानि-अल्पकाल में एकाधिकारी प्रतिस्पर्धा में उत्पादन (निर्गत) काम कर रही फर्म को हानि भी हो सकती है। हानि उस समय होती है जब फर्म की औसत संप्राप्ति (AR) औसत (AC) से कम होती है अर्थात् जब AR1 निर्धारित होती है। औसत लागत QC है, जो कि कीमत अथवा औसत संप्राप्ति से अधिक है। इसलिए फर्म को PC प्रति इकाई हानि हो रही है, परंतु संतुलन उत्पादन की कीमत औसत परिवर्ती लागत (AVC) के बराबर है, क्योंकि बिंदु P पर AR वक्र AVC वक्र को छू रहा है। इस स्थिति में उत्पादन (निर्गत) x फर्म को कुल हानि CC1P1P के बराबर हो रही है, जो कि बँधी लागत के बराबर है, इसलिए P बिंदु उत्पादन बंद बिंदु (Shut-down Point) है।
प्रश्न 6.
अल्पाधिकार क्या है? अल्पाधिकार में कीमत निर्धारण की समस्या की संक्षेप में व्याख्या कीजिए।
उत्तर:
अल्पाधिकार (Oligopoly) से अभिप्राय बाजार की उस स्थिति से है, जब उद्योग में समरूप वस्तु का उत्पादन करने वाली अथवा निकट स्थानापन्न वस्तुओं का उत्पादन करने वाली फर्मों की संख्या अल्प (3, 4, 5……) परंतु बहुत अधिक नहीं होती।
अल्पाधिकार में कीमत निर्धारण की समस्याएँ (Problems of Price Determination Under Oligopoly)-अल्पाधिकार में कीमत तथा उत्पादन निर्धारण की समस्या वास्तव में एक गंभीर समस्या है। इस समस्या का समाधान सरल व निश्चित नहीं है।
अल्पाधिकार में कीमत तथा उत्पादन निर्धारण की समस्या से सम्बन्धित निम्नलिखित पहलू महत्त्वपूर्ण हैं-
1. एक सामान्य सिद्धांत की रचना कठिन-अल्पाधिकार विभिन्न प्रकार की बाजार स्थितियाँ हो सकती हैं। अल्पाधिकार की गैर-लचीली अवस्था (Tight Oligopoly) भी हो सकती है, जिसमें दो या तीन फर्मे सारे बाजार को नियंत्रित करती हैं। लचीली अवस्था (Loose Oligopoly) भी हो सकती है, जिसमें छह या सात फर्मे बाजार के अधिक भाग को नियंत्रित करती हैं। इसके अंतर्गत वस्तु-विभेदीकरण (Product Differentiation) अथवा समरूप उत्पाद (Homogeneous Product) भी पाए जा सकते हैं। इसमें फर्मों का गठबंधन. (Collusion) अथवा गैर-गठबंधन (Non-Collusion) भी हो सकता है। इसलिए अर्थशास्त्र में ऐसा कोई सर्वमान्य सिद्धांत नहीं है, जो सभी प्रकार की अल्पाधिकार स्थितियों में कीमत तथा उत्पादन निर्धारण की व्याख्या कर सके।
2. अल्पाधिकार में माँग वक्र का अनिश्चित होना अल्पाधिकार में कीमत तथा उत्पादन के अनिर्धारण का एक अन्य कारण माँग का अनिर्धारित होना है। अल्पाधिकार में एक फर्म के निर्णय दूसरी फर्मों के निर्णयों पर निर्भर करते हैं। इसलिए अल्पाधिकारी फर्म की माँग वक्र का निर्धारण संभव नहीं होता, क्योंकि प्रतिद्वन्द्वियों की क्रियाओं के फलस्वरूप उसका खिसकाव होता रहता है। अतः प्रतिद्वन्द्रियों की क्रियाएँ तथा प्रतिक्रियाएँ अल्पाधिकारी माँग वक्र को अनिर्धारित बना देती हैं।
3. अल्पाधिकारी फर्म का उद्देश्य केवल अधिकतम लाभ प्राप्त करना ही नहीं होता-अल्पाधिकारी का उद्देश्य केवल लाभों को अधिकतम करना नहीं होता। चूंकि पूर्ण प्रतिस्पर्धा तथा एकाधिकार की स्थिति में फर्मों का उद्देश्य लाभ को अधिकतमं करना होता है। फलस्वरूप, ऐसे बाजारों में उत्पादन की कीमतें तथा मात्रा निर्धारित करना संभव हो जाता है, परंतु अल्पाधिकार में फर्मों के कई अन्य उद्देश्य जैसे बिक्री को अधिकतम करना अथवा दीर्घकाल तक उचित मात्रा में स्थायी लाभों को प्राप्त करना आदि हो सकते हैं। इन विभिन्न उद्देश्यों के कारण भी अल्पाधिकार में कीमत तथा उत्पादन मात्रा अनिर्धारित रह जाती है।
4. व्यवहार में भिन्नता अल्पाधिकार में परस्पर निर्भरता के फलस्वरूप फर्मों के व्यवहार में भिन्नता पाई जाती है। जैसे कि-
(i) एक तो यह कि फर्मे आपस में मिल-जुलकर अपने उद्देश्यों को प्राप्त करने का निर्णय कर सकती हैं अथवा दूसरी सीमा यह है कि वे जीवन-पर्यंत एक-दूसरे से लड़ते रहें। यदि वे आपस में समझौते भी करते हैं तो ये कुछ शीघ्र ही टूट जाते हैं।
(ii) दूसरा, फर्मे अपने में से एक को नेता चुनकर कीमत तथा उत्पादन निर्धारण कर सकती हैं, परंतु इस अवस्था में भी कोई ऐसा सरल समाधान नहीं है कि जिससे यह पता चले कि फर्म अपनी कीमत व उत्पादन का निर्धारण किस प्रकार से करेगी। अतः स्पष्ट है कि अल्पाधिकार में कीमत तथा उत्पादन-निर्धारण संबंधी समस्या का कोई निश्चित समाधान नहीं है। इसका कारण प्रतिस्पर्धी फर्मों की प्रतिक्रिया में अनिश्चितता है।
अतः अल्पाधिकार में, परस्पर निर्भरता के फलस्वरूप फर्मों के व्यवहार में विभिन्नता संभव होती है। प्रतिद्वन्द्वी फर्मे परस्पर सहयोग भी कर सकती हैं अथवा स्वतन्त्र रहकर प्रतिस्पर्धा भी कर सकती हैं। वे समझौते कर सकती हैं या समझौते तोड़ सकती हैं। अतएव अल्पाधिकार में फर्मों के व्यवहार संबंधी इतनी अनिश्चितताएँ होती हैं जिस कारण से उनके बारे में कोई स्पष्ट निर्णय नहीं लिया जा सकता। कुछ अर्थशास्त्रियों के अनुसार, अल्पाधिकारियों में प्रतिस्पर्धा की तुलना ‘ताश के खेल’ (Playing Cards) से की जा सकती है। जिस प्रकार ताश के खेल का परिणाम अनिश्चित होता है, उसी प्रकार अल्पाधिकार में उत्पादन की कीमत तथा मात्रा निर्धारण का कोई समाधान नहीं होता, इसलिए उन्हें अनिर्धारित कहा जाता है।
यहाँ यह भी स्पष्ट कर देना अनिवार्य है कि यद्यपि अल्पाधिकार में, कीमत तथा उत्पादन निर्धारण की समस्या महत्त्वपूर्ण है। इन बाधाओं के होते हुए भी अल्पाधिकार की स्थिति में कीमत निर्धारण की दो मुख्य विशेषताएँ हैं-
1. अल्पाधिकार में कीमतें दृढ़ होती हैं इस स्थिति में बाजार की अन्य अवस्थाओं; जैसे पूर्ण प्रतिस्पर्धा, एकाधिकारी प्रतिस्पर्धा की तुलना में कीमतों में बहुत कम परिवर्तन होता है।
2. यदि अल्पाधिकार की स्थिति में, कीमतों में परिवर्तन होता है तो सभी फर्मों की कीमतों में परिवर्तन होगा, जिससे एक प्रकार का कीमत युद्ध (Price War) सा छिड़ जाता है। यह विशेषता भी अन्य बाजारों में नहीं पाई जाती।
इस प्रकार उपरोक्त तथ्यों के आधार पर यह कहा जा सकता है कि अल्पाधिकार में कीमत तथा उत्पादन-निर्धारण का कोई निश्चित समाधान नहीं है।
प्रश्न 7.
द्वि-अधिकार क्या है? द्वि-अधिकार में फर्म की कीमत तथा उत्पादन मात्रा निर्धारण संक्षेप में समझाइए।
उत्तर:
द्वि-अधिकार का अर्थ-जब बाज़ार में किसी वस्तु का उत्पादन या विक्रय करने वाली केवल दो फर्मे होती हैं, तो उसे द्वि-अधिकार कहते हैं।
द्वि-अधिकार के अंतर्गत कीमत तथा उत्पादन-मात्रा निर्धारण (Price and Output Determination under Duopoply) यद्यपि द्वि-अधिकार के अंतर्गत कीमत तथा उत्पादन मात्रा के निर्धारण की समस्या अत्यंत जटिल होती है तथापि द्वि-अधिकार में कीमत निर्धारण की संभावित दशाओं का विश्लेषण निम्नलिखित प्रकार किया जा सकता है-
(1) समझौता हो जाने पर यदि दोनों विक्रेता आपस में समझौता करके बाज़ारों का बँटवारा कर लेते हैं तो दोनों विक्रेता अपने-अपने बाज़ारों में एकाधिकारी के समान कीमत निश्चित करने की स्थिति में हो जाते हैं। बाज़ारों का बँटवारा हो जाने के पश्चात् दोनों विक्रेता स्वतंत्र रूप से अपने-अपने क्षेत्रों में लागत-स्थितियों तथा माँग के अनुसार समायोजन करके कीमत निश्चित कर लेते हैं। यदि दोनों एकाधिकारियों की लागत-स्थितियाँ समान हों तथा दोनों की वस्तुओं की माँग की लोच समान हो तो दोनों बाज़ारों में कीमत भी समान होगी अन्यथा उनमें अंतर होने की संभावना बनी रहेगी।
(2) प्रतिस्पर्धा की स्थिति में यदि दोनों फर्मों के बीच कोई समझौता नहीं है तो उनमें प्रतिस्पर्धा रहेगी और कीमत युद्ध (Price War) छिड़ने की संभावना रहेगी। प्रत्येक विक्रेता अपने उत्पाद की कीमत घटाकर दूसरे विक्रेता के ग्राहकों को अपनी ओर खींचने का प्रयत्न करेगा तथा यह कीमत घटाने का क्रम तब तक चलेगा जब तक कि दोनों विक्रेताओं की कीमत उनकी सीमांत लागत के बराबर नहीं हो जाती है। यदि दोनों विक्रेताओं की वस्तुएँ समरूप नहीं हैं तो दोनों की कीमत में अंतर बना रह सकता है। व्यवहार में द्वि-अधिकारी फर्मे कीमत-युद्ध से बचने के लिए मूल्य नेतृत्व और आपसी समझौते का सहारा लेती हैं। इसलिए कहा जाता है कि द्वि-अधिकार का अंतिम हल कीमत नेतृत्व एवं गुटबंदी में निहित होता है।

प्रश्न 8.
बाजार संरचना (Market Structure) का अर्थ बताते हए इसको निर्धारित करने वाले कारकों का वर्णन करें।
उत्तर:
बाज़ार संरचना का अर्थ बाज़ार संरचना से अभिप्राय उद्योग में काम कर रही फर्मों की संख्या, फर्मों के बीच प्रतियोगिता का स्वरूप और वस्तु की अपनी प्रकृति से है।
बाज़ार संरचना को निर्धारित करने वाले कारक-बाज़ार संरचना को निर्धारित करने वाले कारक निम्नलिखित हैं-
1. वस्तु के क्रेताओं और विक्रेताओं की संख्या-क्रेताओं और विक्रेताओं की अधिक संख्या होने का अर्थ यह है कि कोई भी क्रेता या विक्रेता अपने स्वतंत्र व्यवहार से बाजार कीमत को प्रभावित नहीं कर सकता। पूर्ण प्रतिस्पर्धा बाजार की यह पहली शर्त य है जिसमें प्रत्येक विक्रेता और क्रेता कुल उत्पादन का एक सूक्ष्म भाग बेचता या खरीदता है। बाज़ार में केवल एक विक्रेता होने को एकाधिकार बाज़ार कहते हैं जबकि अधिक विक्रेता होने को एकाधिकारी प्रतिस्पर्धा बाज़ार कहते हैं, क्योंकि वे अपनी वस्तु के ट्रेडमार्क व ब्रांड आदि से कीमत को प्रभावित करते हैं।
2. वस्तु की प्रकृति यदि बाज़ार में बेची जाने वाली वस्तु समरूप व मानकीकृत है अर्थात् उसमें भेद नहीं किया जा सकता तो वस्तु की कीमत एक (या समान) रहेगी। कोई भी विक्रेता ऐसी वस्तु को अधिक कीमत पर नहीं बेच सकता। यह पूर्ण प्रतिस्पर्धा बाज़ार की दूसरी शर्त या विशेषता है। यदि वस्तु; जैसे टूथपेस्ट में नाम, ब्रांड, आकृति, गुण आदि के आधार पर भेद किया जा सकता है तो फर्म अपने ब्रांड की वस्तु की कीमत अधिक वसूल कर सकती है। ऐसी स्थिति एकाधिकारी प्रतिस्पर्धा बाज़ार में पाई जाती है।
3. फर्मों का निर्बाध प्रवेश व बहिर्गमन-इससे अभिप्राय है कि फर्म को उद्योग में आने या इससे बाहर जाने की पूर्ण स्वतंत्रता है या नहीं। यदि किसी उद्योग में अधिक लाभ के आकर्षण के कारण नई फर्मों को प्रवेश करने की स्वतंत्रता है तो उस उद्योग में असामान्य लाभ समाप्त हो जाएंगे। इसी प्रकार यदि उद्योग में घाटा उठाने वाली फर्मों को उद्योग छोड़ने की पूरी छूट है तो घाटा (Loss) भी समाप्त हो जाएगा। संक्षेप में फर्मों के निर्बाध प्रवेश व बहिर्गमन से पूर्ण प्रतिस्पर्धा की स्थिति बन जाएगी। यह भी देखना होगा कि वस्तुओं और साधनों (जैसे श्रम, पूँजी उद्यम आदि) की गतिशीलता है या नहीं अर्थात् वस्तुओं को एक स्थान से दूसरे स्थान पर लाने ले जाने या साधनों को एक धंधे से दूसरे धंधे में जाने की पूरी स्वतंत्रता है या नहीं।
उपर्युक्त कारकों के आधार पर बाज़ार को प्रायः चार श्रेणियों में वर्गीकृत किया जाता है-(i) पूर्ण प्रतिस्पर्धा, (ii) एकाधिकार, (iii) एकाधिकारी प्रतिस्पर्धा और (iv) अल्पाधिकार। अंतिम तीन श्रेणियाँ अपूर्ण प्रतिस्पर्धा के रूप हैं।
प्रश्न 9.
एकाधिकार की परिभाषा दीजिए। इसकी मुख्य विशेषताएँ बताइए।
उत्तर:
एकाधिकार बाज़ार का अर्थ-एकाधिकार बाज़ार (Monopoly Market) बाज़ार की वह अवस्था है जिसमें वस्तु का केवल एक ही विक्रेता होता है तथा उसका वस्तु की पूर्ति पर पूर्ण नियंत्रण होता है। एकाधिकार उस वस्तु का उत्पादन करता है, जिसका कोई निकट स्थानापन्न नहीं होता।
एकाधिकार बाज़ार की विशेषताएँ एकाधिकार की मुख्य विशेषताएँ निम्नलिखित हैं-
1. एक विक्रेता-एकाधिकार बाज़ार में वस्तु का केवल एक ही विक्रेता होता है। अतः इस बाज़ार में फर्म तथा उद्योग का अंतर समाप्त हो जाता है।
2. निकट स्थानापन्न का न होना-एकाधिकार बाज़ार जिस वस्तु का उत्पादन या विक्रय करता है, उसका कोई निकट स्थानापन्न नहीं होता।
3. प्रवेश पर प्रतिबंध एकाधिकार बाज़ार में नई फर्मों के प्रवेश पर प्रतिबंध होता है। इसलिए एकाधिकारी का कोई प्रतियोगी नहीं होता।
4. पूर्ति पर प्रभावी नियंत्रण-वस्तु की पूर्ति पर एकाधिकारी बाज़ार का पूर्ण नियंत्रण होता है।
5. स्वतंत्र कीमत नीति-एकाधिकार बाज़ार का वस्तु की कीमत पर पूर्ण नियंत्रण होता है। वह स्वतंत्र कीमत नीति अपना सकता है। वह अपनी इच्छानुसार वस्तु की कीमत में वृद्धि या कमी कर सकता है। वह कीमत निर्धारण करने वाला होता है, न कि कीमत स्वीकार करने वाला। अतः क्रेताओं को वह कीमत देनी पड़ती है, जो एकाधिकारी तय करता है और चूँकि एकाधिकारी को वस्तु का मूल्य निर्धारण करने की पूर्ण स्वतंत्रता होती है, इसलिए उसे असामान्य लाभ प्राप्त होते हैं।
6. कीमत विभेद-एकाधिकारी अपनी वस्त की विभिन्न क्रेताओं से तथा विभिन्न बाज़ारों में विभिन्न कीमतें ले सकता है।
7. विभिन्न औसत एवं सीमांत आगम वक्र-एकाधिकार में औसत और सीमांत आगम वक्र अलग-अलग होते हैं; जैसाकि संलग्न रेखाचित्र में दिखाए गए हैं। एकाधिकार उत्पादन (निर्गत) फर्म का औसत आगम (AR) वक्र अथवा माँग-वक्र बाएँ से दाएँ नीचे की ओर झुकते हैं जो यह बताते हैं कि कम कीमत पर अधिक और अधिक कीमत पर कम वस्तु बेची जा सकती है। सीमांत आगम (MR) वक्र भी औसत आगम (AR) की तरह नीचे को ढालू होता है और औसत आगम (AR) वक्र के नीचे रहती है।
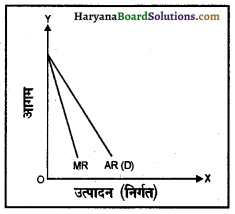
प्रश्न 10.
अल्पाधिकार में कीमत अनम्यता क्या है? इसके कारण पर प्रकाश डालें। रेखाचित्र का प्रयोग करें।
उत्तर:
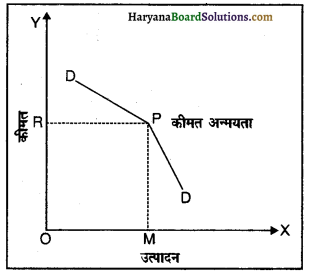
अल्पाधिकार में कीमत अनम्यता अथवा कीमत-दृढ़ता का अर्थ-जैसाकि पहले भी स्पष्ट किया जा चुका है, अल्पाधिकार में चूँकि सभी विक्रेताओं को कड़ी प्रतिस्पर्धा का सामना करना पड़ता है तथा उनके समक्ष सदैव कीमत की अनिश्चितता की स्थिति बनी रहती है, इसलिए प्रायः सभी विक्रेता कीमत के ऐसे संतोषजनक स्तर को स्वीकार कर लेते हैं जो सभी के लिए लाभदायक हो। इस कीमत-स्तर को स्वीकार करके प्रायः सभी फर्मे इस कीमत-स्तर को बनाए रखने का प्रयास करती हैं जिससे इस बाज़ार-स्थिति में कीमत में स्थिरता पाई जाती है। इसका एक कारण और भी होता है कि यदि कोई फर्म अपनी कीमत कम करती है तो सभी फर्मे अपनी कीमतें कम करती हैं, लेकिन यदि कोई फर्म कीमत में वृद्धि करती है तो अन्य फर्मों द्वारा कीमत में वृद्धि आवश्यक नहीं है। परिणामस्वरूप कीमत में दृढ़ता अथवा स्थिरता दिखाई पड़ती है तथा एक फर्म की माँग रेखा विकुंचित (Kinked) हो जाती है अर्थात् अल्पाधिकार के अंतर्गत वस्तु के माँग वक्र में एक कोना होता है जो वर्तमान मूल्य से संबंधित होता है। उसी बिंदु पर कीमतें स्थिर रहती हैं, न घटती हैं, न बढ़ती हैं। अतः अल्पाधिकार के अंतर्गत कीमतों में स्थिरता होती है।
कीमत अनम्यता/कीमत-दृढ़ता के कारण-कीमत अनम्यता के कारण निम्नलिखित हैं-
अल्पाधिकारी, चूँकि वर्तमान स्तर से कीमत घटाकर माँग में अधिक वृद्धि नहीं कर सकता और वर्तमान स्तर से कीमत बढ़ाने पर उसकी बिक्री बहुत कम हो जाने पर वह वर्तमान कीमत में परिवर्तन लाने का इच्छुक नहीं होगा। अन्य शब्दों में, चूँकि वर्तमान कीमत को बदलने में कोई लाभ नहीं है, इसलिए अल्पाधिकारी वर्तमान कीमत पर ही अपनी वस्तु को बेचता रहेगा। इस प्रकार दृढ़ कीमतों की विकुंचित माँग वक्र सिद्धांत की सहायता से व्याख्या की जा सकती है। रेखाचित्र में वर्तमान कीमत MP है जिस पर माँग वक्र DD विकुंचित है। बाज़ार में MP कीमत स्थिर या दृढ़ रहेगी, क्योंकि अल्पाधिकारी स्थिति में कोई भी उत्पादक कीमत को कम अथवा अधिक करने से लाभान्वित नहीं होगा। इस पर ध्यान देना चाहिए कि यदि वर्तमान कीमत MP कीमत अन्मयता MP औसत लागत से अधिक होगी तो उत्पादकों को जो लाभ प्राप्त होंगे, वे सामान्य लाभ से अधिक होंगे। इस स्थिति में कीमत में-
- प्रतियोगी विक्रेताओं की प्रतिक्रियाओं की अनिश्चितताओं के कारण कोई भी फर्म कीमत को कम करने को तैयार नहीं होती है।
- फर्मे यह निष्कर्ष निकाल चुकी होती हैं कि कीमत-युद्ध से कोई उत्पादन लाभ नहीं है।
- फर्मे गैर-कीमत प्रतिस्पर्धा को अधिक पसंद करने लगती हैं।
- यदि फर्मों को ऐसा आभास हो कि कीमत कम करने से पारस्परिक समझौते भंग हो जाएँगे और फर्म को कठिनाई का सामना करना पड़ेगा।
इन कारणों से कीमत में स्थिरता तथा दृढ़ता पाई जाती है तथा एक फर्म का माँग वक्र मोड़दार हो जाता है। इस प्रकार कोमेदार माँग कीमत-स्थिरता के कारणों पर प्रकाश डालती है परंतु यह स्थिर-कीमत किस प्रकार निश्चित की जाती है, इसके संबंध में कोनेदार माँग प्रकाश नहीं डालती। साथ-ही-साथ इसके द्वारा इस बात पर भी प्रकाश नहीं पड़ता कि नई कीमत पर नया कोना कैसे बनता है?

प्रश्न 11.
एकाधिकारी प्रतिस्पर्धा की परिभाषा दीजिए। इसकी मुख्य विशेषताएँ बताइए।
उत्तर:
एकाधिकारी प्रतिस्पर्धा का अर्थ एकाधिकारी प्रतिस्पर्धा (Monopolistic Competition) बाज़ार की उस अवस्था को कहते हैं जिसमें बहुत-सी फर्मे मिलती-जुलती वस्तुओं का उत्पादन व विक्रय कर रही होती हैं। ये वस्तुएँ बिल्कुल एक जैसी (Exactly Identical) तो नहीं होतीं, किंतु मिलती-जुलती (Similar) अवश्य होती हैं अर्थात् इनका प्रयोग एक-जैसा होता है तथा ये एक-दूसरे के निकट स्थानापन्न (Close Substitutes) होती हैं और इनमें ब्रांड, ट्रेडमार्क, गुण, रंग, रूप, सुगन्ध आदि के अंतर के कारण वस्तु विभेद (Product Differentiation) पाया जाता है; जैसे लक्स, हमाम, रेक्सोना, लिरिल आदि नहाने के साबुनों (Toilet Soaps) का उत्पादन करने वाली अनेक फळं एकाधिकारी प्रतिस्पर्धा की उदाहरण हैं।
संक्षेप में, एकाधिकारी प्रतिस्पर्धा बाज़ार की वह अवस्था होती है जहाँ छोटे-छोटे अनेक विक्रेता पाए जाते हैं जो विभेदीकृत परंतु निकट प्रतिस्थापन्न वस्तुएँ बेचते हैं।
एकाधिकारी प्रतिस्पर्धा की विशेषताएँ-एकाधिकारी प्रतिस्पर्धा की मुख्य विशेषताएँ निम्नलिखित हैं-
1. फर्मों की अधिक संख्या-एकाधिकारी प्रतिस्पर्धा में फर्मों की संख्या अधिक होती है। इस प्रकार विक्रेताओं में प्रतिस्पर्धा पाई जाती है।
2. वस्तु विभेद-एकाधिकारी प्रतिस्पर्धा में अनेक फर्मे मिलती-जुलती वस्तुओं का उत्पादन करती हैं। उन वस्तुओं में रंग, रूप, आकार, डिज़ाइन, पैकिंग, ब्रांड, ट्रेडमार्क, सुगंध आदि के आधार पर वस्तु विभेद (Product Variation) किया जाता है; जैसे पेप्सोडेंट, कोलगेट, फोरहन्स, क्लोज़अप आदि टूथपेस्ट। इन पदार्थों में एकरूपता तो नहीं होती, लेकिन वे एक-दूसरे के निकट स्थानापन्न (Close Substitutes) होते हैं।
3. फर्मों के निर्बाध प्रवेश और बहिर्गमन-एकाधिकारी प्रतिस्पर्धा में नई फर्मों के बाज़ार में प्रवेश करने और पुरानी फर्मों को बाज़ार छोड़ने की पूर्ण स्वतन्त्रता होती है।
4. विक्रय लागतें-एकाधिकारी प्रतिस्पर्धा बाज़ार में प्रत्येक फर्म को अपनी वस्तु का प्रचार करने के लिए विज्ञापनों पर बहुत व्यय करना पड़ता है। अतः एकाधिकारी प्रतिस्पर्धा में फर्मों में अपनी-अपनी बिक्री बढ़ाने के लिए कीमत प्रतियोगिता तो नहीं पाई जाती, बल्कि गैर-कीमत प्रतिस्पर्धा (Non-Price Competition) पाई जाती है।
5. प्रत्येक फर्म अपनी वस्तु के लिए एकाधिकारी है प्रत्येक फर्म का अपनी वस्तु पर एकाधिकार होता है अर्थात् उस नाम की वस्तु कोई अन्य फर्म नहीं बना सकती; जैसे लक्स (Lux) साबुन के उत्पादन पर हिंदुस्तान लीवर लिमिटेड का एकाधिकार है। इस बाज़ार में उपभोक्ता भी कुछ विशेष वस्तुओं के लिए अपनी-अपनी पसंद रखते हैं। उदाहरण के लिए, कुछ लोग ब्रुक ब्राड चाय अधिक पसंद करते हैं, जबकि कुछ ताज चाय। ऐसे क्रेताओं के लिए उत्पादक एकाधिकारी ही होता है।
6. उद्योग व ग्रुप में अंतर-एकाधिकारी प्रतिस्पर्धा में अनेक फर्मे एक समान वस्तुओं का उत्पादन नहीं करती, अपितु मिलती-जुलती वस्तुओं का उत्पादन करती हैं। ऐसी विभिन्न फर्मों के समूह को उद्योग न कहकर ग्रुप (Group) कहा जाता है।
7. आगम (संप्राप्ति) वक्र या माँग वक्र-एकाधिकारी प्रतिस्पर्धा में हर फर्म की अपनी कीमत नीति होती है। इसमें फर्म के औसत तथा सीमांत संप्राप्ति वक्र एकाधिकारी बाज़ार की तरह दाईं ओर नीचे को झुके हुए होते हैं, जैसाकि संलग्न रेखाचित्र में दिखाया गया है। इसका अर्थ यह है कि प्रत्येक फर्म को अधिक वस्तु बेचने के लिए कीमत कम करनी पड़ती है। फर्म का औसत संप्राप्ति (AR) वक्र ही फर्म का माँग वक्र होता है। ध्यान रहे कि एकाधिकारी प्रतिस्पर्धा में माँग वक्र पूर्ण प्रतिस्पर्धा की भाँति समस्तरीय (पूर्ण लोचदार) भी नहीं होता क्योंकि एकाधिकारी प्रतिस्पर्धा में किसी विशेष फर्म के उत्पाद के प्रति निष्ठावान होते हुए भी यदि मिलती-जुलती वस्तुओं की कीमत में अंतर अधिक हो जाए तो उपभोक्ता सस्ते ब्रांड की ओर शिफ्ट होंगे क्योंकि इस बाज़ार में वस्तुएँ निकट स्थानापन्न होती हैं। इसलिए माँग उत्पादन (निर्गत) अथवा औसत आगम वक्र एकाधिकार की तुलना में, अधिक लोचदार होता है।
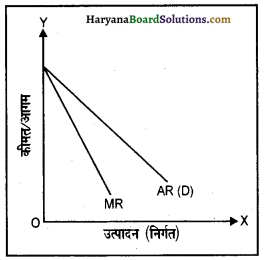
प्रश्न 12.
अल्पाधिकार (Oligopoly) परिभाषित कीजिए। इसकी मुख्य विशेषताएँ बताएँ।
उत्तर:
अल्पाधिकार का अर्थ-अपूर्ण प्रतिस्पर्धा का यह एक महत्त्वपूर्ण रूप है जहाँ चंद (कुछ) फर्मों में प्रतिस्पर्धा (प्रतियोगिता) होती बाजार में अल्प अर्थात कछ ही फर्मों का अधिकार होता है। इस प्रकार यह एकाधिकार (जिसमें केवल एक विक्रेता होता है) और एकाधिकारी प्रतिस्पर्धा (जिसमें अधिक फमें होती हैं) के बीच की स्थिति प्रकट करती है।
अल्पाधिकार की विशेषताएँ-अल्पाधिकार बाज़ार की मुख्य विशेषताएँ निम्नलिखित हैं-
1. कुछ बड़ी फर्मे फर्मों का अल्प या कम होना इसकी प्रमुख विशेषता है। अल्प होने का अर्थ यह है कि फर्म कीमत और उत्पादन की मात्रा का निर्णय लेते समय प्रतियोगी फर्मों की प्रतिक्रिया (Reaction) को ध्यान में रखती हैं। इस दृष्टि से फर्मे अंतर्निभर (Interdependent) होती हैं, क्योंकि प्रत्येक फर्म द्वारा कुल उत्पादन का एक बड़ा भाग पैदा किया व बेचा जाता है जिससे वस्तु की कीमत निश्चित रूप से प्रभावित होती है। प्रत्येक फर्म अपनी क्रिया से दूसरी फर्म को प्रभावित करती है।
2. समरूप व विभेदीकृत पदार्थ-अल्पाधिकार बाज़ार में बिकने वाले पदार्थ समरूप भी हो सकते हैं; जैसे इस्पात, उर्वरक आदि और विभेदीकृत पदार्थ भी हो सकते हैं जिन्हें ब्रांड, आकार, गुण, रंग, पैकिंग आदि के आधार पर विभेदीकृत भी किया जा सकता है; जैसे कारें, टी०वी० सेट, मोटर साइकिल, स्कूटी आदि।
3. नई फर्मों का प्रवेश कठिन-एक ही वस्तु का निर्माण करने व बेचने वाली फर्मे कुछ (जैसे पाँच या सात) ही होती हैं जो आपसी मेल-जोल व सामूहिक व्यवहार से नई फर्म का प्रवेश रोकने का भरसक प्रयास करती हैं। इसके अतिरिक्त फर्मों में परस्पर निर्भरता पाई जाती है।
4. बिक्री लागते-चाहे फर्मों की संख्या सीमित होती हो फिर भी वे अपनी वस्तु लोकप्रिय बनाने व बिक्री बढ़ाने के लिए समाचार पत्रों व रेडियो, टी.वी. आदि पर विज्ञापन, मुफ्त नमूने बाँटने व सेल्समैन आदि रखने पर व्यय करती हैं जिन्हें बिक्री लागते कहते हैं।
5. माँग वक्र की अनिश्चितता-यहाँ कीमत अधिकतर अपरिवर्तित रहती है, क्योंकि कोई भी फर्म ग्राहकों से वंचित होने के डर से कीमत नहीं बढ़ाती और न ही कीमत कम करती है कि कहीं दूसरी फर्मे कीमत ज्यादा गिराकर ग्राहक आकर्षित न कर लें। इसलिए किसी भी फर्म को यह अनुमान नहीं होता कि कीमत बढ़ाने या घटाने से माँग पर क्या प्रभाव पड़ेगा। फलस्वरूप माँग वक्र का स्वरूप अनिश्चित होता है।
प्रश्न 13.
पूर्ण प्रतियोगिता और एकाधिकार में अंतर बताइए।
उत्तर:
पूर्ण प्रतियोगिता और एकाधिकार में निम्नलिखित अंतर हैं-
| अंतर का आधार | पूर्ण प्रतियोगिता | एकाधिकार |
| 1. फर्मों की संख्या | पूर्ण प्रतियोगिता में फर्मों की संख्या बहुत अधिक होती है। | एकाधिकार में केवल एक ही फर्म बाज़ार में होती है। |
| 2. वस्तु की प्रकृति | पूर्ण प्रतियोगिता में वस्तु समरूप होती है। | एकाधिकार में वस्तुएँ समरूप अथवा विभेदीकृत हो सकती हैं। |
| 3. माँग वक्र | पूर्ण प्रतियोगिता में फर्म का माँग वक्र पूर्णतया लोचदार होता है। माँग वक्र X-अक्ष के समानांतर सीधी रेखा होती है। | एकाधिकार में फर्म का माँग वक्र लोचदार होता है। माँग वक्र ऊपर से नीचे गिरता हुआ अर्थात् ऋणात्मक ढाल वाला होता है। |
| 4. कीमत | पूर्ण प्रतियोगिता में पूरे बाज़ार में वस्तु की एक ही कीमत पाई जाती है। | एकाधिकारी फर्म विभिन्न क्रेताओं से एक-समान कीमत अथवा विभिन्न कीमतें वसूल कर सकती है। |
| 5. स्वतंत्रता | पूर्ण प्रतियोगिता में फर्मों के प्रवेश तथा बहिर्गमन की पूर्ण स्वतंत्रता होती है। | एकाधिकार में नई फर्मों के प्रवेश पर प्रतिबंध होता हैं। |
| 6. विक्रय लागतें | पूर्ण प्रतियोगिता में विक्रय लागतें नहीं होती। | एकाधिकार में मामूली-सी विक्रय लागतें हो सकती है। |
प्रश्न 14.
पूर्ण प्रतिस्पर्धा (प्रतियोगिता) और एकाधिकारी प्रतिस्पर्धा में अंतर बताइए।
उत्तर:
पूर्ण प्रतिस्पर्धा और एकाधिकारी प्रतिस्पर्धा में निम्नलिखित अंतर हैं-
| अंतर का आधार | पूर्ण प्रतिस्पर्धा | एकाधिकारी प्रतिस्पर्धा |
| 1. फर्मों की संख्या | पूर्ण प्रतिस्पर्धा में फर्मों की संख्या बहुत अधिक होती है। | एकाधिकारी प्रतिस्पर्धा में फर्मों की संख्या सीमित होती है। |
| 2. कीमत | पूर्ण प्रतिस्पर्धा बाज़ार में एक ही कीमत पाई जाती है। | एकाधिकारी प्रतिस्पर्धा में वस्तु की विभिन्न कीमतें पाई जाती हैं। |
| 3. वस्तु की प्रकृति | पूर्ण प्रतिस्पर्धा में वस्तुएँ समरूप होती हैं। अर्थात् विभिन्न फर्मों द्वारा उत्पादित वस्तुओं में कोई अंतर नहीं होता। | एकाधिकारी प्रतिस्पर्धा में विभिन्न फर्मों द्वारा उत्पादित वस्तुओं में वस्तु विभेद पाया जाता है। |
| 4. बाज़ार का ज्ञान | पूर्ण प्रतिस्पर्धा में क्रेताओं और विक्रेताओं को बाज़ार की स्थिति का ज्ञान होता है। | एकाधिकारी प्रतिस्पर्धा में क्रेताओं और विक्रेताओं को बाज़ार की स्थिति का पर्याप्त ज्ञान नहीं होता। |
| 5. मूल्य सापेक्षता | पूर्ण प्रतिस्पर्धा में माँग की पूर्ण मूल्य सापेक्षता पाई जाती है। | एकाधिकारी प्रतिस्पर्धा में माँग की मूल्य सापेक्षता कम होती है |
| 6. विक्रय लागते | पूर्ण प्रतिस्पर्धा में विक्रय लागतों का अभाव पाया जाता है। | एकाधिकारी प्रतिस्पर्धा में फर्मों की विक्रय लागते अधिक होती हैं। |
प्रश्न 15.
एकाधिकार और एकाधिकारी प्रतिस्पर्धा में अंतर बताइए।
उत्तर:
एकाधिकार और एकाधिकारी प्रतिस्पर्धा में निम्नलिखित अंतर हैं-
| अंतर का आधार | एकाधिकार | एकाधिकारी प्रतिस्पर्धा |
| 1. विक्रेताओं की संख्या | एकाधिकार में वस्तु का केवल एक विक्रेता होता है। | एकाधिकारी प्रतिस्पर्धा में वस्तुओं की संख्या अधिक होती है। |
| 2. वस्तु की किस्म | एकाधिकार में एक ही किस्म की वस्तु का विक्रय किया जाता है और उस वस्तु का कोई निकट स्थानापन्न नहीं होता। | एकाधिकारी प्रतिस्पर्धा में वस्तु विभेद के कारण वस्तु की अनेक किस्में पाई जाती हैं। |
| 3. फर्म का माँग वक्र | एकाधिकार में फर्म का माँग वक्र सामान्यतया बेलोचदार या कम लोचदार होता है। | एकाधिकारी प्रतिस्पर्धा में एक फर्म का माँग वक्र अधिक लोचदार होता है। |
| 4. कीमत | एकाधिकार में एक विक्रेता होता है जिसके कारण वस्तु की कीमत सामान्यतया ऊँची होती है। | एकाधिकारी प्रतिस्पर्धा में अनेक विक्रेता होते हैं और उनकी आपसी प्रतिस्पर्धा के कारण वस्तु की कीमत सामान्यतया कम होती है। |
| 5. लाभ | एकाधिकार में एक फर्म को असामान्य लाभ प्राप्त होते हैं। | एकाधिकारी प्रतिस्पर्धा में केवल अल्पकाल में ही फर्म को असामान्य लाभ प्राप्त होते हैं। |
| 6. फर्मों का प्रवेश | एकाधिकार में नई फर्मों के प्रवेश पर अनेक रुकावटें पाई जाती हैं। | एकाधिकारी प्रतिस्पर्धा में नई फर्मों को बाज़ार में प्रवेश की पूर्ण स्वतंत्रता होती है। |
संख्यात्मक प्रश्न
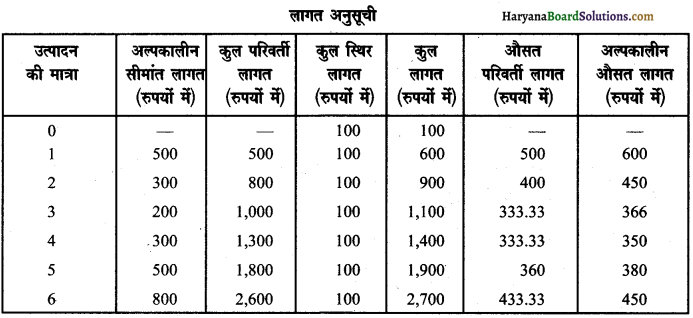
प्रश्न 1.
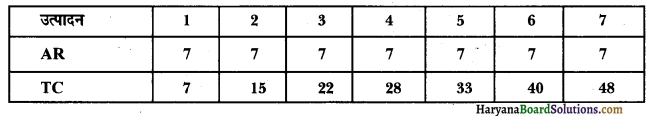
नीचे दी गई जानकारी के आधार पर संतुलन वाले उत्पादन स्तर का निर्धारण कीजिए। सीमांत लागत (MC), सीमांत आगम (MR) विधि का प्रयोग करें। सकारण उत्तर दीजिए।
हल:
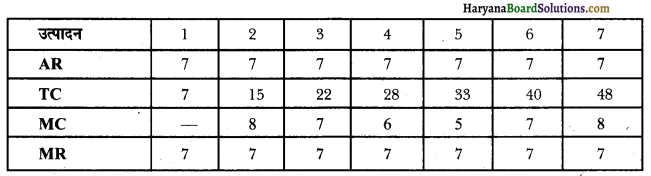
उत्पादन की संतुलन स्थिति उत्पादन की छठी इकाई में प्राप्त होती है क्योंकि उत्पादन के इस स्तर पर उत्पादन की संतुलन दशा को संतुष्ट करने वाली निम्नलिखित दो शर्ते पूरी हो जाती हैं
(i) सीमांत लागत (7 रुपए) सीमांत आगम (7 रुपए) के बराबर है।
(ii) इस स्तर पर उत्पादन के बाद MC >MR हैं अर्थात् सीमांत आगम संप्राप्ति से अधिक आती है।

प्रश्न 2.
दी गई सारणी में एक एकाधिकारी प्रतिस्पर्धी फर्म की कुल लागत एवं कुल आगम सारणी दी गई है। संतुलन उत्पादन की मात्रा ज्ञात कीजिए-
| इकाइयाँ | कुल लागत (रु०) | कुल संप्राप्ति (रु०) |
| 1 | 8 | 10 |
| 2 | 15 | 19 |
| 3 | 21 | 27 |
| 4 | 28 | 34 |
| 5 | 36 | 40 |
| 6 | 45 | 45 |
| 7 | 55 | 49 |
हल:
| इकाइयाँ | कुल लागत (रु०) | कुल संप्राप्ति (रु०) | कुल लाभ (रु०) |
| 1 | 8 | 10 | 10 – 8 = 2 |
| 2 | 15 | 19 | 19 – 15 = 4 |
| 3 | 21 | 27 | 27 – 21 = 6 |
| 4 | 28 | 34 | 34 – 28 = 6 |
| 5 | 36 | 40 | 40 – 36 = 4 |
| 6 | 45 | 45 | 45 – 45 = 0 |
| 7 | 55 | 49 | 49 – 55 = -6 |
उपर्युक्त तालिका के अनुसार एकाधिकारी फर्म का कुल लाभ = 6 प्रतिस्पर्धा फर्म के संतुलन उत्पादन की मात्रा 4 इकाइयाँ हैं चूंकि इस स्थिति में फर्म का कुल लाभ = 6 सर्वाधिक है।
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()

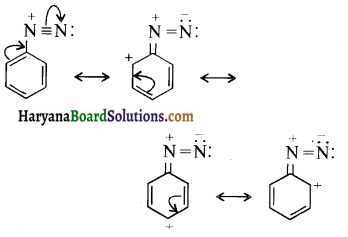
![]()





















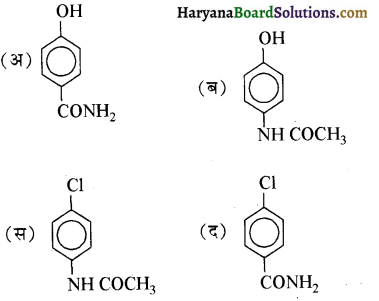
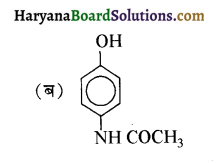

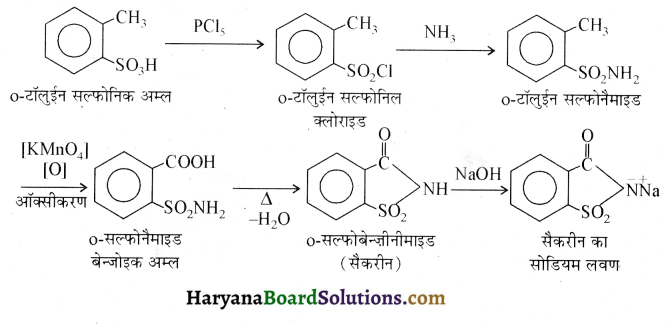

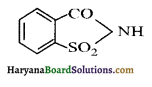


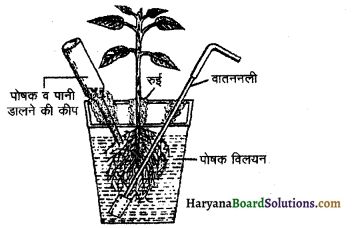
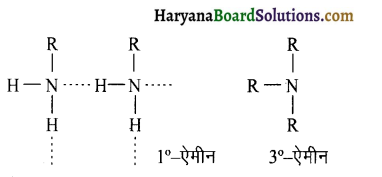
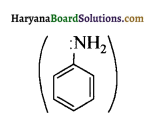 में नाइट्रोजन का एकाकी इलेक्ट्रॉन युग्म बेन्जीन वलय के साथ अनुनाद (+M प्रभाव) करता है जिससे इसके नाइट्रोजन पर इलेक्ट्रॉन घनत्व कम हो जाता है अतः इसकी इलेक्ट्रॉन देने की प्रवृत्ति कम हो जाती है इसलिए इसका क्षारीय गुण कम होता है। इसी कारण ऐनिलीन का pKb मेथिलऐमीन की तुलना में अधिक होता है क्योंकि क्षारीय गुण ∝ \(\frac{1}{\mathrm{pK}_{\mathrm{b}}} \propto \mathrm{K}_{\mathrm{b}}\) (क्षार वियोजन स्थिरांक)
में नाइट्रोजन का एकाकी इलेक्ट्रॉन युग्म बेन्जीन वलय के साथ अनुनाद (+M प्रभाव) करता है जिससे इसके नाइट्रोजन पर इलेक्ट्रॉन घनत्व कम हो जाता है अतः इसकी इलेक्ट्रॉन देने की प्रवृत्ति कम हो जाती है इसलिए इसका क्षारीय गुण कम होता है। इसी कारण ऐनिलीन का pKb मेथिलऐमीन की तुलना में अधिक होता है क्योंकि क्षारीय गुण ∝ \(\frac{1}{\mathrm{pK}_{\mathrm{b}}} \propto \mathrm{K}_{\mathrm{b}}\) (क्षार वियोजन स्थिरांक)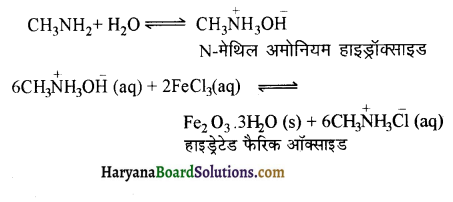
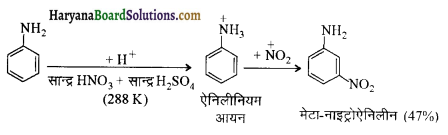
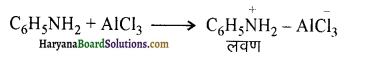
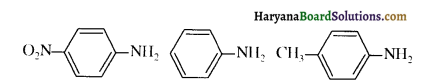
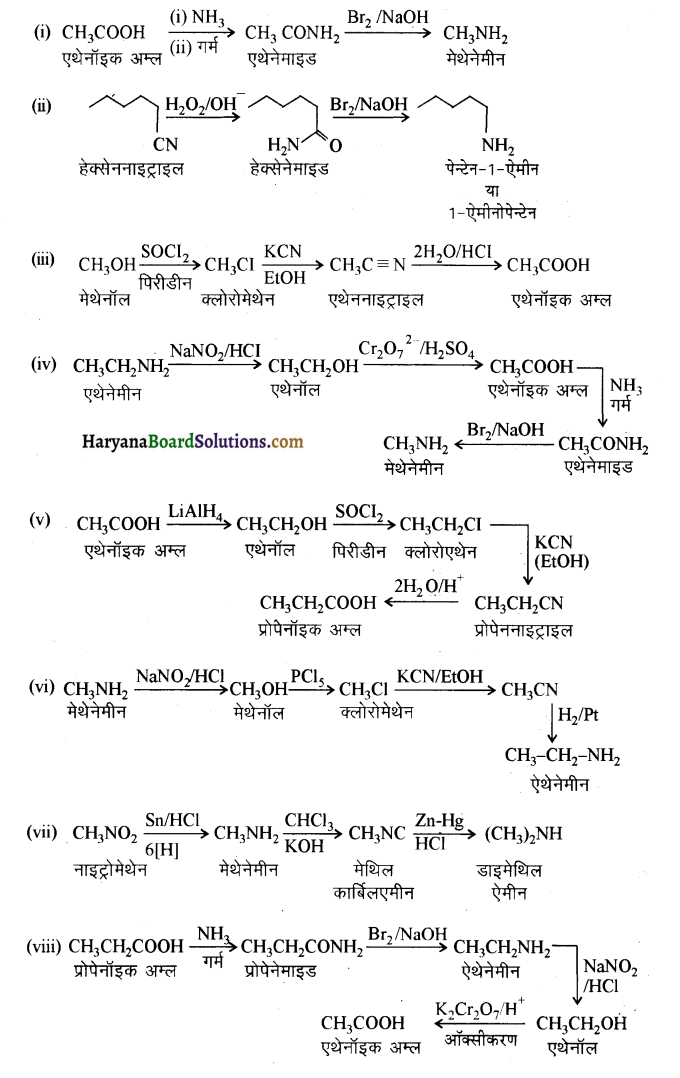

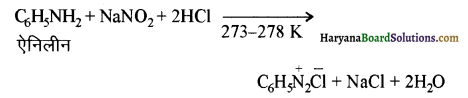

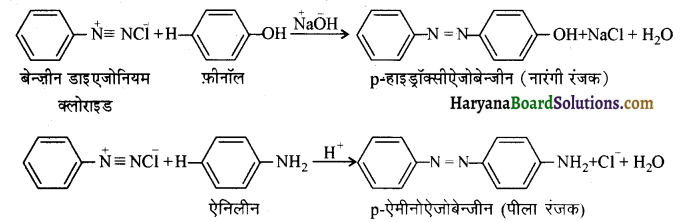
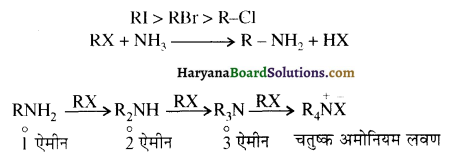
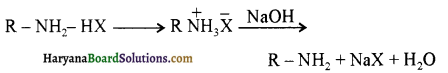
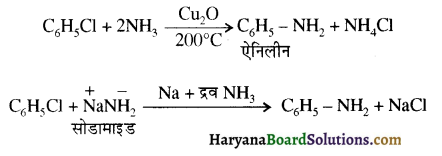
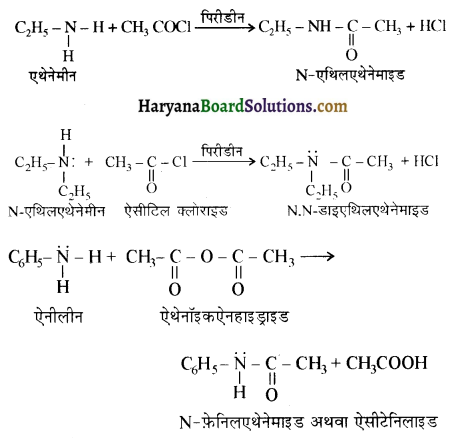
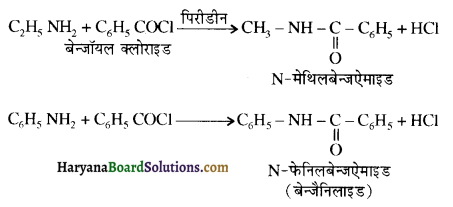
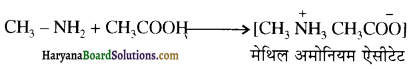
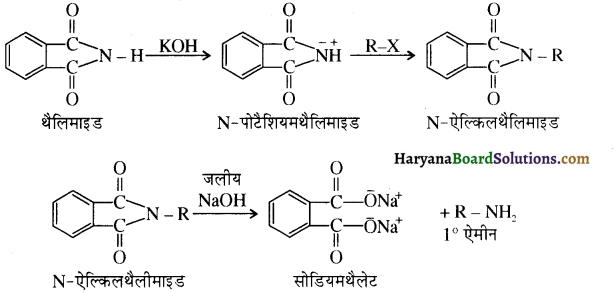
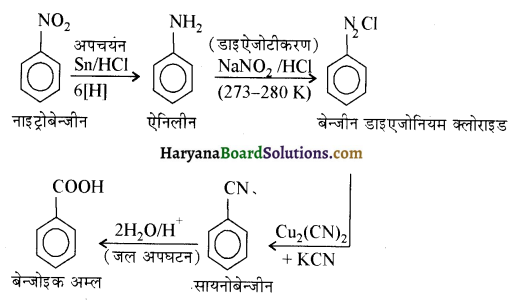
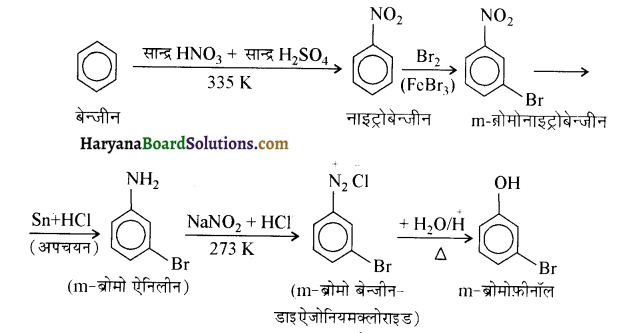
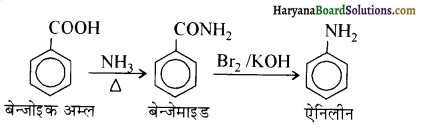
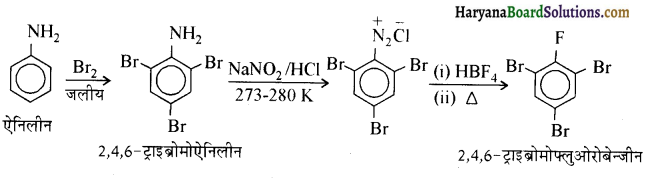
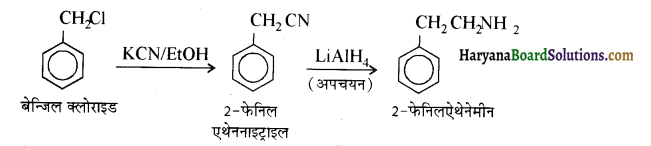
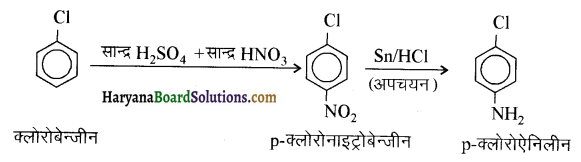
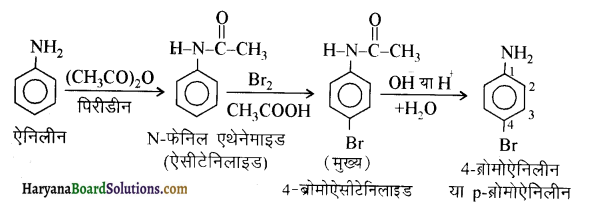
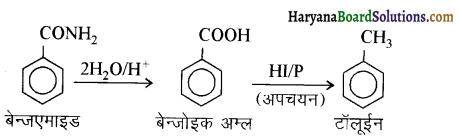
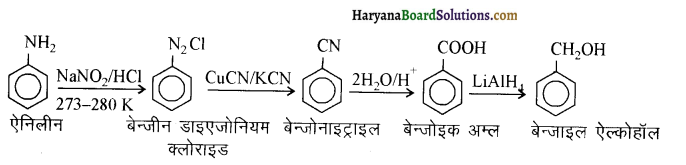
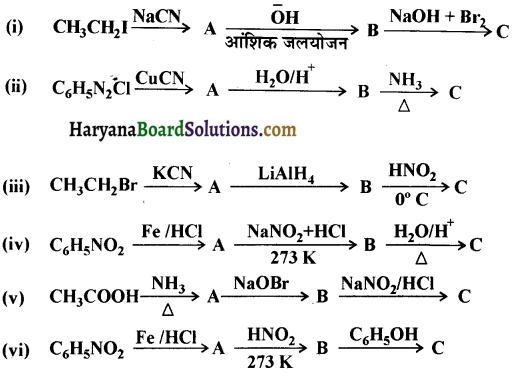
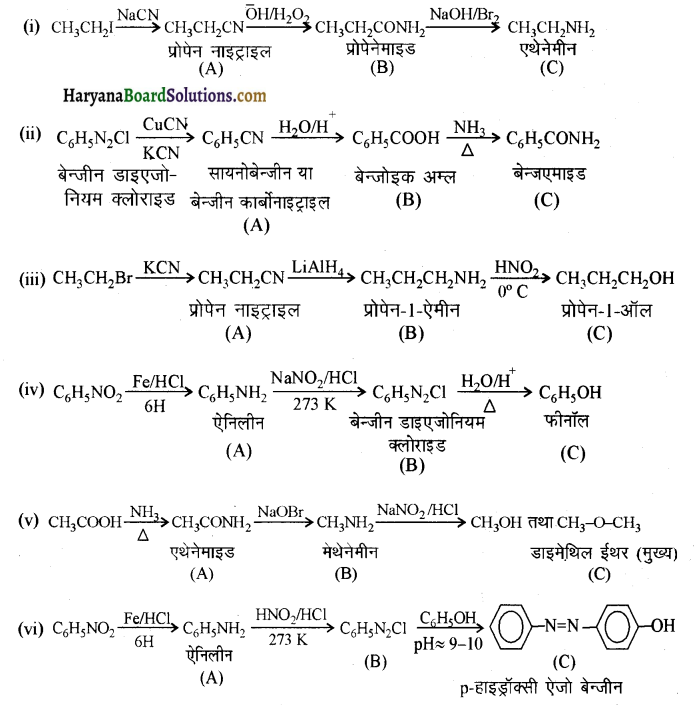
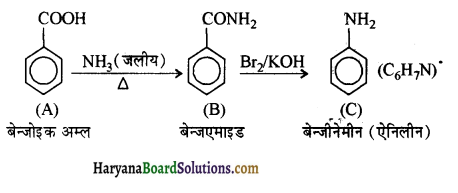
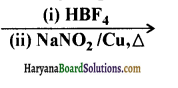
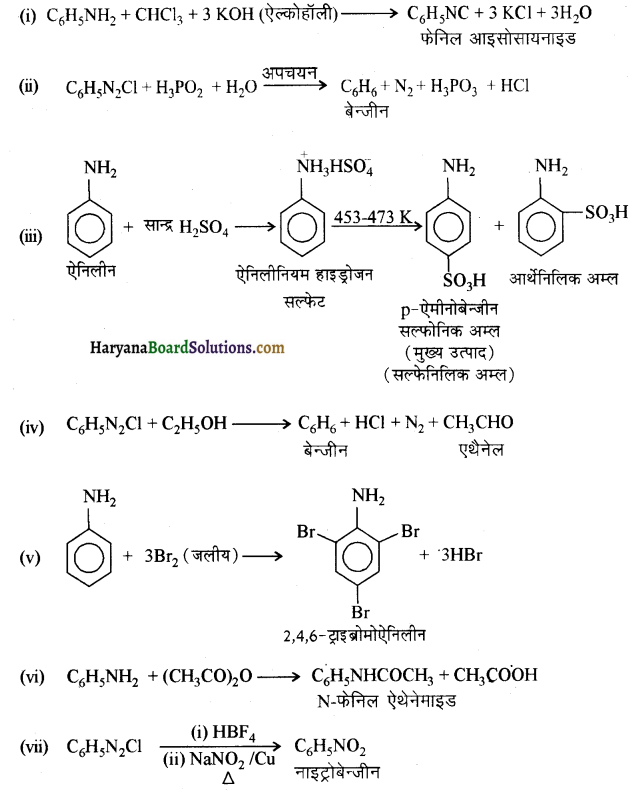
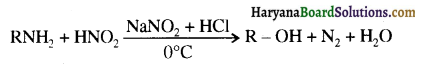
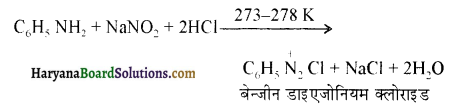
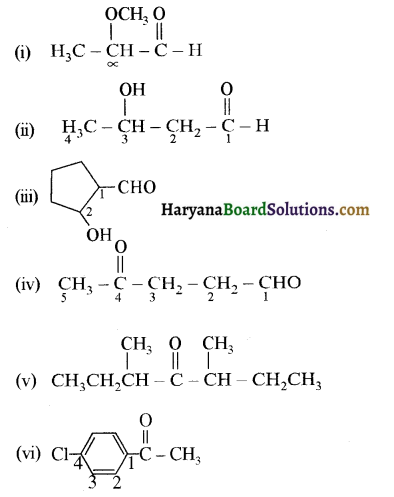
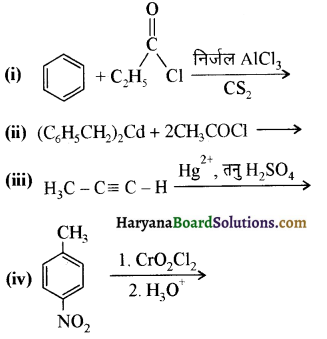
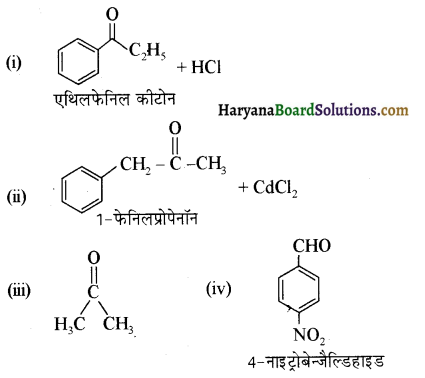
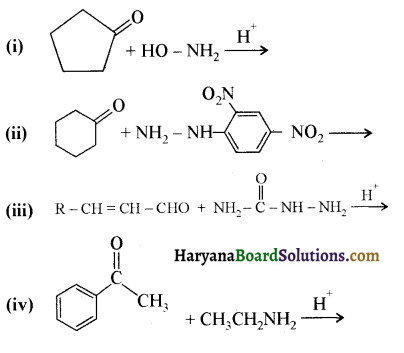
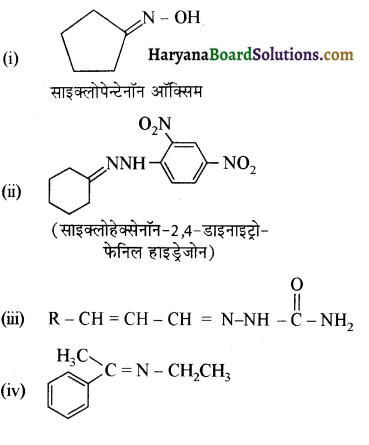
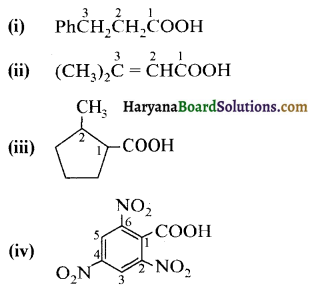
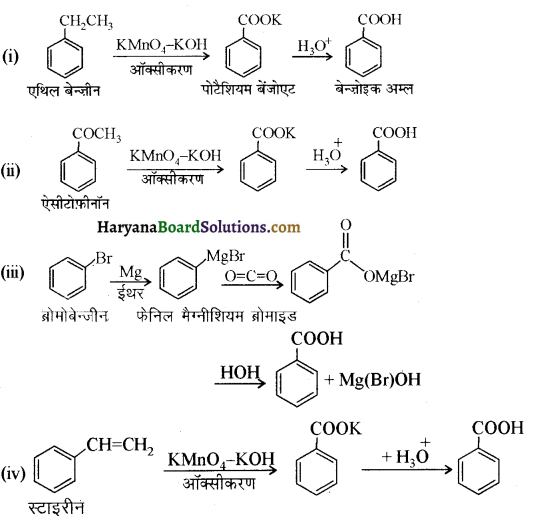
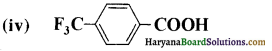










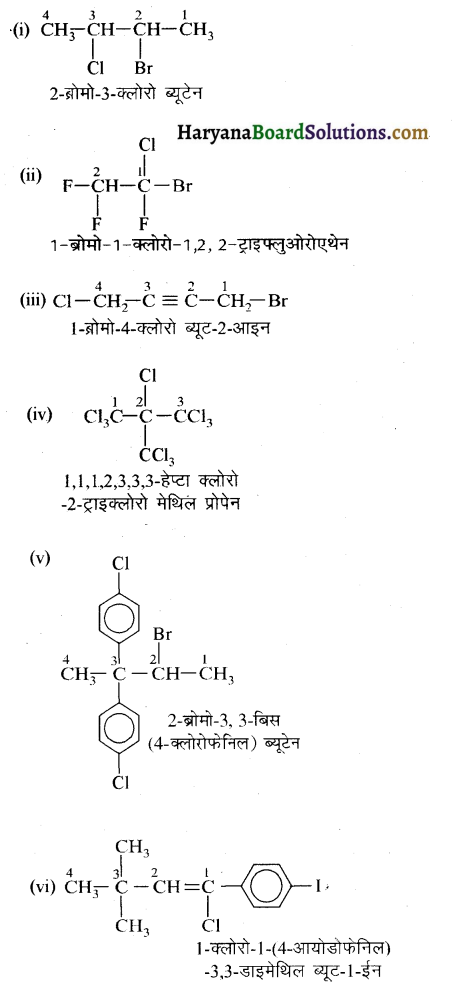
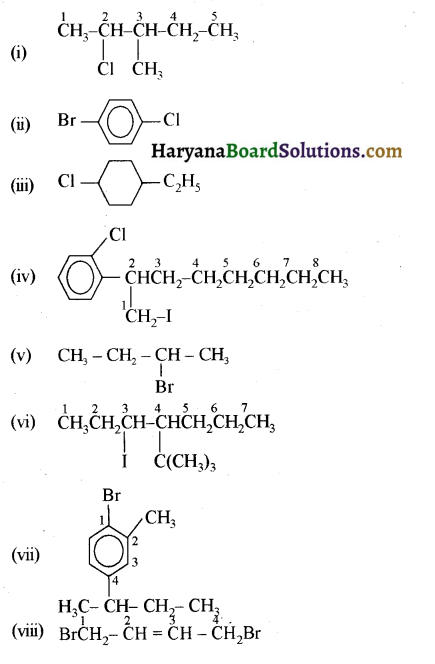
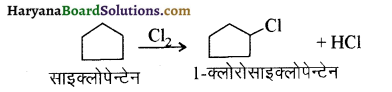
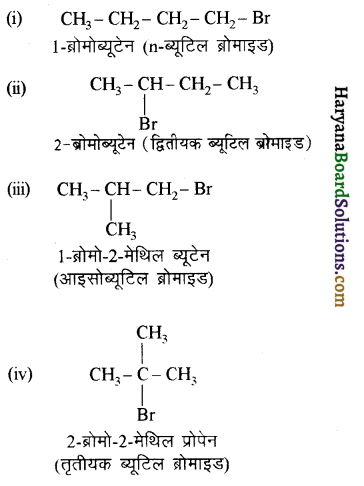
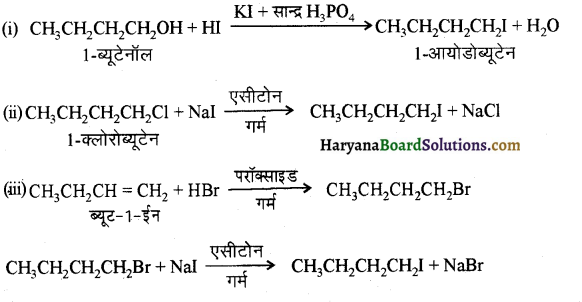
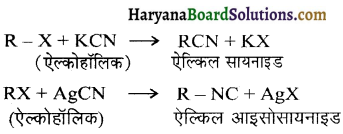
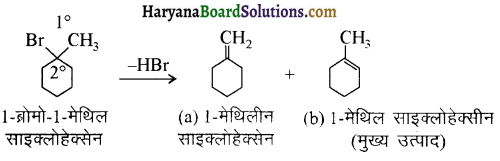
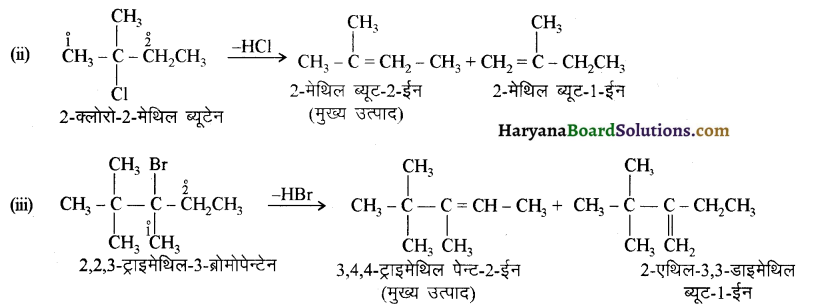
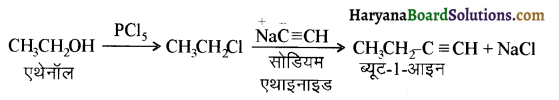
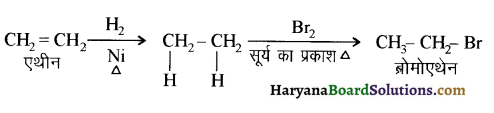

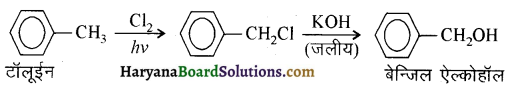
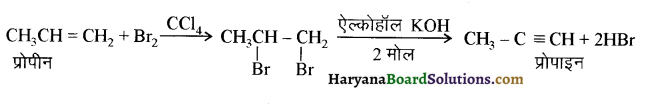
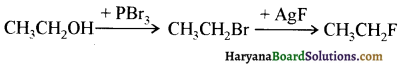
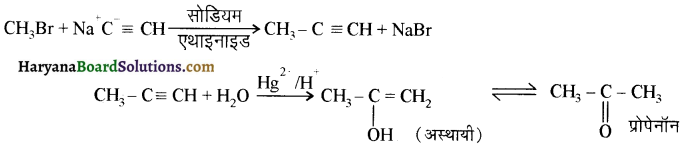
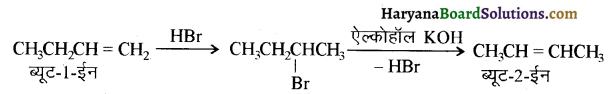
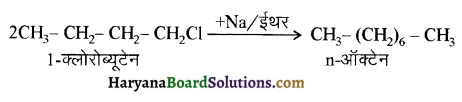
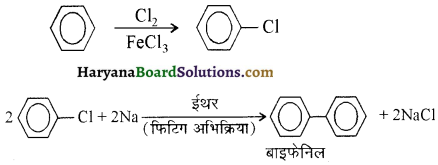
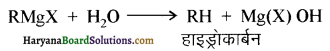
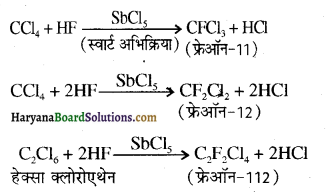
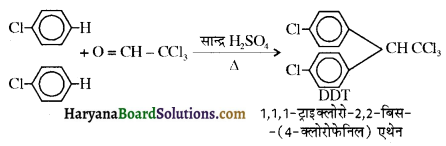
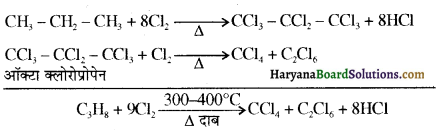
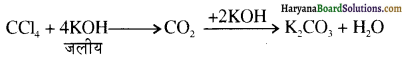
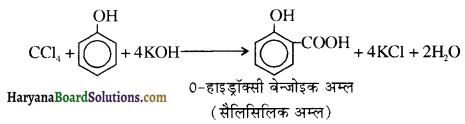
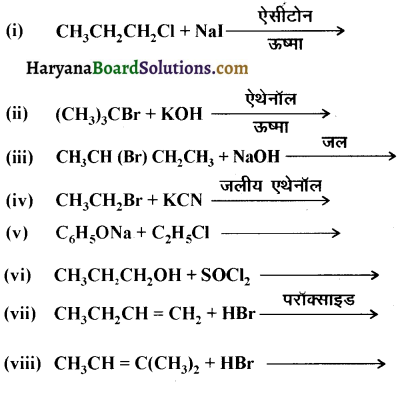
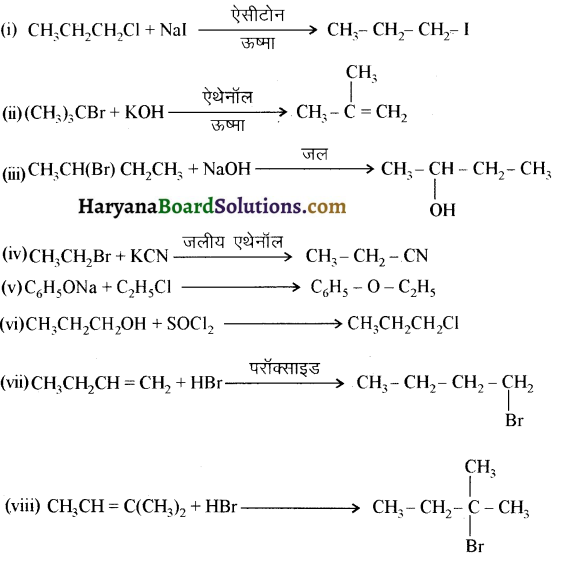

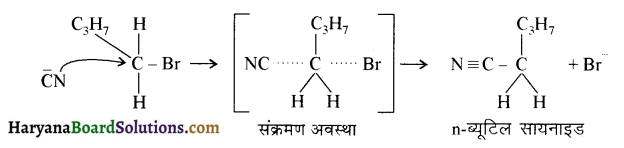

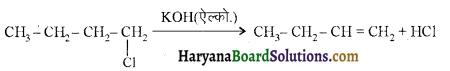
 में से
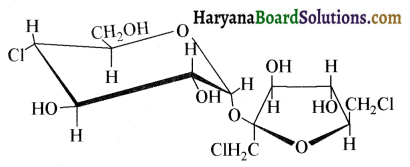
में से  का जलीय KOH से शीघ्रता से जल अपघटन होगा क्योंकि इसके जल अपघटन में बनने वाला मध्यवर्ती कार्बधनायन अधिक स्थायी होता है, क्योंकि इसमें दो बेन्जीन वलय के कारण अनुनाद अधिक होगा जबकि C6H5CH2Cl से बने कार्बधनायन में केवल एक बेन्जीनवलय ही अनुनाद में भाग लेती है।
का जलीय KOH से शीघ्रता से जल अपघटन होगा क्योंकि इसके जल अपघटन में बनने वाला मध्यवर्ती कार्बधनायन अधिक स्थायी होता है, क्योंकि इसमें दो बेन्जीन वलय के कारण अनुनाद अधिक होगा जबकि C6H5CH2Cl से बने कार्बधनायन में केवल एक बेन्जीनवलय ही अनुनाद में भाग लेती है।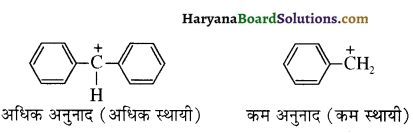
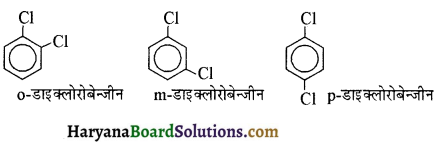
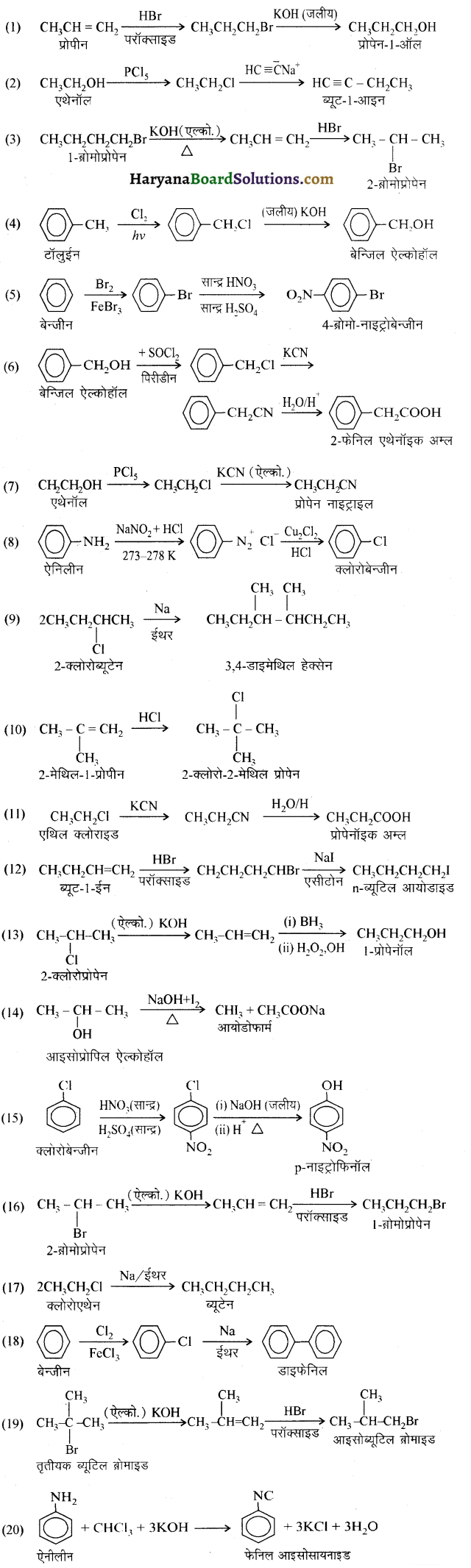
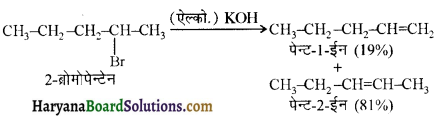
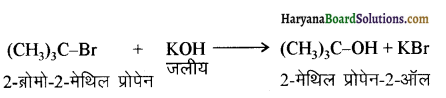
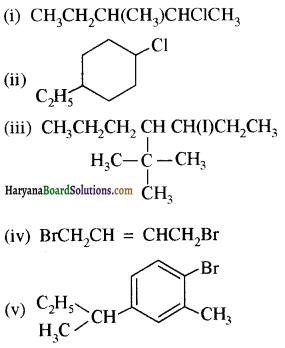
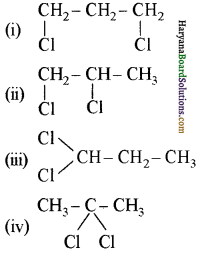
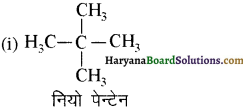
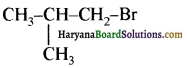 (आइसोब्यूटिल ब्रोमाइड)। प्रश्नानुसार, यौगिक ‘क’ n – ब्यूटिल ब्रोमाइड नहीं है अतः यह आइसोब्यूटिल ब्रोमाइड होगा।
(आइसोब्यूटिल ब्रोमाइड)। प्रश्नानुसार, यौगिक ‘क’ n – ब्यूटिल ब्रोमाइड नहीं है अतः यह आइसोब्यूटिल ब्रोमाइड होगा।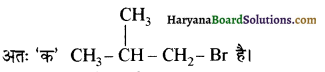



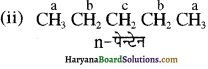
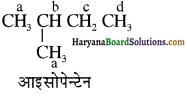
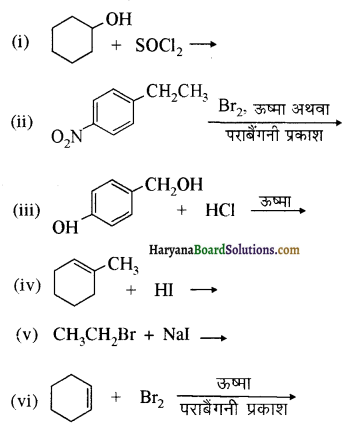
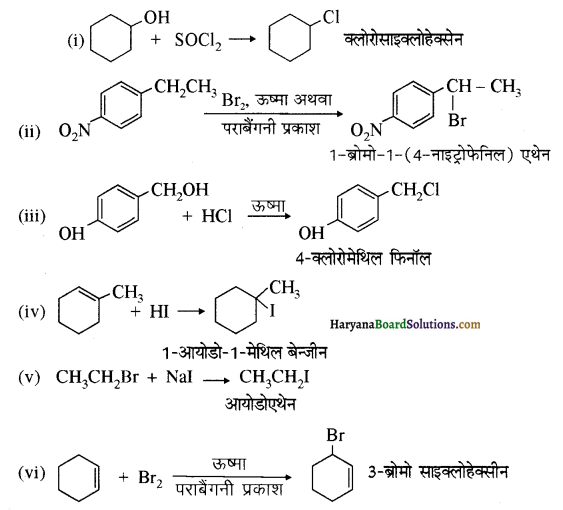

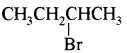
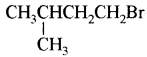




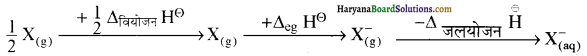

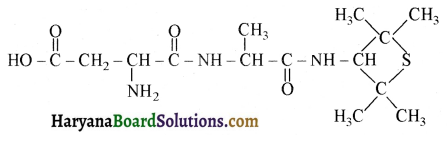
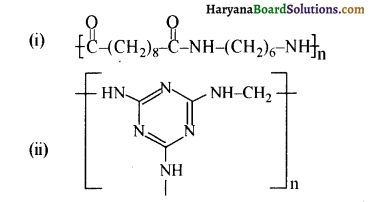
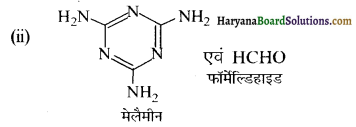
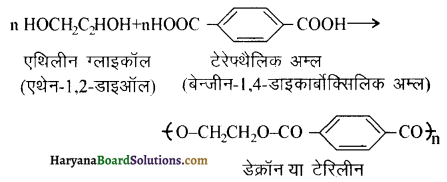
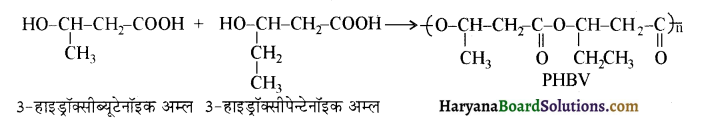
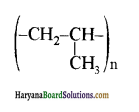 का बनना संकलन बहुलकन है जबकि हैक्सा मेथिलीन डाइऐमीन (NH2-(CH2)6NH2) तथा ऐडिपिक अम्ल (HOOC- (CH2)4COOH) के बहुलकन से नाइलॉन 6,6 का बनना संघनन बहुलकन है। इसमें H2O का विलोपन होता है।
का बनना संकलन बहुलकन है जबकि हैक्सा मेथिलीन डाइऐमीन (NH2-(CH2)6NH2) तथा ऐडिपिक अम्ल (HOOC- (CH2)4COOH) के बहुलकन से नाइलॉन 6,6 का बनना संघनन बहुलकन है। इसमें H2O का विलोपन होता है।
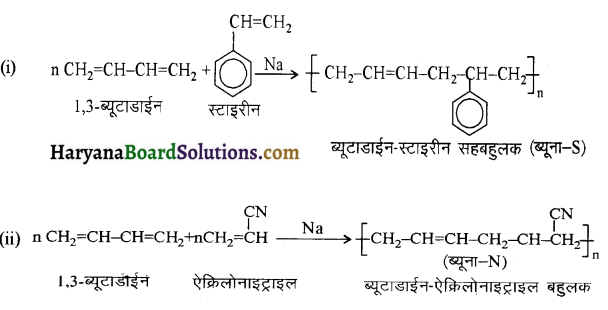
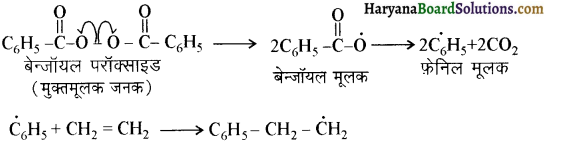
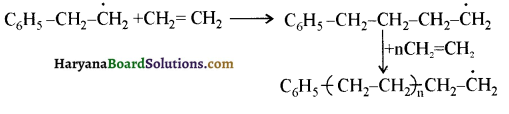
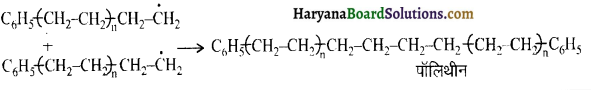
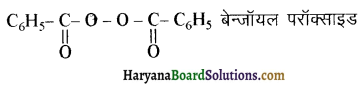
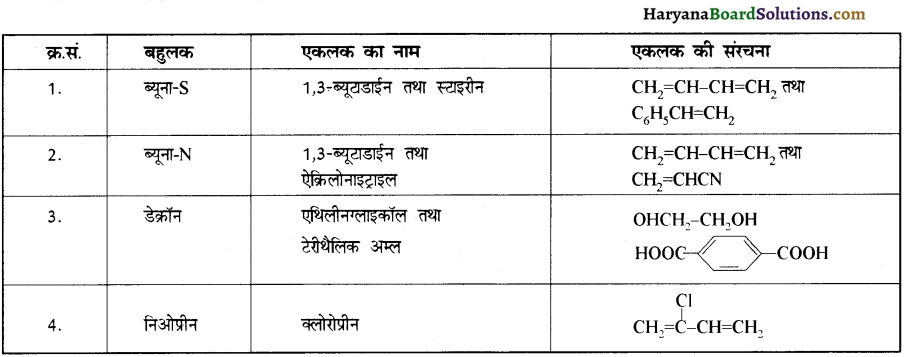
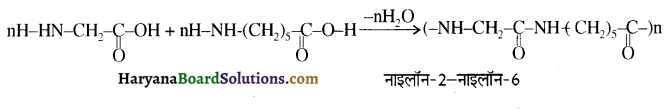
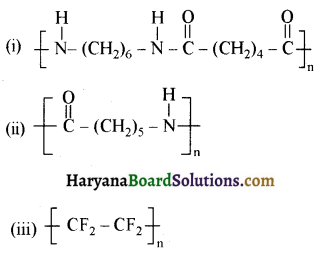
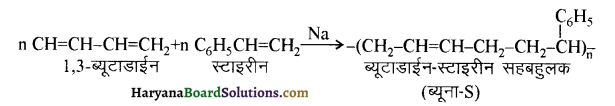
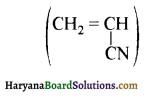 का सहबहुलक है जबकि ब्यूना-S, 1,3-ब्यूटाडाईन तथा स्टाइरीन
का सहबहुलक है जबकि ब्यूना-S, 1,3-ब्यूटाडाईन तथा स्टाइरीन 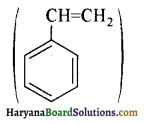 का सहबहुलक है।
का सहबहुलक है।