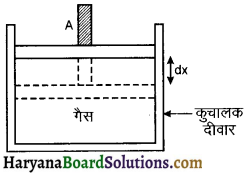
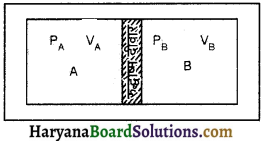
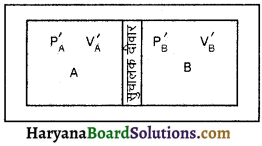
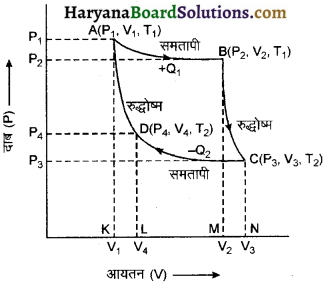
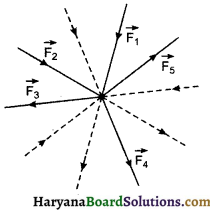
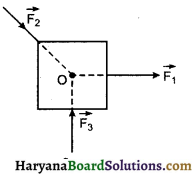
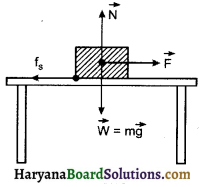
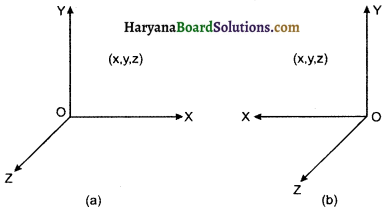
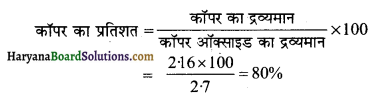
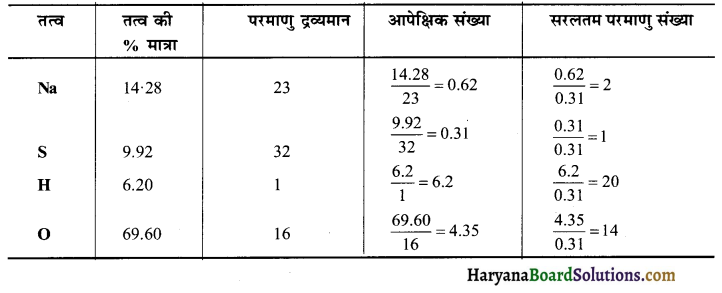
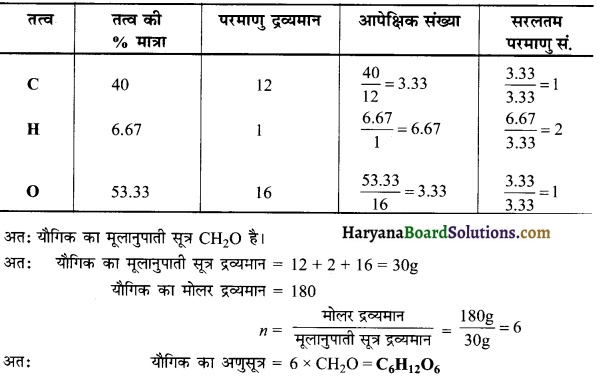
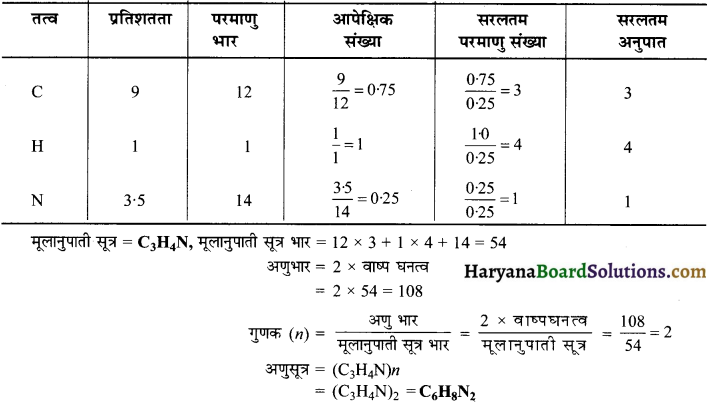
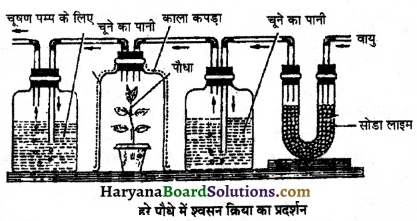
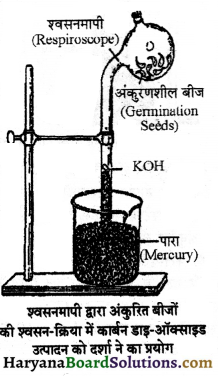
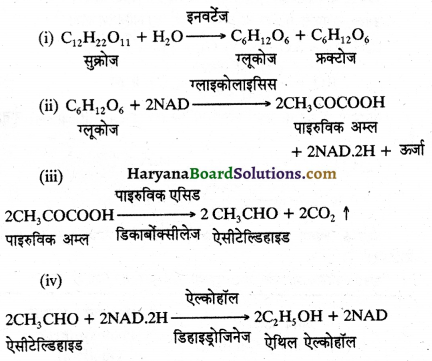
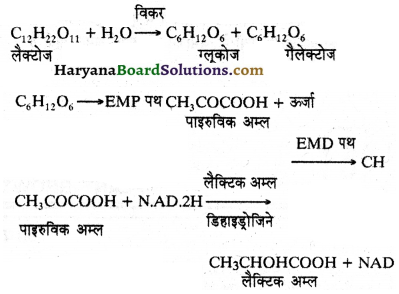
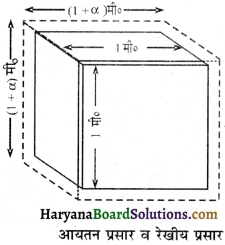
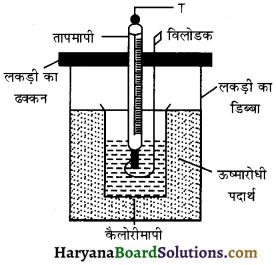
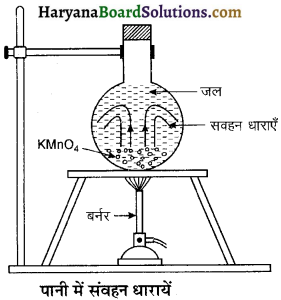
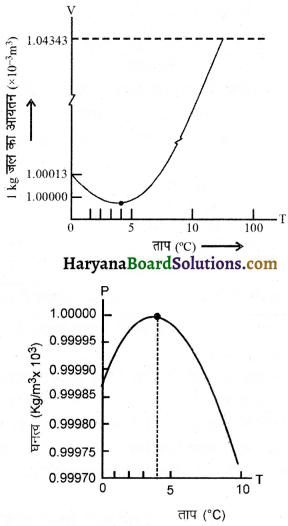
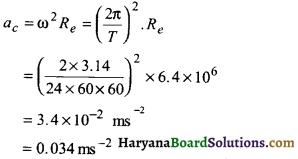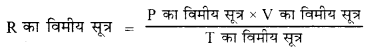HBSE 11th Class Physics Important Questions Chapter 8 गुरुत्वाकर्षण
Haryana State Board HBSE 11th Class Physics Important Questions Chapter 8 गुरुत्वाकर्षण Important Questions and Answers.
Haryana Board 11th Class Physics Important Questions Chapter 8 गुरुत्वाकर्षण
बहुविकल्पीय प्रश्न (Multiple Choice Questions)
प्रश्न 1.
कल्पना कीजिए कि हल्का ग्रह भारी तारे के परितः R त्रिज्या के वृत्तीय पथ पर गति कर रहा है तथा इसका परिक्रमण काल 7 है। भारी ग्रह व तारे के बीच गुरुत्वाकर्षण बल R-5/2 के अनुक्रमानुपाती हो तो-
(a) T² ∝ R³
(b) T² ∝ R7/2
(c) T² ∝ R3/2
(d) T² ∝ R3.75
उत्तर:
(b) T² ∝ R7/2
प्रश्न 2.
m द्रव्यमान के एक पिण्ड को पृथ्वी तल से h = R/5 ऊँचाई पर ले जाया जाता है, जहाँ R पृथ्वी की त्रिज्या है। यदि पृथ्वी तल पर गुरुत्वीय त्वरण (g) हो तो पिण्ड की स्थितिज ऊर्जा में वृद्धि होगी-
(a) mgh
(b) \(\frac{4}{5}\)mgh
(c) \(\frac{5}{6}\)mgh
(d) \(\frac{6}{7}\)migh
उत्तर:
(b) \(\frac{4}{5}\)mgh
प्रश्न 3.
सोने के दो एकसमान ठोस गोले एक-दूसरे को स्पर्श कर रहे हैं। इनके बीच गुरुत्वाकर्षण बल होगा-
(a) त्रिज्या के वर्ग के समानुपाती ।
(b) त्रिज्या के घन के समानुपाती ।
(c) त्रिज्या के चतुर्थ घात के समानुपाती ।
(d) त्रिज्या के वर्ग के व्युत्क्रमानुपाती ।
उत्तर:
(c) त्रिज्या के चतुर्थ घात के समानुपाती ।
![]()
प्रश्न 4.
चन्द्रमा पर वायुमण्डल की अनुपस्थिति का निम्न कारण है-
(a) चन्द्रमा काफी हल्का है।
(b) चन्द्रमा पृथ्वी के परितः परिक्रमण करता है।
(c) गैसों के अणुओं की वर्ग माध्य मूल वेग पलायन वेग से अधिक है।
(d) उपर्युक्त सभी।
उत्तर:
(c) गैसों के अणुओं की वर्ग माध्य मूल वेग पलायन वेग से अधिक है।
प्रश्न 5.
सूर्य के चारों ओर घूमते ग्रह की माध्य त्रिज्या दी जाती है-
(a) दीर्घवृत्त की अर्ध दीर्घ अक्ष (a) के बराबर ।
(b) दीर्घवृत्त की अर्ध लघु अक्ष (b) के बराबर ।
(c) अर्घ दीर्घ व अर्थ लघु अक्ष का माध्य \(\frac{a+b}{2}\)।
(d) अर्ध दीर्घ व अर्ध लघु अक्ष का गुणोत्तर माध्य \(\sqrt{ab}\)।
उत्तर:
(a) दीर्घवृत्त की अर्ध दीर्घ अक्ष (a) के बराबर ।
प्रश्न 6.
पृथ्वी तल से \(\sqrt{gR_e}\), वेग से फेंके गये प्रक्षेप्य की ऊर्जा क्या होगी? (Re पृथ्वी की त्रिज्या है)।
(a) 2Re
(b) Re / 2
(c) Re
(d) अनन्त
उत्तर:
(c) Re
![]()
प्रश्न 7.
गुरुत्वीय त्वरण का मान अधिकतम होता है-
(a) पृथ्वी की भूमध्य रेखा पर
(b) पृथ्वी के ध्रुवों पर
(c) किसी पहाड़ की चोटी पर
(d) पृथ्वी के अन्दर गहरी खान में
उत्तर:
(b) पृथ्वी के ध्रुवों पर
प्रश्न 8.
सार्वत्रिक गुरुत्वाकर्षण नियतांक G की विमा है-
(a) [ML2T-2]
(b) [M-1LT-2]
(c) [M-1L3T-2]
(d) [M-1L3T-1]
उत्तर:
(c) [M-1L3T-2]
प्रश्न 9.
यदि पृथ्वी की घूर्णन गति बढ़ जाये तो अक्षांश पर स्थित किसी वस्तु का भार-
(a) बढ़ जायेगा
(b) घट जायेगा
(c) अपरिवर्तित रहेगा
(d) कुछ निश्चित नहीं है
उत्तर:
(b) घट जायेगा
प्रश्न 10.
पृथ्वी की सतह के निकट चक्कर लगा है। उपग्रह का कक्षीय वेग लगभग होगा-
(a) 8km/s
(c) 4 km/s
(b) 11.2 km/s
(d) 6km/s
उत्तर:
(a) 8km/s
प्रश्न 11.
चन्द्रमा पर पलायन वेग है (लगभग).
(a) 11.2 km/s
(b) 5 km/s
(c) 10 km/s
(d) 2.4 km/s
उत्तर:
(d) 2.4 km/s
![]()
प्रश्न 12.
पृथ्वी व चन्द्रमा के द्रव्यमान तथा त्रिज्या क्रमशः M1,R1 व M2,R2 हैं। उनके केन्द्रों के बीच की दूरी d है। उनके बीच मध्य- बिन्दु से m द्रव्यमान के कण को किस न्यूनतम वेग से प्रक्षेपित किया जाना चाहिए जिससे वह अनन्त पर पहुँच जाए?
(a) \(2 \sqrt{\frac{G}{d}\left(M_1+M_2\right)}\)
(b) \(2 \sqrt{\frac{2G}{d}\left(M_1+M_2\right)}\)
(c) \(2 \sqrt{\frac{2G}{d}\left(M_1+M_2\right)}\)
(d) \(2 \sqrt{\frac{GM(M_1+M_2)}{d(M_1+M_2)}}\)
उत्तर:
(a) \(2 \sqrt{\frac{G}{d}\left(M_1+M_2\right)}\)
प्रश्न 13.
न्यूटन का गुरुत्वाकर्षण का नियम सार्वत्रिक होता है क्योंकि-
(a) वह सदैव आकर्षण होता है।
(b) वह सौरमण्डल के सभी सदस्यों एवं कणों पर लागू होता है।
(c) यह सभी द्रव्यमान पर दूरियों के लिए लागू होता है तथा माध्यम से प्रभावित नहीं होता है।
(d) उपर्युक्त में से कोई नहीं।
उत्तर:
(c) यह सभी द्रव्यमान पर दूरियों के लिए लागू होता है तथा माध्यम से प्रभावित नहीं होता है।
प्रश्न 14.
पृथ्वी तल के निकट परिक्रमा करने वाले कृत्रिम उपग्रह का परिक्रमण काल होता है-
(a) 24 घण्टा
(b) 84 मिनट
(c) 48 मिनट
(d) 12 घण्टा
उत्तर:
(b) 84 मिनट
प्रश्न 15.
किसी खोखले गोले के केन्द्र पर गुरुत्वीय क्षेत्र की तीव्रता होती है-
(a) \(\frac{GM}{r^2}\)
(b) g
(c) 0
(d) \(\frac{2GM}{r^2}\)
उत्तर:
(c) 0
अति लघु उत्तरीय प्रश्न (Very Short Answer Questions)
प्रश्न 1.
धूमकेतु की पूँछ सूर्य से दूर होने का क्या कारण है?
उत्तर:
सूर्य द्वारा उत्सर्जित विकिरणों के दाव के कारण इस पर उपस्थित गैसें सूर्य से दूर की ओर पूँछ बना लेती हैं।
प्रश्न 2.
किसी उपग्रह का वेग उसके द्रव्यमान पर किस प्रकार निर्भर करता है?
उत्तर:
उपग्रह का वेग उसके द्रव्यमान पर निर्भर नहीं करता है।
प्रश्न 3.
समुद्र में उत्पन्न ज्वार भाटे का प्रमुख कारण क्या है?
उत्तर:
चन्द्रमा का पृथ्वी पर गुरुत्वाकर्षण प्रभाव ज्वार भाटे का प्रमुख कारण है।
प्रश्न 4.
तुल्यकाली उपग्रह क्या होता है?
उत्तर:
ऐसा उपग्रह जो पृथ्वी के किसी निश्चित भू-भाग के ऊपर सदैव देखा जा सकता है तुल्यकाली उपग्रह कहलाता है। इसका आवर्तकाल 24 घंटे होता है।
प्रश्न 5.
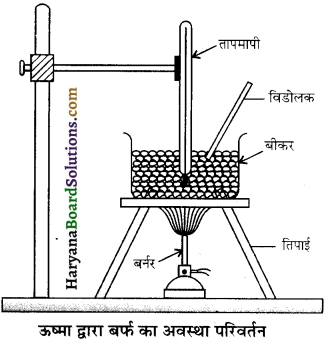
चन्द्रमा पर 10°C पर पानी से भरी बोतल का ढक्कन खोलने पर क्या होगा?
उत्तर:
पानी उबलने लगेगा क्योंकि चन्द्रमा पर वायुमण्डल न होने के कारण क्वथनांक काफी घट जाता है और पानी उबलने लगता है।
प्रश्न 6.
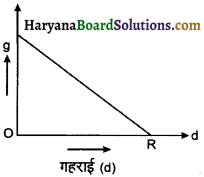
पृथ्वी के अन्दर केन्द्र की ओर जाने पर g का मान दूरी के साथ कैसे बदलता है?
उत्तर:
पृथ्वी अन्दर की ओर जाने पर गुरुत्वीय त्वरण का परिवर्तन चित्र की भाँति रेखीय रूप से होता है।
प्रश्न 7.
समुद्र में ज्वार भाटा क्यों उत्पन्न होता है?
उत्तर:
चन्द्रमा के गुरुत्वाकर्षण प्रभाव के कारण ज्वार भाटा उत्पन्न होता है।
![]()
प्रश्न 8.
पृथ्वी ध्रुवों पर चपटी क्यों है?
उत्तर:
अपनी अक्ष पर घूर्णन के कारण पृथ्वी ध्रुवों पर चपटी होती
प्रश्न 9.
यदि पृथ्वी सूर्य के चारों ओर वृत्तीय कक्षा में घूमती है, तो गुरुत्वाकर्षण बल द्वारा किया गया कार्य क्या होगा?
उत्तर:
शून्य; क्योंकि पृथ्वी पर सूर्य का आकर्षण बल (अभिकेन्द्रीय बल) सदैव पृथ्वी की गति के लम्बवत् होता है।
प्रश्न 10.
1 kg wt (किग्रा भार ) में कितने न्यूटन होते हैं?
उत्तर:
1kg wt = 1kg द्रव्यमान का भार = mg
= 1 × 9.8 न्यूटन
1kg wt = 9.8 न्यूटन
प्रश्न 11.
एक उपग्रह को ग्रह के परितः घूमने के लिए अभिकेन्द्रीय बल कहाँ से प्राप्त होता है?
उत्तर:
ग्रह एवं उपग्रह के मध्य लगने वाला गुरुत्वाकर्षण बल ही आवश्यक अभिकेन्द्रीय बल प्रदान करता है।
प्रश्न 12.
किसी उपग्रह की बन्धन ऊर्जा से क्या अभिप्राय है?
उत्तर:
ऊर्जा की वह मात्रा जो उपग्रह को देने पर उपग्रह पलायन कर जाये, उपग्रह की बन्धन ऊर्जा कहलाती है। इसका मान,
\(E_b=\frac{1}{2} \frac{G M m}{r}\)
प्रश्न 13.
सरल लोलक पर आधारित घड़ी उपग्रह पर काम में नहीं ली जाती है, क्यों?
उत्तर:
उपग्रह में वस्तुएँ भारहीनता की स्थिति में होती हैं अतः g = 0 होता है इसलिए सरल लोलक पर आधारित घड़ी \(\left(T=2 \pi \sqrt{\frac{l}{g}}\right)\) कार्य नहीं करती है।
प्रश्न 14.
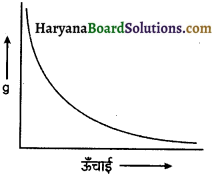
पृथ्वी तल से ऊपर जाने पर g का मान किस प्रकार बदलता है? ग्राफ बनाइये।
उत्तर:
पृथ्वी तल से ऊपर जाने पर g का मान घटता है व निम्न चित्र के अनुसार बदलता है।
प्रश्न 15.
कृत्रिम उपग्रह में चलने कूदने तथा पानी पीने में कठिनाई महसूस होती है, क्यों?
उत्तर:
भारहीनता के कारण।
प्रश्न 16.
किसी वस्तु को पृथ्वी तल से अनन्त तक ले जाने में कितना कार्य करना पड़ता है?
उत्तर:
पृथ्वी तल पर वस्तु की गुरुत्वीय स्थितिज ऊर्जा \(\frac{GMm}{R}\) के बराबर कार्य करना पड़ता है।
प्रश्न 17.
यदि दो वस्तुओं के मध्य दूरी % घटा दी जाये तो उनके मध्य लगने वाला बल कितने प्रतिशत बढ़ जायेगा ?
उत्तर:
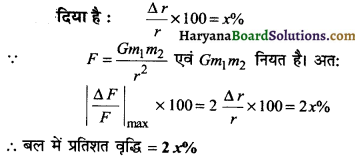
![]()
प्रश्न 18.
पृथ्वी के केन्द्र पर ४ का मान क्या होगा?
उत्तर:
शून्य ।
प्रश्न 19.
संचार उपग्रह पृथ्वी सतह से कितनी ऊँचाई पर परिक्रमा करते हैं?
उत्तर:
36000km की ऊँचाई पर
प्रश्न 20.
ध्रुवीय उपग्रह किसे कहते हैं?
उत्तर:
वे कृत्रिम उपग्रह जिनकी कक्षा का तल पृथ्वी के उत्तरी व दक्षिणी ध्रुवों के पास से गुजरता है, ध्रुवीय उपग्रह कहलाते हैं। इनकी कक्षा पश्च गतिक होती है।
प्रश्न 21.
समस्त पृथ्वी पर एक साथ संचार लिंक करने की दृष्टि से न्यूनतम कितने भू-स्थाई उपग्रह आवश्यक हैं?
उत्तर:
तीन
प्रश्न 22.
पार्किंग कक्षा किसे कहते हैं?
उत्तर;
उपग्रह की वह कक्षा जिसका केन्द्र पृथ्वी के केन्द्र से सम्पाती होता है, पार्किंग कक्षा कहलाती है।
प्रश्न 23.
ठोस गोले के केन्द्र पर गुरुत्वीय स्थितिज ऊर्जा का मान क्या होता है? यह मान सतह पर गुरुत्वीय स्थितिज ऊर्जा के मान का कितने प्रतिशत होता है?
उत्तर:
गोले के केन्द्र पर स्थितिज ऊर्जा \(U_0=\frac{3}{2} \frac{G M m}{R}\)
सतह पर गुरुत्वीय स्थितिज ऊर्जा \(U_s=-\frac{G M m}{R}\)
∴ \(\frac{U_0}{U_s} \times 100=\frac{3}{2} \times 100=\mathbf{1 5 0} \%\)
प्रश्न 24.
चन्द्रमा पर गुरुत्वीय त्वरण, पृथ्वी पर गुरुत्वीय त्वरण का कौन-सा भाग है?
उत्तर:
चन्द्रमा पर गुरुत्वीय त्वरण पृथ्वी पर गुरुत्वीय त्वरण का \(\frac{1}{6}\) भाग होता है अर्थात्
\(g_m=\frac{g_e}{6}\)
प्रश्न 25.
गुरुत्वीय स्थितिज ऊर्जा किसे कहते हैं? इसकी विमा लिखिए।
उत्तर:
किसी वस्तु को अनन्त से किसी बिन्दु तक लाने में जो कार्य करना पड़ता है उसे उस बिन्दु पर उस वस्तु की गुरुत्वीय स्थितिज ऊर्जा कहते हैं। इसका विमीय सूत्र = [M1L2T-2]
प्रश्न 26.
पृथ्वी तल से किसी वस्तु के लिए पलायन वेग का मान 11.2 km / s है। जब वस्तु क्षैतिज से 30° पर फेंकी जाये तो पलायन वेग का मान क्या होगा?
उत्तर:
पलायन वेग प्रक्षेपण कोण पर निर्भर नहीं करता है अतः 30° के कोण पर प्रक्षेपित करने पर भी पलायन वेग 11.2 kms-1 ही होगा।
![]()
प्रश्न 27.
चन्द्रमा पृथ्वी की तुलना में बहुत हल्का है, फिर ये पृथ्वी के गुरुत्वाकर्षण द्वारा गिरता क्यों नहीं?
उत्तर:
चन्द्रमा पृथ्वी के परितः वृत्तीय कक्षा में परिक्रमा करता है। अतः पृथ्वी द्वारा आरोपित समस्त गुरुत्वाकर्षण बल अभिकेन्द्र बल के रूप में व्यय हो जाता है इसीलिए हल्का होने पर भी चन्द्रमा गिरता नहीं है।
प्रश्न 28.
10g सोने का भार ध्रुवों पर भूमध्य रेखा की तुलना में अधिक होता है, क्यों?
उत्तर:
किसी स्थान पर किसी वस्तु का भार mg
स्पष्ट है कि भार का मान 8 पर निर्भर करता है, और ध्रुवों पर गुरुत्वीय त्वरण अधिकतम तथा भूमध्य रेखा पर न्यूनतम होता है। इसीलिए 10g सोने का भार ध्रुवों पर भूमध्य रेखा की अपेक्षा अधिक होता है।
प्रश्न 29.
भारत द्वारा छोड़े गये प्रथम उपग्रह का नाम बताइये।
उत्तर:
आर्यभट्ट 19 अप्रैल 1975 ।
प्रश्न 30.
गुरुत्वीय क्षेत्र की विमा लिखिए।
उत्तर:
गुरुत्वीय क्षेत्र की तीव्रता,
\(E_g=\frac{F}{M}\)
∴ Eg का विमीय सूत्र = \(\frac{\left[M^1 L^1 T^{-2}\right]}{\left[M^1\right]}=\left[M^0 L^1 T^{-2}\right]\)
प्रश्न 31 –
केप्लर का द्वितीय नियम किस भौतिक राशि के संरक्षण पर आधारित है?
उत्तर:
कोणीय संवेग संरक्षण के सिद्धान्त पर
प्रश्न 32.
पृथ्वी की परिक्रमा करते उपग्रह में बैठा अंतरिक्ष यात्री एक गेंद उपग्रह के बाहर छोड़ देता है। क्या गेंद पृथ्वी तल पर पहुँचेगी?
उत्तर:
नहीं गेंद भी उपग्रह के साथ-साथ पृथ्वी की परिक्रमा करेगी।
प्रश्न 33.
जब कोई वस्तु पृथ्वी की ओर गिरती है तो क्या पृथ्वी भी उस वस्तु की ओर गिरती है? यदि हाँ तो पृथ्वी का गिरना हमें दिखाई क्यों नहीं देता?
उत्तर:
क्योंकि पृथ्वी का द्रव्यमान बहुत अधिक होने के कारण, पृथ्वी का वस्तु की ओर त्वरण नगण्य होता है।
प्रश्न 34.
पृथ्वी के केन्द्र से R दूरी पर गुरुत्वीय विभव कितना होता है?
उत्तर:
पृथ्वी के केन्द्र से R दूरी पर गुरुत्वीय विभव
\(V_G=- \frac{GM}{R}\)
![]()
प्रश्न 35.
केप्लर के तीसरे नियम का गणितीय स्वरूप क्या है?
उत्तर:
T² = K r³ ;
जहाँ T = ग्रह का आवर्तकाल
r = सूर्य एवं पृथ्वी के मध्य औसत दूरी;
K = नियतांक
प्रश्न 36.
चन्द्रमा पर उतरने से पहले अंतरिक्ष यात्री अपनी पीठ पर भारी वजन क्यों बाँध लेते हैं?
उत्तर:
चन्द्रमा पर 8 का मान कम होने के कारण।
प्रश्न 37.
किसी पिण्ड की गुरुत्वीय स्थितिज ऊर्जा शुक्र ग्रह पर.7.5 × 106 J है। पिण्ड को ग्रह से बाहर फेंकने के लिए आवश्यक ऊर्जा का मान बताइये।
उत्तर:
आवश्यक ऊर्जा =.0. (-7.5 × 106) J
= 7.5 × 105 J
प्रश्न 38.
पृथ्वी तल पर पलायन वेग का मान कितना है?
उत्तर:
पृथ्वी तल पर पलायन वेग 11.2 km.s-1 है।
प्रश्न 39.
किसी प्रक्षेप्य द्वारा प्राप्त महत्तम ऊँचाई का सूत्र लिखिए।
उत्तर:
\(h=\frac{v^2 R}{2 g R-v^2}\)
प्रश्न 40.
एक कमानीदार तुला एक कृत्रिम उपग्रह में टंगी है जिससे 11 द्रव्यमान का एक पिण्ड लटका है। तुला का पाठ्यांक कितना होगा?
उत्तर:
शून्या
प्रश्न 41 –
गुरुत्वाकर्षण नियतांक 6 को सार्वत्रिक नियतांक क्यों कहते हैं?
उत्तर:
क्योंकि G का मान समय स्थिति अथवा पिण्डों की प्रकृति व अवस्था पर निर्भर नहीं होता है, अतः इसे सार्वत्रिक नियतांक कहते हैं।
प्रश्न 42 –
क्या घर्षण बल गुरुत्वाकर्षण से बढ़ता है?
उत्तर:
नहीं; क्योंकि घर्षण बल की उत्पत्ति विद्युतीय प्रकृति की है।
प्रश्न 43.
किस वैज्ञानिक ने सर्वप्रथम G का प्रायोगिक मान ज्ञात किया?
उत्तर:
कैवेन्डिश
प्रश्न 44.
कृत्रिम उपग्रह की कक्षा को वायुमण्डल से बाहर क्यों रखा जाता है?
उत्तर:
ताकि वायु के घर्षण के कारण उपग्रह की ऊर्जा कम न हो जाये।
![]()
लघु उत्तरीय प्रश्न
प्रश्न 1.
भार व द्रव्यमान में अन्तर स्पष्ट कीजिए।
उत्तर:
भार व द्रव्यमान में अन्तर
| भार | द्रव्यमान |
| 1. पृथ्वी द्वारा पिण्ड पर आरोपित आकर्षण बल पिण्ड का भार कहलाता है। | 1. किसी पिण्ड में उपस्थित द्रव्य की मात्रा को उसका द्रव्यमान कहते हैं। |
| 2. इसका मात्रक न्यूटन या किग्रा-भार है। | 2. इसका मात्रक किग्रा है। |
| 3. यह सदिश राशि है। | 3. यह अदिश राशि है। |
| 4. इसका मान g के साथ परिवर्तित होता हैं। | 4. इसका मान g के साथ परिवर्तित नहीं होता है। |
प्रश्न 2.
यदि कोई पिण्ड पृथ्वी तल से v(v > ve) वेग से फेंका जाता है तो पृथ्वी के गुरुत्वीय क्षेत्र के बाहर इसका वेग ज्ञात कीजिए।
उत्तर:
पृथ्वी तल पर कुल ऊर्जा = अनन्त पर कुल ऊर्जा

प्रश्न 3.
दो पिण्डों A व B के बीच की दूरी है। गुरुत्वाकर्षण की पारस्परिक क्रिया में बल को दूरी के व्युत्क्रम वर्ग के नियम के अनुसार लेने पर पिण्ड 1 का त्वरण है। यदि पारस्परिक क्रिया दूरी के व्युत्क्रम चतुर्थ घात के नियम का पालन करे, तो पिण्ड का त्वरण क्या होगा ?

उत्तर:
A पर B के कारण गुरुत्वीय बल

प्रश्न 4.
किसी ग्रह से सूर्य की औसत दूरी पृथ्वी से सूर्य की औसत दूरी की नौ गुनी है। ग्रह कितने वर्ष में सूर्य की परिक्रमा करेगा?
उत्तर:
केप्लर के तृतीय नियम से
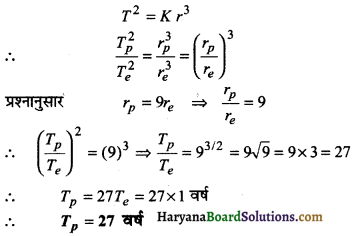
![]()
प्रश्न 5.
दो पिण्डों के मध्य गुरुत्वाकर्षण बल F है। यदि उनके बीच की दूरी 2 गुनी कर दें, तो उनके मध्य आकर्षण बल कितना होगा?
उत्तर:
r दूरी पर बल F = \(\frac{G m_1 m_2}{r^2}\)
और 2r दूरी पर बल F’ = \(\frac{G m_1 m_2}{(2 r)^2}=\frac{1}{4} \frac{G m_1 m_2}{r^2}=\frac{1}{4} F\)
या F’ = \(\frac{F}{4}\)
प्रश्न 6.
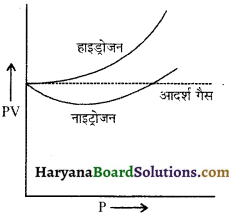
बृहस्पति पर वातावरण हल्की गैसों (सामान्यतः हाइड्रोजन) से युक्त है, जबकि पृथ्वी के वातावरण में बहुत कम हाइड्रोजन गैस है, क्यों?
उत्तर:
बृहस्पति ग्रह पर पलायन वेग पृथ्वी पर पलायन वेग से काफी अधिक है। इसलिए वहाँ से वस्तुओं को पलायन के लिए काफी अधिक वेग की आवश्यकता होती है। ऊष्मीय वेग इस पलायन वेग से कम होता है; अतः वहाँ से हल्की गैसें पलायन नहीं कर पाती हैं। इसीलिए हाइड्रोजन गैस बृहस्पति ग्रह के वातावरण में अधिक पायी जाती है।
प्रश्न 7.
रेडियन प्रति घंटा में भूस्थिर उपग्रह का कोणीय वेग कितना होगा?
उत्तर:
भूस्थिर उपग्रह का आवर्तकाल
T = पृथ्वी के घूर्णन का आवर्तकाल = 24 घंटे
∴ कोणीय वेग ω = \(\frac{2π}{T}=\frac{2π}{24}\) रेडियन प्रति घंटा
या w = \(\frac{π}{12}\) रेडियन / घंटा
प्रश्न 8.
जब कोई उपग्रह गिरता हुआ पृथ्वी के वायुमण्डल में प्रवेश करता है तो वह गर्म हो जाता है, अर्थात् उसकी यान्त्रिक ऊर्जा में ह्रास होता है। परन्तु उपग्रह बढ़ती हुई चाल से कुण्डलिनी के रूप में नीचे गिरता है, क्यों?
उत्तर:
अपनी कक्षा में घूमते हुए उपग्रह की कुल ऊर्जा ऋणात्मक होती है जब उपग्रह पृथ्वी के वायुमण्डल में प्रवेश करता है तो उसकी यांत्रिक ऊर्जा में (जोकि ऋणात्मक होती है) हास होता है अतः यह और ऋणात्मक हो जाती है परन्तु कक्षीय चाल vo = \(\frac{GM_e}{R_e+h}\) तभी बढ़ेगी जब ऊँचाई घटेगी। अतः उपग्रह कुण्डलिनी के रूप में बढ़ती हुई चाल से नीचे गिरता है।
प्रश्न 9.
पृथ्वी पर कोई पिण्ड आपस में गुरुत्वीय बल के कारण एक दूसरे की तरफ गति नहीं करते; क्यों?
उत्तर:
दो पिण्डों के मध्य आकर्षण बल, पृथ्वी की तुलना में उनके कम द्रव्यमानों के कारण नगण्य होता है अतः इनसे निर्मित त्वरण भी बहुत कम (शून्य) होता है इसीलिए वे एक दूसरे की ओर गति नहीं करते हैं।
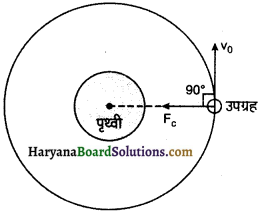
प्रश्न 10.
पृथ्वी के परितः गतिशील उपग्रह पर एक बल लगता है। इस बल के कारण पृथ्वी द्वारा उपग्रह पर कितना कार्य किया जाता है?
उत्तर:
पृथ्वी द्वारा उपग्रह पर आरोपित गुरुत्वाकर्षण बल उपग्रह को आवश्यक अभिकेन्द्रीय बल प्रदान करने में व्यय हो जाता है। चूंकि अभिकेन्द्र बल एवं उपग्रह की कक्षीय चाल vo परस्पर लम्बवत् होते हैं। अतः इस बल द्वारा कोई कार्य नहीं किया जाता है।
![]()
प्रश्न 11.
चन्द्रमा के खिंचाव के कारण ज्वार भाटा अधिक तथा सूर्य के खिंचाव के कारण ज्वार भाटा कम प्रभावी होता है जबकि सूर्य का खिंचाव चन्द्रमा की अपेक्षा अधिक होता है। समझाइये क्यों?
उत्तर:
जिस प्रकार गुरुत्वाकर्षण बल दूरी के वर्ग के व्युत्क्रमानुपाती होता है उसी प्रकार ज्वार भाटा दूरी की तृतीय घात के व्युत्क्रमानुपाती है। चूँकि पृथ्वी से चन्द्रमा की दूरी सूर्य की तुलना में काफी कम है, इसीलिए चन्द्रमा के खिचाव के कारण ज्वार भाटा अधिक आता है।
प्रश्न 12.
एक हाथी एवं एक चींटी में से किसका पलायन वेग अधिक होगा और किसकी पलायन ऊर्जा अधिक होगी?
उत्तर:
पलायन वेग के सूत्र ve = \(\sqrt{\frac{2GM}{R}}\) में वस्तु का द्रव्यमान (m) नहीं है। अतः हाथी एवं चीटी दोनों के लिए पलायन वेग समान होगा। परन्तु पलायन ऊर्जा Ee = \(\frac{1}{2}\)mve² द्रव्यमान के अनुक्रमानुपाती होती है अतः हाथी के लिए पलायन ऊर्जा काफी अधिक होगी।
प्रश्न 13.
समझाइये कि टेनिस की गेंद पहाड़ी पर अधिक एवं मैदान पर कम क्यों उछलती है?
उत्तर;
गुरुत्वीय त्वरण g का मान मैदान की अपेक्षा पहाड़ी पर कम होता है अतः टेनिस की गेंद का भार (mg) पहाड़ी पर कम एवं मैदान पर अधिक होता है भार जितना कम होता है गेंद उतनी ही अधिक उछलती है। इसीलिए मैदान की अपेक्षा पहाड़ी पर टेनिस की गेंद अधिक उछलती है।
प्रश्न 14.
मध्य रात्रि में सूर्य हमें पृथ्वी की दिशा में खींचता है। परन्तु मध्य दिन में पृथ्वी की विपरीत दिशा में खींचता है। क्या हमारा भार रात को अधिक एवं दिन में कम होता है? समझाइये |
उत्तर:
नहीं; क्योंकि गुरुत्वाकर्षण खिंचाव पिण्ड को निश्चित अभिकेन्द्रीय बल प्रदान करता है जिससे वह अपनी कक्षा में घूर्णन कर सके। वह पिण्ड के भार में परिवर्तन नहीं करता है।
प्रश्न 15.
m द्रव्यमान का एक कण, त्रिज्या के क्षैतिज वृत्त में एक अभिकेन्द्रीय बल \(\frac{k}{r^2}\) के अन्तर्गत् घूम रहा है, जहाँ k नियतांक है। कण में कुल कितनी ऊर्जा है ?
उत्तर:
गतिज ऊर्जा K = \(\frac{1}{2}\)mv²
दिया है –
F = \(\frac{k}{r^2}=frac{mv^2}{r^2}\) ⇒ mv² = \(\frac{k}{r}\)
∴ K = \(\frac{1}{2}\)mv² = \(\frac{k}{2r}\)
स्थितिज ऊर्जा U = -F.r = –\(\frac{k}{r^2}\).r = \(– \frac{k}{r}\)
कुल ऊर्जा,
Et = K + U = \(\frac{k}{2r}-\frac{k}{r}=- \frac{k}{2r}\)
या Et = \(– \frac{k}{2r}\)
![]()
प्रश्न 16.
अपनी अक्ष पर पृथ्वी के घूमने की वह चाल ज्ञात कीजिए ताकि भूमध्य रेखा पर किसी वस्तु का भार इस समय के भार का 3/5 हो जाये। भूमध्य रेखा की त्रिज्या 6400 km मान लीजिए।
उत्तर:
दिया है- g’ = \(\frac{3}{5}\)g
जहाँ g = पृथ्वी पर गुरुत्वीय त्वरण
भूमध्य रेखा के लिए-
∵ g’ = g – R ω²
∴ \(\frac{3}{5}\)g = g – R ω²
या R ω² = g – \(\frac{3}{5}\)g = \(\frac{2}{5}\)g
या ω² = \(\frac{2g}{5R}\) ⇒ ω = \(\sqrt{\frac{2g}{5R}}=\sqrt{\frac{2 \times 9.8}{5 \times 6.4 \times 10^6}}\)
या ω = 7.8 × 10-4 rad.s-1
प्रश्न 17.
पृथ्वी के परितः वृत्तीय पथ पर परिक्रमा करते उपग्रह पर अभिकेन्द्र बल है। इस पर पृथ्वी का गुरुत्वीय बल कितना है? तथा इस पर परिणामी बल कितना है?
उत्तर:
पृथ्वी के परितः वृत्तीय पथ पर परिक्रमा करने के लिए आवश्यक अभिकेन्द्रीय बल गुरुत्वीय बल ही प्रदान करता है। अतः गुरुत्वीय बल ही परिणामी बल F है।
प्रश्न 18.
क्या घर्षण बल व अन्य सम्पर्क बल गुरुत्वाकर्षण के कारण उत्पन्न होते हैं?
उत्तर:
नहीं; घर्षण अथवा अन्य सम्पर्क बलों की उत्पत्ति विद्युत बलों के कारण होती है।
प्रश्न 19.
यदि दो ग्रहों की त्रिज्याएं R1 व R2 हों तथा माध्य घनत्व ρ1 व ρ2 हों तो सिद्ध कीजिए कि दोनों ग्रहों पर गुरुत्वीय त्वरणों का अनुपात R1ρ1 : R2ρ2 होगा।
उत्तर:
गुरुत्वीय त्वरण

![]()
प्रश्न 20.
यदि किसी उपग्रह की घूर्णन आवृत्ति N हो तो सिद्ध कीजिए कि (R+h)³ ∝ \(\frac{1}{N^2}\)
उत्तर:
उपग्रह का आवर्तकाल

प्रश्न 21.
यदि पृथ्वी के समीप परिक्रमा कर रहे उपग्रह की गतिज ऊर्जा दो गुनी हो जाये तो क्या उपग्रह अपनी कक्षा को छोड़कर पलायन कर जायेगा? यदि हाँ तो क्यों?
उत्तर:
गतिज ऊर्जा दो गुनी हो जाती है अतः
K’ = 2K
या \(\frac{1}{2}\)mv’² = \(\frac{1}{2}\)mv² × 2
या v’ = vo√2
पृथ्वी के समीप परिक्रमा करने वाले उपग्रह की कक्षीय चाल vo एवं पलायन वेग में निम्न सम्बन्ध होता है-
∵ ve = vo√2
∴ v’ = ve (पलायन वेग )
अतः उपग्रह अपनी कक्षा छोड़कर पलायन कर जायेगा।
प्रश्न 22.
साधारणतः पृथ्वी से फेंके गये प्रक्षेप्य का पथ परवलयाकार होता है परन्तु अधिक ऊँचाई तक फेंके गये प्रक्षेप्यों का पथ दीर्घ वृत्ताकार होता है, क्यों?
उत्तर;
साधारण ऊँचाई तक g का मान लगभग नियत रहता है। अतः प्रक्षेप्य लगभग नियत त्वरण के अन्तर्गत गति करता है जिससे इसका पथ परवलयाकार हो जाता है परन्तु अत्यधिक ऊंचाई पर गुरुत्वीय त्वरण पृथ्वी के केन्द्र से दूरी के वर्ग के व्युत्क्रमानुपाती g ∝ \(\frac{1}{r^2}\) होता है, फलस्वरूप g का मान घटता चला जाता है अतः परिवर्ती गुरुत्वीय त्वरण के कारण प्रक्षेप्य पथ दीर्घ वृत्ताकार हो जाता है।
![]()
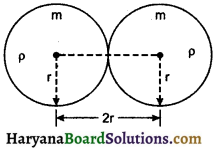
प्रश्न 23.
किसी धातु के दो समान आकार के गोले (ठोस) एक-दूसरे को स्पर्श करते हुए रखे हैं। उनके बीच कार्य करने वाला बल उनकी त्रिज्या से किस प्रकार सम्बन्धित है?
उत्तर:
गोलों के मध्य गुरुत्वाकर्षण बल,
\(F=G \frac{m_1 m_2}{r^2}\)
गोले समान धातु के हैं अतः इनके घनत्व (ρ) भी समान होंगे अतः
= \(\frac{G m_1 m_2}{(2 r)^2}=\frac{G \frac{4}{3} \pi r^3 \rho \frac{4}{3} \pi r^3 \rho}{4 r^2}\)
\(F=\frac{4}{9} \pi^2 G \rho^2 r^4\)
या F ∝ r4
प्रश्न 24.
एक पिण्ड को पृथ्वी के केन्द्र से ऊपर उठाते हुए चन्द्रमा तक ले जाते हैं। पिण्ड के भार में क्या परिवर्तन होंगे?
उत्तर:
पृथ्वी के केन्द्र पर g= 0, अतः पिण्ड का भार भी शून्य होता है। पृथ्वी के केन्द्र से ऊपर जाने पर g का मान भी बढ़ता है और पृथ्वी सतह पर अधिकतम हो जाता है पुनः पृथ्वी सतह से ऊपर जाने पर g का मान दूरी घटने के साथ-साथ घटता है और जहाँ पर पृथ्वी व चन्द्रमा की गुरुत्वाकर्षण सीमाएं मिलती है, वहाँ पर भार शून्य हो जाता है। इसके बाद चन्द्रमा के गुरुत्वाकर्षण के कारण भार पुनः बढ़ता जायेगा।
प्रश्न 25.
पृथ्वी सतह से h ऊँचाई पर जाने पर यदि वस्तु पर लगने वाला गुरुत्वाकर्षण बल आधा रह जाता है तो h व R में सम्बन्ध बताइये।
उत्तर:
∵ Fh = \(\frac{1}{2}\)Fs
∴ \(\frac{G M \cdot m}{(R+h)^2}=\frac{1}{2} \frac{G M m}{R^2} \Rightarrow \frac{1}{(R+h)^2}=\frac{1}{2 R^2}\)
या (R+h )² = 2R²
या (R+h) = R√2
या h = R√2 – R = R(√2 – 1)
या h = R(1.414 – 1)
या h = 0.414 R
प्रश्न 26.
एक उपग्रह किसी ग्रह के समीप परिक्रमा करता है। यदि उपग्रह का आवर्तकाल T एवं ग्रह का माध्य घनत्व d हो, तो सिद्ध कीजिए कि T × √d एक सार्वत्रिक नियतांक है।
उत्तर:
किसी ग्रह के उपग्रह का आवर्तकाल,
\(T=2 \pi \sqrt{\frac{(R+h)^3}{G M}}\)
∵ उपग्रह ग्रह के समीप परिक्रमा करता है अतः h << R
∴ h को छोड़ने पर
\(2 \pi \sqrt{\frac{R^3}{G \cdot \frac{4}{3} \pi R^3 \cdot d}}=\sqrt{\frac{4 \pi^2 \times 3}{4 \pi G d}}=\sqrt{\frac{3 \pi}{G d}}\)
या T × √d = \(\sqrt{\frac{3 \pi}{G d}}\) = एक सार्वत्रिक नियतांक
या T . √d = सार्वत्रिक नियतांक
![]()
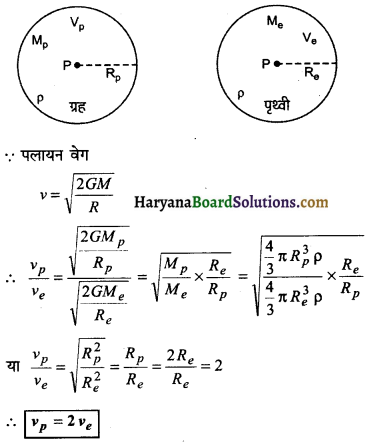
प्रश्न 27.
एक ग्रह की त्रिज्या पृथ्वी की त्रिज्या से दो गुनी है तथा ग्रह तथा पृथ्वी दोनों के औसत घनत्व समान हैं। यदि ग्रह एवं पृथ्वी पर पलायन वेग क्रमशः vp तथा ve हों, तो सिद्ध कीजिए कि vp = 2ve.
उत्तर:
दिया है-
Rp = 2Re
ρp = ρe = ρ
प्रश्न 28.
कोई ग्रह सूर्य के परितः v ms-1 की चाल से Ts में एक पूरा चक्कर लगाता है। दिखाइये कि इस ग्रह पर सूर्य की ओर दिष्ट
त्वरण का मान \(\frac{2πv}{T}\) होता है।
उत्तर:
अभिकेन्द्रीय त्वरण,
ac = \(\frac{v^2}{r}\)
= \(\frac{v}{r}\) v = ω v = \(\frac{2π}{T}\) v
या ac = \(\frac{2πv}{r}\)
प्रश्न 29.
यदि हम अपनी छोटी अंगुली भी हिलाते हैं तो सम्पूर्ण ब्रह्माण्ड को छोड़ना पड़ता है, क्यों?
उत्तर:
न्यूटन के गुरुत्वाकर्षण नियम से इस ब्रह्माण्ड का प्रत्येक कण दूसरे कणों को आकर्षित करता है और यह आकर्षण बल दूरी के वर्ग के व्युत्क्रमानुपाती होता है अतः जब हम अपनी अंगुली उठाते हैं तो कणों के मध्य दूरी बदलती है जिससे आकर्षण बदलता है यह ब्रह्माण्ड को विचलित कर देता है।
प्रश्न 30.
कृत्रिम उपग्रह में कोई ईंधन नहीं होता फिर भी यह पृथ्वी के चारों ओर घूमता है क्यों?
उत्तर:
पृथ्वी तथा उपग्रह के मध्य लगने वाला गुरुत्वाकर्षण बल उपग्रह को पृथ्वी के चारों ओर वृत्तीय कक्षा में घूमने के लिए आवश्यक अभिकेन्द्रीय बल प्रदान करता है। इसीलिए उपग्रह पृथ्वी के परितः घूमता रहता है।
प्रश्न 31.
अंतरिक्ष यान में भारहीनता के कारण एक यात्री को क्या-क्या परेशानियाँ अनुभव होती हैं? इनका समाधान क्या है?
उत्तर:
भारहीनता के कारण अंतरिक्ष यात्री गिलास से पानी नहीं पी सकता है और न ही गिलास से पानी डाल सकता है। इस स्थिति से बचने के लिए अंतरिक्ष यान इस तरह बनाया जाता है कि इसमें खोखले रिम वाले बड़े-बड़े पहिए बनाये जाते हैं, पहियों को घुमा दिया जाता है। इस रिम में बने कैबिन में बैठा यात्री अभिकेन्द्र बल के कारण भार अनुभव करता है।
![]()
दीर्घ उत्तरीय प्रश्न (Long Answer Questions )
प्रश्न 1.
केप्लर के ग्रहीय गति के नियम लिखिए एवं केप्लर के तृतीय नियम से गुरुत्वाकर्षण नियम का सत्यापन कीजिए।
उत्तर:
केप्लर के नियम (Kepler’s Laws)
केप्लर (1571-1630) ने टायको ब्रेह (1546-1601) के द्वारा किये गये प्रहीय प्रेक्षणों का कई वर्षों तक अध्ययन किया और निम्नलिखित तीन नियम प्रस्तुत किये-
प्रथम नियम : प्रत्येक ग्रह सूर्य के चारों ओर दीर्घ-वृत्ताकार कक्षा (elliptical orbit) में परिक्रमण करता है और सूर्य कक्षा की एक नाभि (focus) पर स्थित होता है।
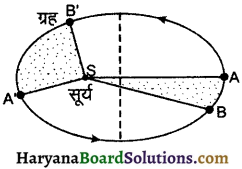
द्वितीय नियम : ग्रह को सूर्य से मिलाने वाली रेखा समान समयान्तराल में समान क्षेत्रफल तय करती है अर्थात् ग्रह की क्षेत्रीय चाल (Areal Speed) नियत रहती है।
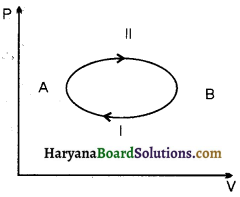
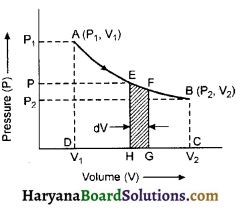
माना ग्रह dt समय में dA क्षेत्रफल प्रस्थार्पित करता है, तो क्षेत्रीय चाल \(\frac{d A}{d t}\) = नियतांक। चित्र में ग्रह को B से A तक जाने में जितना समय लगता है, उतना ही समय B’ से A’ तक जाने में लगता है। अत: क्षेत्रफल SAB = क्षेत्रफल SA’B’ । दोनों क्षेत्रफल समान होने का अर्थ है कि ग्रह की कक्षीय चाल बदलती है। सूर्य से दूर जाने पर कक्षीय चाल घटती है और पास आने पर बढ़ती है। अतः क्षेत्रीय चाल कोणीय संवेग के रूप में लिखने पर घूमते हुए ग्रह का कोणीय संवेग नियत रहता है। अर्थात्
\(\frac{d A}{d t}=\frac{L}{2m}\)
यहाँ L कोणीय संवेग है तथा m ग्रह का द्रव्यमान है।
तृतीय नियम-ग्रह के आवर्त काल का वर्ग ग्रह एवं सूर्य के बीच औसत दूरी के घन के अनुक्रमानुपाती होती है। अर्थात्
T² ∝ r³
या T² = k r³
जहाँ k, एक नियतांक है एवं r, सूर्य एवं ग्रह के मध्य औसत दूरी है।
केप्लर के नियम से न्यूटन के गुरुत्वाकर्षण नियम (Derivation of Newton’s Law of Gravitation from Kepler’s Law) :
न्यूटन ने पाया कि अधिकांश ग्रह सूर्य के परित: लगभग वृत्ताकार कक्षाओं में गति करते हैं। केप्लर के द्वितीय नियम के अनुसार, ग्रह के त्रिज्यीय सदिश की क्षेत्रफलीय चाल नियत रहती है। अत: वृत्ताकार कक्षा में त्रिज्य सदिश की तथा स्वयं ग्रह की रेखीय चाल क्रमशः v तथा ω नियत रहेगी।
माना r त्रिज्या के वृत्ताकार पथ पर गतिशील होने के कारण ग्रह के द्रव्यमान m पर केन्द्र की ओर लगने वाला अभिकेन्द्र बल F लगता है, तो

इस प्रकार केप्लर के नियमों के आधार पर न्यूटन ने निम्नलिखित निष्कर्ष निकाले-
- ग्रहों पर अभिकेन्द्र बल आरोपित होता है जिसकी दिशा सूर्य की ओर होती है।
- इस बल का परिमाण, ग्रह तथा सूर्य के बीच दूरी के वर्ग के व्युत्क्रमानुपाती होती है। (F ∝ \(\frac{1}{r^2}\))
- यह बल ग्रह के द्रव्यमान के अनुक्रमानुपाती है,
(F ∝ m)
प्रश्न 2.
गुरुत्वीय विभव से क्या तात्पर्य है? बिन्दु द्रव्यमान के लिए सूत्र निगमित कीजिए ।
उत्तर:
गुरुत्वीय विभव (Gravitational Potential) :
एकांक द्रव्यमान को अनन्त से किसी बिन्दु तक लाने में जो कार्य करना पड़ता है, उसे उस बिन्दु पर गुरुत्वीय विभव कहते हैं।” ये सदैव ऋणात्मक होता है और अनन्त पर इसका मान शून्य मानते हैं। इसे V से व्यक्त करते हैं। इसका मात्रक Jkg-1 एवं विमीय सूत्र [M0 L2 T-2] है।
किन्हीं दो बिन्दुओं के मध्य गुरुत्वीय विभवान्तर उस कार्य के बराबर है जो एकांक द्रव्यमान को एक बिन्दु से दूसरे बिन्दु तक ले जाने में करना पड़ता है। अत: A व B दो बिन्दुओं के बीच गुरुत्वीय विभवान्तर
\(V_B-V_A=\left(\frac{U_B-U_A}{m}\right)\) …………..(1)
बिन्दु द्रव्यमान के कारण विभव (Potential due to Point Mass) :
माना M द्रव्यमान का कण स्थिति A पर रखा है। कण के केन्द्र से r दूरी पर बिन्दु P है जिस पर हमें कण के कारण गुरुत्वीय विभव ज्ञात करना है। बिन्दु P की स्थिति r का फलन है अत: इस बिन्दु पर गुरुत्वीय विभव भी r का फलन होगा। अत: P पर गुरुत्वीय विभव-

![]()
प्रश्न 3.
गुरुत्वीय विभव से क्या तात्पर्य है? किसी ठोस गोलाकार पिण्ड के कारण विभिन्न स्थितियों में गुरुत्वीय विभव के लिए सूत्र निगमित कीजिए ।
उत्तर:
गुरुत्वीय विभव (Gravitational Potential) :
एकांक द्रव्यमान को अनन्त से किसी बिन्दु तक लाने में जो कार्य करना पड़ता है, उसे उस बिन्दु पर गुरुत्वीय विभव कहते हैं।” ये सदैव ऋणात्मक होता है और अनन्त पर इसका मान शून्य मानते हैं। इसे V से व्यक्त करते हैं। इसका मात्रक Jkg-1 एवं विमीय सूत्र [M0 L2 T-2] है।
किन्हीं दो बिन्दुओं के मध्य गुरुत्वीय विभवान्तर उस कार्य के बराबर है जो एकांक द्रव्यमान को एक बिन्दु से दूसरे बिन्दु तक ले जाने में करना पड़ता है। अत: A व B दो बिन्दुओं के बीच गुरुत्वीय विभवान्तर
\(V_B-V_A=\left(\frac{U_B-U_A}{m}\right)\) …………..(1)
किसी ठोस गोलाकार पिण्ड के कारण गुरुत्वीय विभव (Gravitational Potential Due to Solid Sphere) :
माना M द्रव्यमान एवं R त्रिज्या का एक ठोस गोला है जिसका केन्द्र O है। किसी बाहरी बिन्दु पर गुरुत्वीय विभव ज्ञात करने के लिए गोले को बिन्दु द्रव्यमान माना जा सकता है।
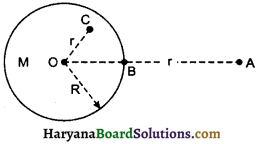

प्रश्न 4.
खोखले गोले के कारण उसके बाहर पृष्ठ पर एवं उसके अन्दर गुरुत्वीय विभव के लिए सूत्र प्राप्त कीजिए ।
उत्तर:
गोलीय कोश के कारण गुरुत्वीय विभव (Gravitational Potential due to Hollow Sphere):
1. बाह्य बिन्दु A पर (r > R) गुरुत्वीय विभव
\(V_{\text {out }}=-\frac{G M}{r}\) ………..(7)
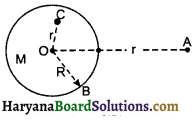
2. पृष्ठ पर स्थित बिन्दु (r = R) पर गुरुत्वीय विभव-
\(V_s=-\frac{G M}{R}\) ………….(8)
3. गोले के आन्तरिक बिन्दु C(r < R) पर विभव-
गोले के अन्दर गुरुत्वीय क्षेत्र का मान शून्य होता है। अत: एकांक द्रव्यमान को पृष्ठ के अन्दर एक स्थान से दूसरे स्थान तक ले जाने में कोई अतिरिक्त कार्य नहीं करना पड़ता है। अतः अन्दर किसी बिन्दु पर गुरुत्वीय वभव वही होगा जो उसके पृष्ठ पर होता है।
∴ \(V_{\text {in }}=-\frac{G M}{R}\) ……….(9)
खोखले गोले के कारण दूरी के साथ गुरुत्वीय विभव में परिवर्तन निम्न चित्र (8.23) में प्रदर्शित है।
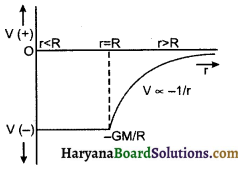
![]()
प्रश्न 5.
एक कृत्रिम उपग्रह पृथ्वी के निकट निश्चित वृत्तीय कक्षा में चक्कर लगा रहा है। सिद्ध कीजिए कि इसका परिक्रमण काल \(T=\sqrt{\frac{3π}{ρG}}\) होगा, जहाँ ρ पृथ्वी का घनत्व एवं G गुरुत्वाकर्षण नियतांक है।
उत्तर:
उपग्रह का परिक्रमण काल (Revolution Period of Satellite):
उपग्रह अपने ग्रह के चारों ओर एक चक्कर लगाने में जितना समय लेता है, उसे उपग्रह का परिक्रमण काल कहते हैं।
यदि उपग्रह का परिक्रमण काल T हो, तो
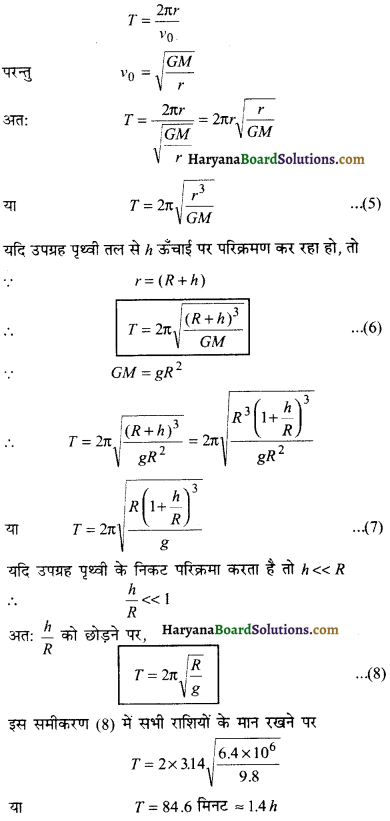
\(T=2π \sqrt{\frac{(R+h)^3}{GM}}\)
उपग्रह पृथ्वी के अति निकट परिक्रमा करता है अत: h<< R
h को R की तुलना में छोड़ने पर-

प्रश्न 6.
उपग्रह की ऊर्जा एवं बन्धन ऊर्जा से क्या अभिप्राय है?
इनके लिए सूत्र प्राप्त कीजिए ।
उत्तर:
उपग्रह की ऊर्जा (Energy of Satellite)
अपनी कक्षा में परिक्रमण करते समय उपग्रह की कक्ष्पिय चाल के कारण उसमें गतिज ऊर्जा होती है और उसकी स्थिति के कारण स्थितिज ऊर्जा होती है। इन दोनों प्रकार की ऊर्जाओं का योग उपग्रह की कुल ऊर्जा होती है।

स्पष्ट है कि कुल ऊर्जा ऋणात्मक होती है जिसका अभिप्राय है कि उपग्रह ग्रह के साथ बद्ध निकाय है। इसे मुक्त करने के लिए बाह्य ऊर्जा की आवश्यकता होती है।
उपग्रह की बन्धन ऊर्जा (Binding Energy of Satellite) :
“ऊर्जा की वह न्यूनतम मात्रा जो किसी उपग्रह को दे देने पर उपग्रह सदैव के लिए अपनी कक्षा छोड़कर चला जाये अर्थात् पलायन कर जाये, उपग्रह की बन्धन ऊर्जा कहलाती है।’ इसे Eb से व्यक्त करते हैं।
उपग्रह की कुल ऊर्जा, E_t=-\frac{1}{2} \frac{G M m}{r}
उपग्रह जब पलायन कर जायेगा तो अनन्त पर उसकी ऊर्जा शून्य हो जायेगी। अत: उपग्रह की बन्धन ऊर्जा
\(E_b=E_{\infty}-E_t=0-\left[-\frac{1}{2} \frac{G M m}{r}\right]\)
या \(E_b=\frac{1}{2} \frac{G M m}{r}\)
![]()
प्रश्न 7.
सिद्ध कीजिए कि पलायन वेग पिण्ड के द्रव्यमान पर निर्भर नहीं करता है।
उत्तर:
पलायन वेग (Escape Velocity) :
“वह न्यूनतम वेग जिससे फेंके जाने पर कोई वस्तु पलायन कर जाये अर्थात् पृथ्वी की गुरुत्वाकर्षण सीमा के बाहर चली जाये और लौटकर वापस न आ सके, पलायन वेग कहलाता है।’ इसकी कोई निश्चित दिशा नहीं होती है। अत: इसे पलायन वेग न कहकर पलायन चाल कहना अधिक यथार्थ होगा। आदतन हम इसे पलायन वेग कह देते हैं।
(i) पृथ्वी सतह से पलायन वेग के लिए सूत्र-हम जानते हैं कि जब किसी वस्तु को पृथ्वी सतह से दूर की ओर फेंका जाता है तो उसकी गतिज ऊर्जा गुरुत्वीय स्थितिज ऊर्जा में बदलने लगती है और जहाँ पर सम्पूर्ण गतिज ऊर्जा गुरुत्वीय स्थितिज ऊर्जा में बदल जाती है, वहीं से वस्तु वापस लौट आती है। इस आधार पर स्पष्ट है कि यदि वस्तु को पृथ्वी सतह से उसकी गुरुत्वीय स्थितिज ऊर्जा के बराबर गतिज ऊर्जा दे दी जाये तो वह अनन्त पर पहुँच जायेगी अर्थात पलायन कर जायेगी। अत:
पलायन ऊर्जा = गुरुत्वीय स्थितिज ऊर्जा का परिमाण

![]()
प्रश्न 8.
न्यूटन का गुरुत्वाकर्षण नियम लिखिए एवं सार्वत्रिक गुरुत्वाकर्षण नियतांक (G) की परिभाषा, मात्रक एवं विमीय सूत्र ज्ञात कीजिए।
उत्तर;
गुरुत्वाकर्षण का सार्वत्रिक नियम (Universal Law of Gravitation) इस नियम के अनुसार, “बह्माण्ड में प्रत्येक द्रव्य कण किसी भी अन्य द्रव्य कण को अपनी ओर एक बल द्वारा आकर्षित करता है जिसका मान (परिमाण) दोनों कणों के द्रव्यमानों के गुणनफल के अनुक्रमानुपाती एवं उनके द्रव्यमान केन्द्रों के बीच की दूरी के वर्ग के व्युत्क्रमानुपाती होता है।” इस बल की दिशा दोनों कण्णों को मिलाने वाली रेखा की सीध में होती है।

माना m1 व m2 द्रव्यमान के दो कण परस्पर r दूरी पर चित्र के अनुसार हैं।
यदि इन दोनों के मध्य लगने वाला गुरुत्वाकर्षण बल F हो तो उक्त गुरुत्वाकर्षण बल के नियमानुसार
एवं \(F \propto m_1 m_2\)
\(F \propto \frac{1}{r^2}\)
दोनों नियमों को मिलाने पर
या \(F \propto \frac{m_1 m_2}{r^2}\)
या \(F=G \frac{m_1 m_2}{r^2}\) ……….(1)
जहाँ G एक नियतांक है जिसे सार्वत्रिक गुरुत्वाकर्षण नियतांक (Universal Constant of Gravity) कहते हैं। खगोलीय पिण्डों या पृथ्वी व सूर्य के मध्य दूरी इनके व्यास की तुलना में अत्यधिक होने के कारण इन्हें कण माना जा सकता है। अतः समीकरण (1) ऐसी समस्याओं पर भी लागू होता है।
सार्वत्रिक गुरुत्वाकर्षण नियतांक (G):
1. परिभाषा-
∵ गुरुत्वाकर्षण बल, \(F=G \frac{m_1 m_2}{r^2}\)
यदि m1 = m2 = 1, r = 1 तो F = G
अर्थात् “सार्वत्रिक गुरुत्वाकर्षण नियतांक उस गुरुत्व बल के तुल्य है जो एकांक द्रव्यमान के दो कणो के मध्य एकांक दूरी पर कार्य करता है।”

![]()
प्रश्न 9.
पृथ्वी का उपग्रह पृथ्वी के चारों ओर क्यों घूमता है? इसके आवर्तकाल एवं कक्षीय चाल के लिए सूत्रों का निगमन कीजिए।
उत्तर;
उपग्रह की कक्षीय चाल, परिक्रमण काल एवं कुल ऊर्जा (Orbital Speed, Period of Revolution and Total Energy):
उपग्रह (Satellite):
वे आकाशीय पिण्ड जो ग्रहों की परिक्रमा करते हैं, उपग्रह कहलाते हैं। ये दो प्रकार के होते हैं-
(1) प्राकृतिक उपग्रह (Natural Satellites)
उदाहरण-चन्द्रमा पृथ्वी का प्राकृतिक उपग्रह है।
(2) कृत्रिम उपग्रह (Artificial Satellites)
उदाहरण-सभी मानव निर्मित उपग्रह कृत्रिम उपग्रह की श्रेणी में आते हैं; जैसे-INSAT-1A, IB; EDUSAT; G-SAT आदि।
उपग्रह का कक्षीय वेग (Orbital Velocity of Satellite) :
माना m द्रव्यमान का उपग्रह पृथ्वी (द्रव्यमान M ) सतह से h ऊँचाई पर vo कक्षीय चाल से पृथ्वी की परिक्रमा करता है। उपग्रह की कक्षा की त्रिज्या,
r = (R + h)
पृथ्वी एवं उपग्रह के मध्य लगने वाला गुरुत्वाकर्षण बल आवश्यक अभिकेन्द्रीय बल प्रदान करता है।
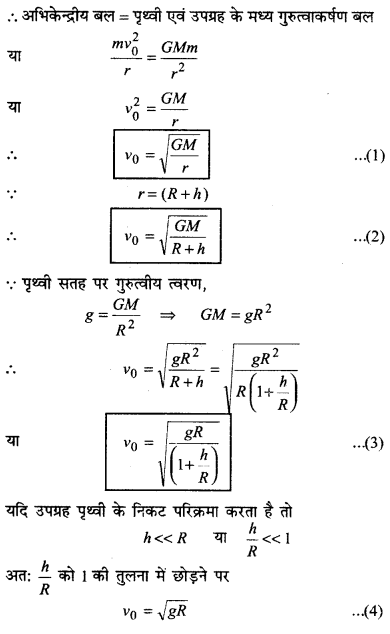
![]()
आंकिक प्रश्न (Numerical Questions) :
गुरुत्वाकर्षण नियम पर आधारित प्रश्न
प्रश्न 1,.
M, 2M, 3M, 4M द्रव्यमान के चार कण a भुजा वाले वर्ग के शीर्षों पर रखे गये हैं तो वर्ग केन्द्र पर रखे M द्रव्यमान वाले कण पर लगने वाला गुरुत्वाकर्षण बल ज्ञात कीजिए।
उत्तर;
\(\frac{4 \sqrt{2} G M^2}{a^2}\)
प्रश्न 2.
दो गोलों के द्रव्यमान 60 kg तथा 50 kg हैं। इनके गुरुत्व केन्द्रों के बीच की दूरी 0.50m है। इनके बीच कितना गुरुत्वाकर्षण बल होगा?
उत्तर:
8.0 × 10-7 N
प्रश्न 3.
M द्रव्यमान का एक समरूप गोला तथा m द्रव्यमान और L लम्बाई की एक समरूप छड़ इस प्रकार रखे गये हैं कि छड़ का पास वाला सिरा गोले के केन्द्र से r दूरी पर स्थित हो तो गोले व छड़ के मध्य लगने वाले गुरुत्वाकर्षण बल की गणना कीजिए।
उत्तर:
\(\frac{GMm}{r(r+L)}\)
![]()
गुरुत्वीय त्वरण पर आधारित प्रश्न
प्रश्न 4.
एक व्यक्ति का पृथ्वी तल पर भार 80 kg है। इस व्यक्ति का चन्द्रमा पर भार क्या होगा? दिया है, चन्द्रमा का द्रव्यमान 7.34 × 1022 kg त्रिज्या = 1.75 × 106 m; गुरुत्वीय नियतांक = 6.67 × 10-11 Nm.kg-2 व्यक्ति का चन्द्रमा पर द्रव्यमान क्या होगा?
उत्तर:
128 N; 80 kg
प्रश्न 5.
यदि पृथ्वी का व्यास उसके वर्तमान व्यास का आधा हो जाये तथा घनत्व वही रहे तो इस आहे आकार की पृथ्वी की सतह पर ‘8 का मान कितना होगा?
उत्तर:
4.90 ms
प्रश्न 6.
किसी व्यक्ति का पृथ्वी पर भार 490 N है। पृथ्वी पर . गुरुत्वीय त्वरण g 9.8 Nkg है। चन्द्रमा की सतह पर गुरुत्वीय त्वरण & है। ज्ञात कीजिए-
(i) चन्द्रमा की सतह पर व्यक्ति का भार ।
(ii) पृथ्वी व चन्द्रमा पर व्यक्ति का द्रव्यमान ।
(iii) यदि व्यक्ति पृथ्वी सतह पर 1 min में 150 m चलता है तो चन्द्रमा पर मिनट में कितना चलेगा?
(iv) यदि व्यक्ति पृथ्वी तल पर 2 mm कूद सकता हो चन्द्रमा पर कितना कूदेगा?
उत्तर:
(i) 81.67 N;
(ii) पृथ्वी व चन्द्रमा दोनों पर द्रव्यमान
(iii) 150m;
(iv) 12m ]
गुरुत्वीय त्वरण में परिवर्तन पर आधारित
प्रश्न 7.
पृथ्वी की सतह से / ऊंचाई तक जाने पर किसी वस्तु के भार में 1% कमी आती है। यदि वस्तु के सतह से / गहराई नीचे ले जाया जाये तो भार में परिवर्तन कितना होगा?
जिससे
उत्तर:
0.5%
प्रश्न 8.
अपनी अक्ष पर पृथ्वी के घूर्णन की चाल ज्ञात कीजिए। ‘भूमध्य रेखा पर किसी व्यक्ति का भार इस समय के भार का
जाये। भूमध्य रेखा पर पृथ्वी की त्रिज्या 6400 किमी है।
उत्तर:
5.53 x 104 रेडियन / से०
![]()
प्रश्न 9.
किस ऊँचाई पर गुरुत्वीय त्वरण का मान पृथ्वी की के मान का (i) 4% तथा (ii) 50% होगा? पृथ्वी की त्रिज्या 6400 km है।
उत्तर:
(i) 25600 km;
(ii) 2649.6 km
प्रश्न 10.
पृथ्वी तल से कितना नीचे जाने पर गुरुत्वीय त्वरण पृथ्वी पर गुरुत्वीय त्वरण का (i) आधा रह जायेगा (ii) एक चौथाई रह जायेगा ? (पृथ्वी की त्रिज्या = 6400km )
उत्तर:
(i) 3200 km
(ii) 4800km
गुरुत्वीय क्षेत्र तथा गुरुत्वीय विभव पर आधारित प्रश्न
प्रश्न 11.
चन्द्रमा तथा पृथ्वी के बीच की औसत दूरी 3.85 × 108 m है। दोनों के मध्य किस स्थान पर गुरुत्वीय क्षेत्र की तीव्रता शून्य होगी?
(दिया है- पृथ्वी का द्रव्यमान = 5.96 × 1024 kg: चन्द्रमा का द्रव्यमान 7.36 ×1022 kg)
उत्तर:
पृथ्वी के केन्द्र से 3.465 × 108 m
प्रश्न 12.
2 किग्रा द्रव्यमान का एक कण 1.0 मी त्रिज्या तथा 100 किग्रा द्रव्यमान के एक समान गोले पर रखा है। गोले के पृष्ठ पर गुरुत्वीय विभव ज्ञात करो तथा कण को दूर करने में गुरुत्वाकर्षण के विरुद्ध किया गया कार्य ज्ञात कीजिए।
उत्तर:
V = 6.67 × 10-9 J/kg, W = 1.3340 × 10-8 J
प्रश्न 13.
(i) चन्द्रमा तथा पृथ्वी के बीच की दूरी 3.85 × 108 m है। दोनों के मध्य किस बिन्दु पर गुरुत्वीय बल क्षेत्र शून्य होगा? (पृथ्वी का द्रव्यमान = 6 × 1024 kg; चन्द्रमा का द्रव्यमान = 7.5 × 1022 kg)
(ii) इस बिन्दु पर गुरुत्वीय विभव कितना होगा?
उत्तर:
(i) पृथ्वी के केन्द्र से 3.46 × 108 cm;
(ii) -1.30 × 106 J.kg-1
गुरुत्वीय स्थितिज ऊर्जा पर आधारित प्रश्नं
प्रश्न 14.
पृथ्वी का द्रव्यमान 6.0 × 1024 kg तथा त्रिज्या 6.4 × 106 m है।
(i) 4 kg के एक पिण्ड को पृथ्वी तल से अनन्त तक ले जाने में कितना कार्य करना होगा?
(ii) 4kg के पिण्ड की पृथ्वी तल पर गुरुत्वीय स्थितिज ऊर्जा कितनी होगी?
(iii) पृथ्वी तल पर गुरुत्वीय विभव कितना होगा?
(iv) यदि पिण्ड अनन्त से पृथ्वी तल पर गिरे तो पृथ्वी तल से टकराते समय पिण्ड का वेग क्या होगा?
(G = 6.67 × 10-11 N.m²kg-2)
उत्तर:
(i) 2.5 × 108 J;
(ii) -2.5 × 108 J;
(iii) -6.25 × 107 J.kg-1;
(iv) 11.18 × 10³ ms-1
प्रश्न 15.
200g द्रव्यमान के तीन कण अनन्त से लाकर किसी समबाहु त्रिभुज के शीर्षो पर रखे जाते हैं। यदि त्रिभुज की प्रत्येक भुजा 40 cm हो तो किया गया कार्य कितना होगा?
उत्तर:
2.0 × 10-11 J
![]()
उपग्रह की कक्षीय चाल, पलायन वेग तथा परिक्रमण काल पर आधारित प्रश्न
प्रश्न 16.
यदि पृथ्वी का द्रव्यमान और त्रिज्या किसी ग्रह की क्रमशः 9 गुनी तथा दुगुनी है तो रॉकेट को इस ग्रह के गुरुत्वाकर्षण बल से बाहर निकालने के लिए आवश्यक न्यूनतम वेग की गणना कीजिए। पृथ्वी की सतह पर पलायन वेग 11.2 km.s-1 लीजिए।
उत्तर:
5.28k.ms-1
प्रश्न 17.
m द्रव्यमान का एक पिण्ड पृथ्वी की सतह से 4R ऊंचाई पर स्थित है, जहाँ R पृथ्वी की त्रिज्या है। पिण्ड को कितना न्यूनतम वेग दिया जाये कि वह पलायन कर जाये?
उत्तर:
प्रश्न 18.
पृथ्वी के समीप उसकी परिक्रमा करने वाले उपग्रह के कक्षीय वेग की गणना कीजिए। यदि पृथ्वी की त्रिज्या 6.4 × 106 m तथा गुरुत्वीय त्वरण 10 ms-2 हो। यदि उपग्रह पृथ्वी तल से 2000 km की ऊँचाई पर रहे तब कक्षीय वेग कितना होगा?
उत्तर:
8 km.s-1; 6.98 kms-1
उपग्रह द्वारा प्राप्त ऊँचाई पर ऊर्जा पर आधारित
प्रश्न 19.
500g के पिण्ड को पृथ्वी से पलायन करने के लिए कितनी आवश्यक ऊर्जा ज्ञात कीजिए। (g = 10 ms-2 तथा पृथ्वी की from Re = 6400 km)
उत्तर:
3.2 × 107 J
![]()
प्रश्न 20.
किसी पिण्ड को पृथ्वी तल से किस वेग से फेंका जाये कि वह (i) 2Re; (ii) 4Re ऊँचाई तक पहुँच जाये? (पृथ्वी त्रिज्या R = 6400km; g = 10 ms-1)
उत्तर:
(i) 9.24 km.s-1;
(ii) 10.11 km.s-1
प्रश्न 21.
500kg का एक कृत्रिम उपग्रह पृथ्वी से 1800 km की ऊंचाई पर पृथ्वी का चक्कर लगा रहा है। उपग्रह की (i) स्थितिज ऊर्जा, (ii) गतिज ऊर्जा, (iii) कुल ऊर्जा ज्ञात कीजिए।
उत्तर:
दिया है- पृथ्वी की त्रिज्या 6400 km तथा g = 10 ms-1
(i) 2.5 × 1010 J;
(ii) 1.25 × 1010 J;
(iii) -1.25 × 1010 J
केप्लर के नियमों पर आधारित प्रश्न
प्रश्न 22.
नेप्चून ग्रह की सूर्य से दूरी पृथ्वी से सूर्य की दूरी की 30 गुनी है। पृथ्वी का परिक्रमण काल 1 वर्ष है। नेप्चून के परिक्रमण काल की गणना कीजिए।
उत्तर:
164.3 वर्ष
प्रश्न 23.
बृहस्पति ग्रह की सूर्य से दूरी पृथ्वी की सूर्य से दूरी की 5.2 गुनी है तो बृहस्पति के घूर्णन का आवर्त्तकाल ज्ञात कीजिए।
उत्तर:
11.86 वर्ष
HBSE 11th Class Physics Important Questions Chapter 8 गुरुत्वाकर्षण Read More »