Haryana State Board HBSE 12th Class Chemistry Solutions Chapter 7 p-ब्लॉक के तत्व Textbook Exercise Questions and Answers.
Haryana Board 12th Class Chemistry Solutions Chapter 7 p-ब्लॉक के तत्व
प्रश्न 7.1.
वर्ग 15 के तत्वों के सामान्य गुणधर्मों की उनके इलेक्ट्रॉनिक विन्यास, ऑक्सीकरण अवस्था, परमाण्विक आकार, यथैी तथा विद्युत्ऋणात्मकता के संदर्भ में विवेचना कीजिए ।
उत्तर:
वर्ग 15 के तत्वों के सामान्य गुणधर्म निम्नलिखित हैं-

(i) इलेक्ट्रॉनिक विन्यास – वर्ग 15 के तत्वों का संयोजकता कोश का इलेक्ट्रॉनिक विन्यास, ns2np3 होता है। इन तत्वों के s कक्षक पूर्णतया भरे होते हैं तथा p कक्षक अर्धपूरित (Half filled) होते हैं, जिससे इनका इलेक्ट्रॉनिक विन्यास अधिक स्थायी होता है।
(ii) ऑक्सीकरण अवस्था – वर्ग 15 के तत्वों की सामान्य ऑक्सीकरण अवस्थाएँ – 3 +3 तथा +5 हैं। परमाणु आकार तथा धातु गुणों में वृद्धि के कारण वर्ग में नीचे जाने पर 3 ऑक्सीकरण अवस्था दर्शाने की प्रवृत्ति कम होती है । वर्ग में नीचे जाने पर +5 ऑक्सीकरण अवस्था का स्थायित्व घटता है।
बिस्मथ [V] का एक ही यौगिक BiF5 ज्ञात है । वर्ग में नीचे की ओर +5 ऑक्सीकरण अवस्था के स्थायित्व में कमी के साथ-साथ ऑक्सीकरण अवस्था ( अक्रिय युग्म प्रभाव के कारण) के स्थायित्व में होती है। ऑक्सीजन के साथ अभिक्रिया से बने यौगिकों में नाइट्रोजन +1, +2, +4 ऑक्सीकरण अवस्थाएँ भी दर्शाती है। फॉस्फोरस भी कुछ ऑक्सो अम्लों में, +1 तथा +4 ऑक्सीकरण अवस्थाएँ दर्शाता है।
नाइट्रोजन की अधिकतम सहसंयोजकता 4 हो सकती है; क्योंकि केवल 4 कक्षक (एक s तथा तीन p) ही बंधन के लिए उपलब्ध हैं। भारी तत्वों के बाह्यतम कोश में रिक्त d कक्षक पाए जाते हैं, जो बंध बनाने के लिए प्रयुक्त किए जा सकते हैं, अतः उनकी सहसंयोजकता बढ़ जाती है। जैसे PF–6 में फॉस्फोरस की संयोजकता 6 है।
(iii) परमाण्विक आकार – वर्ग 15 में नीचे जाने पर परमाणु आकार (सहसंयोजी त्रिज्या) में वृद्धि होती है। N से P तक त्रिज्या में पर्याप्त वृद्धि होती है जबकि As से Bi तक त्रिज्या में वृद्धि अपेक्षाकृत कम होती है। इसका कारण भारी तत्वों में पूर्ण भरे d और / या f कक्षकों की उपस्थिति है।
(iv) आयनन एन्थैल्पी – वर्ग 15 के तत्वों की आयनन एन्थैल्पी, वर्ग 14 तथा वर्ग 16 के संगत तत्वों की आयनन एन्थैल्पी से अधिक होती है क्योंकि इन तत्वों में अर्धपूरित स्थायी विन्यास (np3) होता है। सामान्यतः आवर्त में बाएँ से दाएँ जाने पर आयनन एन्थैल्पी बढ़ती है क्योंकि परमाणु आकार कम होता है तथा प्रभावी नाभिकीय आवेश बढ़ता है।
अतः बाह्यतम इलेक्ट्रॉन अधिक आकर्षण बल से बंधे होते हैं जिन्हें पृथक् करने के लिए अधिक ऊर्जा की आवश्यकता होती है। वर्ग में नीचे की ओर जाने पर आयनन एन्थैल्पी का मान कम होता है क्योंकि परमाणु आकार में वृद्धि होती है। इन तत्वों के लिए विभिन्न आयनन एल्पियों का क्रम निम्न प्रकार होता है-
△iH1 < △iH2 < △iH3
अर्थात् एक इलेक्ट्रॉन निकालने के बाद द्वितीय तथा तृतीय इलेक्ट्रॉन को निकालने के लिए अधिक ऊर्जा की आवश्यकता होती है।
(v) विद्युतऋणात्मकता – सामान्यतः वर्ग में नीचे जाने पर परमाणु आकार में वृद्धि के कारण विद्युतॠणात्मकता का मान घटता है, लेकिन भारी तत्वों में यह अंतर बहुत कम होता है।
![]()
प्रश्न 7.2.
नाइट्रोजन की क्रियाशीलता फॉस्फोरस से भिन्न क्यों है?
उत्तर:
नाइट्रोजन की क्रियाशीलता फॉस्फोरस से भिन्न होती है। इसके निम्नलिखित कारण हैं-
(i) नाइट्रोजन का आकार बहुत छोटा होता है तथा इसकी विद्युतॠणता एवं आयनन एन्थैल्पी, फॉस्फोरस की तुलना में बहुत अधिक है।
(ii) नाइट्रोजन के संयोजी कोश में रिक्त d कक्षक उपलब्ध नहीं हैं जबकि फॉस्फोरस के संयोजी कोश में रिक्त d कक्षक होते हैं।
(iii) नाइट्रोजन में pπ -pπ अतिव्यापन द्वारा त्रिआबन्ध बनाने की प्रवृत्ति होती है अतः इसकी बन्ध एन्थैल्पी बहुत अधिक होती है जिसके कारण यह बहुत कम क्रियाशील होती है जबकि फॉस्फोरस में pπ – pπ अतिव्यापन नहीं होता।
प्रश्न 7.3.
वर्ग 15 के तत्वों की रासायनिक क्रियाशीलता की प्रवृत्ति की विवेचना कीजिए ।
उत्तर:
वर्ग 15 के तत्वों की रासायनिक क्रियाशीलता में बहुत अन्तर होता है। नाइट्रोजन की बन्ध एन्थैल्पी का मान बहुत उच्च होने के कारण यह लगभग अक्रिय होती है। फॉस्फोरस का एक अपररूप, श्वेत फॉस्फोरस बहुत अधिक क्रियाशील होता है जिसका कारण P4 की संरचना में कोणीय तनाव ( angular strain) है। यह वायु में तेजी से आग पकड़कर P4O10 बनाता है जिसके श्वेत धूम बनते हैं। लाल फॉस्फोरस कमरे के ताप पर वायु में स्थायी होता है लेकिन गर्म करने पर क्रिया करता है।
As, Sb तथा Bi (भारी तत्व) कम क्रियाशील होते हैं। आर्सेनिक शुष्क वायु में स्थायी होता है लेकिन इसे वायु में गर्म करने पर यह 615°C पर ऊर्ध्वपातित होकर As4O6 बनाता है । एन्टिमनी वायु तथा जल के प्रति स्थायी होता है लेकिन वायु में गर्म करने पर यह Sb4O6, Sb4O8 या Sb4O10 बनाता है। Bi को वायु में गर्म करने पर यह Bi2O3 बनाता है।
प्रश्न 7.4.
NH3 हाइड्रोजन बंध बनाती है परन्तु PH3 नहीं बनाती। क्यों ?
उत्तर:
नाइट्रोजन के छोटे आकार तथा उच्च विद्युतॠणता के कारण N-H बन्ध, अधिक ध्रुवीय होता है अतः NH3 हाइड्रोजन बंध बनाती है जबकि फॉस्फोरस का आकार बड़ा होता है तथा इसकी विद्युतॠणता भी कम होती है अतः P-H बन्ध लगभग अध्रुवीय होता है इसलिए PH3 में हाइड्रोजन बन्ध नहीं बनता ।
प्रश्न 7.5.
प्रयोगशाला में नाइट्रोजन कैसे बनाते हैं? सम्पन्न होने वाली अभिक्रिया के रासायनिक समीकरणों को लिखिए।
उत्तर:
(i) प्रयोगशाला में नाइट्रोजन बनाने के लिए अमोनियम क्लोराइड के जलीय विलयन की सोडियम नाइट्राइड के साथ अभिक्रिया कराई जाती है-
NH4Cl(aq) + NaNO2(aq) → N2(g) + 2H2O(l) + NaCl(aq)
इस अभिक्रिया में थोड़ी मात्रा में NO तथा HNO3 भी बनते हैं; इन अशुद्धियों को दूर करने के लिए गैस को पोटैशियम डाइक्रोमेट युक्त सल्फ्यूरिक अम्ल के जलीय विलयन में से प्रवाहित किया जाता है।
(ii) अमोनियम डाइक्रोमेट के ताप अपघटन से भी नाइट्रोजन गैस प्राप्त होती है-
![]()
(iii) बेरियम ऐजाइड के ताप अपघटन से अति शुद्ध नाइट्रोजन प्राप्त होती है-
Ba(N3)2 → Ba + 3N2
प्रश्न 7.6.
अमोनिया का औद्योगिक उत्पादन कैसे किया जाता है ?
उत्तर:
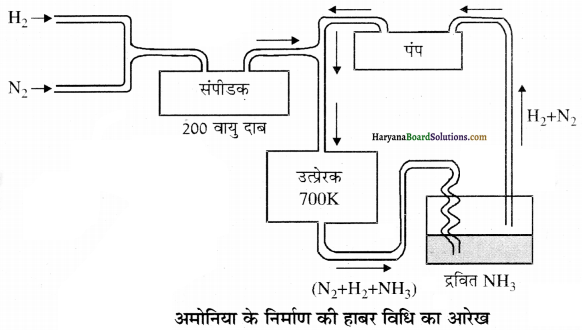
अमोनिया का औद्योगिक निर्माण हाबर प्रक्रम द्वारा किया जाता है-
![]()
अमोनिया के अधिक निर्माण के लिए आवश्यक शर्तें – अमोनिया के निर्माण की अभिक्रिया उत्क्रमणीय तथा ऊष्माक्षेपी होती है। इसके साथ ही अभिक्रिया के कारण आयतन में कमी होती है अतः ले शातैलिए के सिद्धान्त के आधार पर उच्च दाब अमोनिया के अधिक निर्माण में सहायक होगा। अतः अमोनिया के निर्माण के लिए अनुकूलतम शर्तें निम्नलिखित हैं-
(i) लगभग 200 वायुमंडलीय दाब ( 200 × 105 Pa )
(ii) लगभग 700K ताप
(iii) K2O तथा Al2O3 युक्त आयरन ऑक्साइड उत्प्रेरक
(iv) शुद्ध N2 तथा H2 का प्रयोग |
अमोनिया में उपस्थित नमी को CaO द्वारा दूर कर लिया जाता है।
प्रश्न 7.7.
उदाहरण देकर समझाइए कि कॉपर धातु HNO3 के साथ अभिक्रिया करके किस प्रकार भिन्न उत्पाद दे सकती है?
उत्तर:
कॉपर धातु की HNO3 के साथ अभिक्रिया ताप तथा सांद्रता पर निर्भर करती है तथा इन अभिक्रियाओं में कॉपर का ऑक्सीकरण होता है-
(i) कॉपर की तनु तथा ठंडे HNO3 से क्रिया कराने पर कॉपर नाइट्रेट तथा नाइट्रिक ऑक्साइड बनते हैं।
![]()
(ii) कॉपर की सान्द्र तथा गर्म HNO3 से क्रिया कराने पर कॉपर नाइट्रेट तथा नाइट्रोजन डाइऑक्साइड प्राप्त होते हैं।
![]()
प्रश्न 7.8.
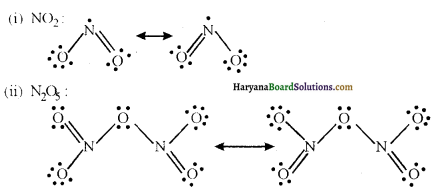
NO2 तथा N2O5 की अनुनादी संरचनाओं को लिखिए।
उत्तर:
NO2 तथा N2O5 की अनुनादी संरचनाएँ अग्र हैं-
प्रश्न 7.9.
HNH कोण का मान, HPH, HASH तथा HSH कोणों की अपेक्षा अधिक क्यों है ?
उत्तर:
NH3 में HNH कोण का मान वर्ग के अन्य हाइड्राइडों की तुलना में अधिक होता है क्योंकि NH3 में N पर sp3 संकरण तथा एक एकाकी इलेक्ट्रॉन युग्म होने के कारण बन्ध कोण लगभग 107.8° होता है जबकि वर्ग नीचे जाने पर परमाणु आकार बढ़ने तथा विद्युतॠणता कम होने के कारण sp3 संकरण का प्रभाव कम होता जाता है अर्थात् M-H बन्ध बनाने में M के शुद्ध p कक्षक हाइड्रोजन के s कक्षक के साथ अतिव्यापन करते हैं, अतः बन्ध कोण कम होता जाता है।
![]()
प्रश्न 7.10.
R3P = O पाया जाता है जबकि R3N = O नहीं | क्यों ? (R = ऐल्किल समूह)
उत्तर:
नाइट्रोजन के संयोजकता कोश में रिक्त d कक्षक नहीं होता अतः इसकी अधिकतम संयोजकता 4 होती है तथा यह dπ – pπ बन्ध नहीं बना सकता अतः R3N = O नहीं पाया जाता जबकि फॉस्फोरस के संयोजकता कोश में रिक्त d कक्षक होने के कारण यह dπ – pπ अतिव्यापन द्वारा R3P = O बना लेता है जिसमें फॉस्फोरस की संयोजकता 5 है। (अष्टक का प्रसार)
प्रश्न 7.11.
समझाइए कि क्यों NH3 क्षारकीय है जबकि BiH3 केवल दुर्बल क्षारक है।
उत्तर:
वर्ग 15 के तत्वों के हाइड्राइडों में केन्द्रीय परमाणु पर एकाकी इलेक्ट्रॉन युग्म उपस्थित होने के कारण ये लुइस क्षार होते हैं क्योंकि इनमें इलेक्ट्रॉन युग्म दान करने की प्रवृत्ति होती है। NH3 में नाइट्रोजन के छोटे आकार के कारण इलेक्ट्रॉन घनत्व अधिक होता है अतः इसकी इलेक्ट्रॉन युग्म देने की प्रवृत्ति अधिक होती है इसलिए यह अधिक क्षारीय है जबकि BiH3 में Bi के बड़े आकार के कारण इलेक्ट्रॉन घनत्व कम हो जाता है अतः इसकी इलेक्ट्रॉन युग्म देने की प्रवृत्ति कम होती है इसलिए यह बहुत ही दुर्बल क्षारक है।
प्रश्न 7.12.
नाइट्रोजन द्विपरमाणुक अणु के रूप में पाया जाता है तथा फॉस्फोरस P4 के रूप में। क्यों ?
उत्तर:
नाइट्रोजन द्विपरमाणुक अणु के रूप में पाया जाता है क्योंकि नाइट्रोजन परमाणु के छोटे आकार तथा d कक्षकों की अनुपस्थिति के कारण इसमें बहुल आबन्ध बनाने की प्रवृति होती है जबकि फॉस्फोरस P4 के रूप में पाया जाता है क्योंकि बड़े आकार के कारण इसमें बहुल आबन्ध बनाने की प्रवृत्ति नहीं होती तथा आन्तरिक अबन्धित इलेक्ट्रॉनों के बीच प्रतिकर्षण होता है। इसमें P-P-P बन्ध कोण 60° होता है अतः pπ – pπ बन्ध संभव नहीं है।
प्रश्न 7.13.
श्वेत फॉस्फोरस तथा लाल फॉस्फोरस के गुणों की मुख्य भिन्नताओं को लिखिए।
उत्तर:
श्वेत फॉस्फोरस तथा लाल फॉस्फोरस के गुणों में मुख्य भिन्नताएँ निम्नलिखित हैं-
(i) श्वेत फॉस्फोरस एक पारभासी मोम जैसा श्वेत ठोस होता है जबकि लाल फॉस्फोरस लोहे जैसी धूसर (grey) चमक वाला होता है।
(ii) श्वेत फॉस्फोरस विषैला होता है जबकि लाल फॉस्फोरस गन्धहीन तथा अविषैला होता है।
(iii) श्वेत फॉस्फोरस जल में अविलेय लेकिन कार्बन-डाइ- सल्फाइड में विलेय होता है लेकिन लाल फॉस्फोरस जल तथा कार्बन-डाइ- सल्फाइड दोनों में अविलेय होता है ।
(iv) रासायनिक रूप से लाल फॉस्फोरस श्वेत फॉस्फोरस की तुलना बहुत कम क्रियाशील होता है।
(v) श्वेत फॉस्फोरस अंधेरे में दीप्त होता है, लाल फॉस्फोरस दीप्त नहीं होता !
(vi) श्वेत फॉस्फोरस विविक्त चतुष्फलकीय P4 अणुओं से बना होता है जबकि लाल फॉस्फोरस बहुलकी होता है जिसमें P4 चतुष्फलक श्रृंखला के रूप में एक-दूसरे से जुड़े रहते हैं ।
प्रश्न 7.14.
फॉस्फोरस की तुलना में नाइट्रोजन श्रृंखलन गुणों को कम प्रदर्शित करता है, क्यों?
उत्तर:
नाइट्रोजन परमाणु के छोटे आकार के कारण एक N-N. बन्ध, एक P-P बन्ध की तुलना में दुर्बल होता है क्योंकि N-N बन्ध में अबन्धी इलेक्ट्रॉनों (एकाकी इलेक्ट्रॉनयुग्मों) के मध्य प्रतिकर्षण अधिक होता है। अतः फॉस्फोरस की तुलना में नाइट्रोजन में श्रृंखलन की प्रवृत्ति कम होती है।
प्रश्न 7.15.
H3PO3 की असमानुपातन अभिक्रिया दीजिए।
उत्तर:
H3PO3 को 473K ताप पर गर्म करने पर इसका असमानुपातन होकर फॉस्फोरिक अम्ल (आर्थोफॉस्फोरिक अम्ल) तथा फॉस्फीन बनती है।
4H3PO3 → 3H3PO4 + PH3
प्रश्न 7.16.
क्या PCl5 ऑक्सीकारक और अपचायक दोनों कार्य कर सकता है ? तर्क दीजिए ।
उत्तर:
PCl5 में P की ऑक्सीकरण अवस्था +5 है जो कि उच्चतम है, अतः यह अपनी ऑक्सीकरण अवस्था कम करके ऑक्सीकारक का कार्य कर सकता है लेकिन अपचायक का नहीं।
उदाहरण – PCl5 + 2Ag → 2AgCl + PCl3
प्रश्न 7.17.
O, S, Se, Te तथा Po को इलेक्ट्रॉनिक विन्यास, ऑक्सीकरण अवस्था तथा हाइड्राइड निर्माण के संदर्भ में आवर्त सारणी के एक ही वर्ग में रखने का तर्क दीजिए ।
उत्तर:
(i) इलेक्ट्रॉनिक विन्यास – O, S, Se, Te तथा Po 16वें वर्ग के तत्व हैं। इन सभी का बाह्यतम इलेक्ट्रानिक विन्यास समान है जो कि ns2np4 है अर्थात् इनके बाह्यतम कोश में 6 इलेक्ट्रॉन होते हैं। अतः इन्हें एक ही वर्ग में रखा जाता है।
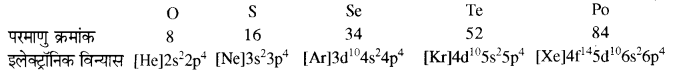
(ii) ऑक्सीकरण अवस्था- ये सभी तत्व – 2 ऑक्सीकरण अवस्था दर्शाते हैं। (Po के अलावा) तथा ऑक्सीजन के अलावा सभी तत्व +2, +4, +6 ऑक्सीकरण अवस्था भी प्रदर्शित करते हैं, ऑक्सीजन केवल +2 अवस्था दर्शाती है। अतः इन्हें एक ही वर्ग में रखा गया है।
(iii) हाइड्राइड निर्माण- सभी तत्व H2E (E= O, S, Se, Te Po) प्रकार के हाइड्राइड बनाते हैं। अतः इन तत्वों को समान वर्ग में रखने का एक कारण यह भी है।
प्रश्न 7.18.
क्यों डाइऑक्सीजन एक गैस है जबकि सल्फर ठोस है?
उत्तर:
ऑक्सीजन परमाणु के छोटे आकार तथा संयोजी कोश में d कश्चकों की अनुपस्थिति के कारण इसमें Pπ – Pπ बन्ध बनाने की प्रबल प्रवृत्ति होती है अतः यह O = O बनाकर अपना अष्टक पूर्ण कर लेता है तथा यह स्वतंत्र अस्तित्व वाले ऑक्सीजन अणुओं (O2) के रूप में गैस अवस्था में पाई जाती है। लेकिन सल्फर के बड़े आकार के कारण S = S बन्ध एन्थैल्पी कम होती है अतः यह S2 न बनाकर Sg के रूप में पाया जाता है जिससे अणुभार बढ़ जाने के कारण अणुओं के मध्य आकर्षण बल बढ़ जाता है। इसी कारण सल्फर ठोस अवस्था में पाया जाता है।
प्रश्न 7.19.
यदि O→O– तथा O→O2- के इलेक्ट्रॉन लब्धि एन्थैल्पी मान पता हो, जो क्रमशः -141 तथा 702 kJ mol-1 हैं, तो आप कैसे स्पष्ट कर सकते हैं कि O2- स्पीशीज वाले ऑक्साइड अधिक बनते हैं न कि O– वाले?
उत्तर:
प्रश्नानुसार O से O– बनने पर ऊर्जा उत्सर्जित होती है। जबकि O– से O-2 बनने पर बहुत अधिक ऊर्जा की आवश्यकता होती है लेकिन O2- स्पीशीज वाले ऑक्साइड अधिक बनते हैं क्योंकि ऑक्साइड बनने पर उत्सर्जित उच्च जालक एन्थैल्पी ( अधिक ऋणावेश के कारण ) द्वितीय उच्च धनात्मक इलेक्ट्रॉन लब्धि एन्थैल्पी की पूर्ति कर देती है।
![]()
प्रश्न 7.20.
कौनसे ऐरोसोल्स ओजोन का क्षय करते हैं?
उत्तर:
ओजोन परत का क्षय करने वाले ऐरोसोल्स निम्नलिखित हैं-
(i) सुपर सोनिक जेट विमानों से उत्सर्जित नाइट्रिक ऑक्साइड (NO), ऊपरी वायुमण्डल में ओजोन परत की सांद्रता को कम करते हैं-
NO(g) + O3(g) → NO2(g) + O2(g)
(ii) ऐरोसोल स्प्रे तथा प्रशीतकों के रूप में प्रयुक्त फ्रेऑन भी ओजोन का क्षय करते हैं-
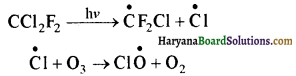
प्रश्न 7.21.
संस्पर्श प्रक्रम ( Contact Process ) द्वारा H2SO4 के उत्पादन का वर्णन कीजिए।
उत्तर:
सम्पर्क विधि (Contact Process ) – इस विधि में तीन पद होते हैं-
(i) सल्फर अथवा सल्फाइड अयस्कों को वायु में जलाकर सल्फर डाइऑक्साइड (SO2) बनाना ।
(ii) V2O5 उत्प्रेरक की उपस्थिति में SO2 की ऑक्सीजन के साथ अभिक्रिया कराकर SO3 में परिवर्तित करना ।
(iii) SO3 को सल्फ्यूरिक अम्ल में अवशोषित करके ओलियम (H2S2O7) प्राप्त करना तथा इसके तनुकरण से H2SO4 प्राप्त करना ।
(i) SO2 बनाना – सल्फर या FeS2 को वायु के साथ गर्म करके SO2 का निर्माण किया जाता है।
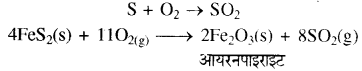
प्राप्त SO2 को धूल के कणों तथा आर्सेनिक यौगिकों की अशुद्धियों से मुक्त कर लिया जाता है। इसके लिए जिलेटिनी FerOH3 प्रयुक्त करते हैं।
![]()
प्रश्न 7.22.
SO2 किस प्रकार से एक वायु प्रदूषक है?
उत्तर:
SO2 ऍक हानिकारक गैसीय प्रदूषक है। वायुमण्डल में उपस्थित SO2, प्रकाश की उपस्थिति में आक्सीकृत होकर SO3 बनाती है जो कि नमी की उपस्थिति में H2SO4 बनाती है जो कि अम्ल वर्षा के रूप में नीचे आती है।
![]()
SO2 पेड़ों की पत्तियों को नुकसान पहुंचाती है तथा मनुष्य की आँखों तथा श्वसन तंत्र के लिए भी हानिकारक है।
प्रश्न 7.23.
हैलोजन प्रबल ऑक्सीकारक क्यों होते हैं?
उत्तर:
हैलोजनों की उच्च विद्युतॠणता तथा अधिक इलेक्ट्रॉन बन्धुता (उच्च ऋणात्मक इलेक्ट्रॉन लब्धि एन्थैल्पी) के कारण इनमें इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति अधिक होती है तथा इनके मानक इलैक्ट्रोड – विभव (अपचयन विभव) के मान भी अधिक होते हैं। अतः ये प्रबल ऑक्सीकारक होते हैं।
प्रश्न 7.24.
स्पष्ट कीजिए कि फ्लुओरीन केवल एक ही ऑक्सो अम्ल, HOF क्यों बनाता है?
उत्तर:
फ्लुओरीन के छोटे आकार तथा उच्च विद्युतॠणता के कारण यह एकमात्र ऑक्सो अम्ल, HOF बनाती है जो कि फ्लुओरिक (I) अम्ल या हाइपोफ्लुओरस अम्ल कहलाता है। फ्लुओरीन उच्चतर ऑक्सो अम्लों में केन्द्रीय परमाणु के रूप में उपयोग में नहीं आ सकता, अतः यह उच्च ऑक्सो अम्ल नहीं बनाता।
प्रश्न 7.25.
व्याख्या कीजिए कि क्यों लगभग एक समान विद्युत्ऋणात्मकता होने के पश्चात् भी नाइट्रोजन हाइड्रोजन आबंध निर्मित करता है, जबकि क्लोरीन नहीं।
उत्तर:
नाइट्रोजन तथा क्लोरीन की विद्युतॠणता लगभग समान होती है फिर भी नाइट्रोजन, हाइड्रोजन बन्ध बनाता है जबकि क्लोरीन नहीं, क्योंकि नाइट्रोजन परमाणु का आकार क्लोरीन परमाणु से छोटा होता है जो कि हाइड्रोजन बन्ध बनाने में सहायक होता है।
प्रश्न 7.26.
ClO2 के दो उपयोग लिखिए।
उत्तर:
ClO2 (क्लोरीन डाइऑक्साइड) को आक्सीकारक तथा विरंजक (Bleaching agent) के रूप में प्रयुक्त किया जाता है।
प्रश्न 7.27.
हैलोजन रंगीन क्यों होते हैं?
उत्तर:
सभी हैलोजन रंगीन होते हैं, इसका कारण यह है कि इनमें दृश्य क्षेत्र में विकिरणों का अवशोषण होता है जिससे बाह्यतम कोश के इलेक्ट्रॉन उत्तेजित होकर उच्च ऊर्जा स्तर में चले जाते हैं क्योंकि संयोजकता कोश व उच्च ऊर्जा स्तर में ऊर्जा अन्तराल कम होता है। विकिरण के भिन्न- भिन्न क्वान्टम अवशोषित करने के कारण ये अलग-अलग रंग प्रदर्शित करते हैं; जैसे- फ्लुओरीन पीला, क्लोरीन हरापन लिए हुए पीला, ब्रोमीन लाल तथा आयोडीन बैंगनी रंग का होता है।
प्रश्न 7.28.
जल के साथ F2 तथा – Cl2 की अभिक्रियाएँ लिखिए।
उत्तर:
फ्लुओरीन (F2) जल को आक्सीकृत करके ऑक्सीजन देती है-
![]()
सूर्य के प्रकाश की उपस्थिति में क्लोरीन, जल के साथ अभिक्रिया करके हाइड्रोक्लोरिक तथा हाइपोक्लोरस अम्ल बनाती है-
Cl2(g) + H2O(l) HCl(aq) + HOCl(aq)
प्रश्न 7.29.
आप HCI से Cl2 तथा Cl2 से HCl को कैसे प्राप्त करेंगे? केवल अभिक्रियाएँ लिखिए।
उत्तर:
(i) HCl से Cl2 प्राप्त करना
सांद्र HCI को मैंगनीज डाइऑक्साइड या KMnO4 जैसे ऑक्सीकारक के साथ गर्म करने से Cl2 प्राप्त होती है।
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O + 5Cl2
(ii) Cl2 से HCl प्राप्त करना
Cl2 की H2 के साथ क्रिया से HCl प्राप्त होती है-
H2 + Cl2 → 2HCl
प्रश्न 7.30.
एन- बार्टलेट Xe तथा PtF6 के बीच अभिक्रिया कराने के लिए कैसे प्रेरित हुए?
उत्तर:
लाल रंग के यौगिक \(\stackrel{+}{\mathrm{O}}_2 \mathrm{PtF}_6^{-}\) के संश्लेषण ने एन- बार्टलेट को Xe तथा PtF6 के बीच अभिक्रिया कराने को प्रेरित किया तथा उन्होंने लाल रंग का ही यौगिक Xe PtF6 बनाया क्योंकि Xe व O2 की प्रथम आयनन एन्थैल्पी लगभग बराबर होती है।
![]()
प्रश्न 7.31.
निम्नलिखित में फॉस्फोरस की ऑक्सीकरण अवस्थाएँ क्या हैं?
(i) H3PO3
(ii) PCl3
(iii) Ca3P2
(iv) Na3PO4
(v) POF3
उत्तर:

प्रश्न 7.32.
निम्नलिखित के लिए संतुलित समीकरण दीजिए।
उत्तर:
(i) जब NaCl को MnO2 की उपस्थिति में सांद्र सल्फ्यूरिक अम्ल के साथ गरम करते हैं तो क्लोरीन गैस निकलती है।
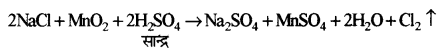
(ii) जब क्लोरीन गैस को Nal के जलीय विलयन में प्रवाहित किया जाता है तो आयोडीन बनती है।
2Nal + Cl2 → 2NaCl + I2
प्रश्न 7.33.
जीनॉन फ्लुओराइड, XeF2, XeF4 तथा XeF6 कैसे बनाए जाते हैं?
उत्तर:
अनुकूल परिस्थितियों में तत्वों की प्रत्यक्ष क्रिया द्वारा जीनॉन तीन प्रकार के द्विअंगी फ्लुओराइड, XeF2, XeF4 तथा XeF6 बनाती है।

143K ताप पर XeF4 तथा O2F2 की क्रिया से भी XeF6 बनता है।
XeF4 + O2F2 → XeF6 + O2
प्रश्न 7.34.
किस उदासीन अणु के साथ ClO– समइलेक्ट्रॉनी है ? क्या यह अणु लुइस क्षारक है ?
उत्तर:
ClF (क्लोरीन फ्लुओराइड) ClO– का समइलेक्ट्रॉनी है क्योंकि दोनों में 26 इलेक्ट्रॉन हैं तथा ClF लुइस क्षारक है क्योंकि इसमें एकाकी इलेक्ट्रॉन युग्म उपस्थित है।
प्रश्न 7.35.
निम्नलिखित प्रत्येक समुच्चय को सामने लिखे गुणों के अनुसार सही क्रम में व्यवस्थित कीजिए-
(क) F2, Cl2, Br2, I2 – आबंध वियोजन एन्थैल्पी के बढ़ते क्रम में
(ख) HF, HCI, HBr, HI -अम्ल सामर्थ्य के बढ़ते क्रम में
(ग) NH3, PH3, AsH3, SbH3, BiH3 – क्षारक सामर्थ्य के बढ़ते क्रम में ।
उत्तर:
(क) I—I < F−F < Br-Br < Cl-Cl
(ख) HF < HCl < HBr < HI
(ग) BiH3 ≤ SbH3 < AsH3 < PH3 < NH3
प्रश्न 7.36.
निम्नलिखित में से कौनसा एक अस्तित्व में नहीं है?
(a) XeOF4
(b) NeF2
(c) XeF2
(d) XeF6
उत्तर:
(b) NeF2
![]()
प्रश्न 7.37.
उस उत्कृष्ट गैस स्पीशीज का सूत्र देकर संरचना की व्याख्या कीजिए जो कि इनके साथ समसंरचनीय है-
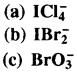
उत्तर:
(a) \(\mathrm{ICl}_4^{-}\) का समसंरचनीय XeF4 है।
XeF4 की संरचना वर्ग समतलीय होती है क्योंकि इसमें Xe पर 4 बन्धित इलेक्ट्रॉन युग्म तथा 2 एकाकी इलेक्ट्रॉन युग्म उपस्थित हैं एवं Xe पर sp3d2 संकरण है।
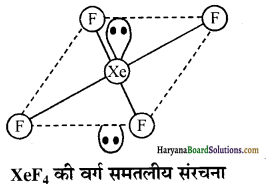
(b) \(\mathrm{IBr}_2^{-}\) का समसंरचनीय XeF2 होता है इसकी संरचना रेखीय है तथा Xe पर sp d संकरण है ( 31.p + 2 b. p ) |
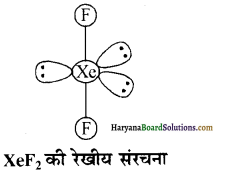
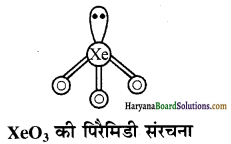
(c) \(\mathrm{BrO}_3\) का समसंरचनीय XeO3 है। इसकी संरचना पिरॅमिडी है तथा Xe पर sp3 संकरण है (3 b.p +1 1.p)।
प्रश्न 7.38.
उत्कृष्ट ‘गैसों के परमाण्विक आकार तुलनात्मक रूप से बड़े क्यों होते हैं?
उत्तर:
उत्कृष्ट गैसों की परमाणु त्रिज्या (आकार) वान्डरवाल त्रिज्या के रूप में ली जाती है जबकि अन्य तत्वों के लिए सहसंयोजी त्रिज्या ली जाती है। उत्कृष्ट गैसों के लिए सहसंयोजी त्रिज्या ज्ञात नहीं की जा सकती क्योंकि ये अणु नहीं बनातीं । चूँकि वान्डरवाल त्रिज्या का मान सहसंयोजी त्रिज्या से अधिक होता है अतः उत्कृष्ट गैसों के परमाण्विक आकार तुलनात्मक रूप से बड़े होते हैं।
प्रश्न 7.39,
निऑन तथा ऑर्गन गैसों के उपयोग सूचीबद्ध कीजिए।
उत्तर:
निऑन तथा ऑर्गन गैसों के उपयोग निम्नलिखित
(a) (i) निऑन का उपयोग विसर्जन ट्यूब (Discharge tube) तथा प्रदीप्त बल्बों (Fluorescent bulbs ) में विज्ञापन प्रदर्शन हेतु किया जाता है।
(ii) निऑन बल्बों का उपयोग वनस्पति उद्यान तथा ग्रीनहाउस में किया जाता है।
(b) (i) ऑर्गन का उपयोग उच्चताप धातु कर्मीय प्रक्रमों में अक्रिय वातावरण उत्पन्न करने के लिए किया जाता है (धातुओं तथा उपधातुओं के आर्क वेल्डिंग में)
(ii) इसका उपयोग विद्युत बल्ब को भरने में किया जाता है।
(iii) प्रयोगशाला में इसका उपयोग वायु सुग्राही (Sensitive) पदार्थों के प्रबन्धन (Handling) में भी किया जाता है।
HBSE 12th Class Chemistry p-ब्लॉक के तत्व Intext Questions
प्रश्न 7.1.
P, As, Sb तथा Bi के द्राइहैलाइडों से पेन्टाहैलाइड अधिक सहसंयोजी क्यों होते हैं?
उत्तर:
किसी यौगिक में केन्द्रीय परमाणु की जितनी उच्च धनात्मक ऑक्सीकरण अवस्था होती है उतनी ही अधिक उसकी ध्रुवण क्षमता होती है जिसके कारण केन्द्रीय परमाणु और दूसरे परमाणु के बीच बने आबंध में सहसंयोजक लक्षण बढ़ते जाते हैं। चूंकि P, As, Sb तथा Bi के पेन्टाहैलाइडों में केन्द्रीय परमाणु की ऑक्सीकरण अवस्था (+5), इनके ट्राइहलाइडों में केन्द्रीय परमाणु की ऑक्सीकरण अवस्था (+3) से अधिक है अतः P, As, Sb तथा Bi के ट्राइहैलाइडों से पेन्यहैलाइड अधिक सहसंयोजी होते हैं।
प्रश्न 7.2.
वर्ग 15 के तत्वों के हाइड्राइडों में BiH3 सबसे प्रबल अपचायक क्यों है?
उत्तर:
वर्ग 15 में NH3 से BiH3 तक हाइड्राइडों का स्थायित्व घटता है क्योंक केन्द्रीय परमाणु का आकार बढ़ने से बन्ध ऊर्जा कम होती है, जिससे इनकी हाइड्रोजन देने की प्रवृत्ति बढ़ जाती है अतः अपचायक गुण बढ़ता है, इसी कारण BiH3 सबसे प्रबल अपचायक है तथा यह सबसे कम स्थायी होता है।
प्रश्न 7.3.
N2 कमरे के ताप पर कम क्रियाशील क्यों है?
उत्तर:
नाइट्रोजन परमाणु के छोटे आकार के कारण N2 में दो नाइट्रोजन परमाणुओं के मध्य त्रिआबन्ध (N ≡ N) होता है जिसमें प्रबल pπ – pπ अतिव्यापन होता है अतः इसकी बन्ध एन्थल्पो अधिक हाता है, इसलिए बन्ध का टूटना मुश्किल होता है। इसी कारण यह कमरे के ताप पर कम क्रियाशील है।
प्रश्न 7.4.
अमोनिया की लब्धि को बढ़ाने के लिए आवश्यक स्थितियों का वर्णन कीजिए।
उत्तर:
अमोनिया का औद्योगिक उत्पादन हाबर विधि द्वारा किया जाता है।
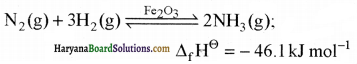
ले-शातैलिए के सिद्धान्त के अनुसार उच्च दाब अमोनिया बनाने के लिए अनुकूल होता है। अतः अमोनिया के उत्पादन के लिए अनुकूलतम परिस्थितियाँ 200 × 105 Pa (लगभग 200 वायुमंडलीय दाब, ~700K ताप तथा थोड़ी मात्रा में K2O एवं Al2O3 युक्त आयरन ऑक्साइड जैसे उत्प्रेरक का उपयोग किया जाता है, ताकि साम्य अवस्था प्राप्त करने की दर बढ़ाई जा सके।
प्रश्न 7.5.
Cu2+ विलयन के साथ अमोनिया कैसे क्रिया करती है?
उत्तर-:
Cu2+ विलयन के साथ अमोनिया (NH3) की क्रिया उपसहसंयोजक बन्ध बनकर संकुल आयन [Cu(NH3)4]2+ बनता है जिसमें NH3 के नाइट्रोजन का एकाकी इलेक्ट्रॉन युग्म धातु आयनों के साथ बन्ध बनाता है क्योंकि NH3 लुइस क्षारक है अतः यह इलेक्ट्रॉन युग्मदाता है।
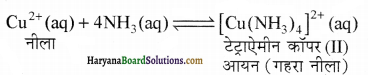
प्रश्न 7.6.
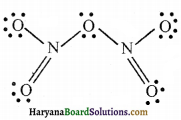
N2O5 में नाइट्रोजन की सहसंयोजकता क्या है?
उत्तर:
N2O5 में नाइट्रोजन की सहसंयोजकता 4 होती है जिसकी पुष्टि निम्नलिखित संरचना से होती है। इसमें नाइट्रोजन परमाणु चार बन्ध बना रहा है।
प्रश्न 7.7.
(a) PH3 से \(\stackrel{+}{\mathrm{P}} \mathrm{H}_4\) का आबंध कोण अधिक है। क्यों?
(b) जब PH3 अम्ल से अभिक्रिया करता है तो क्या बनता है?
उत्तर:
(a) PH3 तथा \(\stackrel{+}{\mathrm{P}} \mathrm{H}_4\) दोनों में ही फॉस्फोरस sp3 संकरित हैं। \(\mathrm{PH}_4^{+}\) में बन्ध कोण 109°28′ तथा इसमें चारों ही बन्धित इलेक्ट्रॉन युग्म होते हैं जबकि PH3 में P पर एक एकाकी इलेक्ट्रॉन युग्म होता है जो कि एकाकी युग्म-आबंध युग्म प्रतिकर्षण के लिए उत्तरदायी है जिससे PH3 में आबंध कोण 109°28′ से कम हो जाता है। अतः PH3 से PH4 का आबंध कोण अधिक है।
(b) जब PH3 अम्ल से अभिक्रिया करता है तो फॉस्फोनियम यौगिक बनते हैं जैसे PH3 + HBr → PH4Br फॉस्फोनियम ब्रोमाइड।
प्रश्न 7.8.
क्या होता है जब श्वेत फॉस्फोरस को CO2 के अक्रिय वातावरण में सांद्र कॉस्टिक सोडा विलयन के साथ गर्म करते हैं?
उत्तर:
श्वेत फास्फोरस को CO2 के अक्रिय वातावरण में सांद्र कॉस्टिक सोडा विलयन के साथ गर्म करने पर PH3 (फॉस्फीन) तथा सोडियम हाइपो फॉस्फाइट (NaH2PO2) बनते हैं।
![]()
प्रश्न 7.9.
क्या होता है जब PCl5 को गर्म करते हैं?
उत्तर:
PCl5 में तीन निरक्षीय या विषुवतरेखीय (equatorial bonds) बन्ध हैं तथा दो अक्षीय बन्ध (axial bonds) हैं जो निरक्षीय बन्धों से बड़े हैं अतः ये निरक्षीय बन्धों से दुर्बल होते हैं, इसी कारण PCl5 को गर्म करने पर यह PCl3 तथा Cl2 में वियोजित हो जाता है।
![]()
प्रश्न 7.10.
PCl5 की जल से अभिक्रिया का संतुलित समीकरण लिखिए।
उत्तर:
PCl5 जल से अभिक्रिया करके (जल-अपघटन) फॉस्फोरस ऑक्सीक्लोराइड (POCl3) देता है जो कि अन्त में फास्फोरिक अम्ल (H3PO4) में परिवर्तित हो जाता है तथा इसके साथ ही HCl भी बनता है।
PCl5 + H2O → POCl3 + 2HCl
POCl3 + 3H2O → H3PO4 + 3HCl
प्रश्न 7.11.
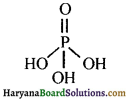
H3PO4 की क्षारकता क्या है?
उत्तर:
H3PO4 में तीन P-OH बन्ध उपस्थित हैं अतः इसकी क्षारकता 3 होती है।
प्रश्न 7.12.
क्या होता है जब H3PO3 को गरम करते हैं?
उत्तर:
ऑर्थोफॉस्फोरस अम्ल (फॉस्फोरस अम्ल ) (H3PO3) को गर्म करने पर असमानुपातन होकर ऑर्थोफॉस्फोरिक अम्ल (फॉस्फोरिक अम्ल ) (H3PO4) तथा फॉस्फीन देता है। इसमें फॉस्फोरस +3 से +5 तथा -3 ऑक्सीकरण अवस्था में परिवर्तित होता है।
![]()
प्रश्न 7.13.
सल्फर के महत्वपूर्ण स्रोतों को सूचीबद्ध कीजिए।
उत्तर:
सल्फर के महत्त्वपूर्ण स्रोत निम्नलिखित हैं-
- भूपर्पटी में सल्फर की मात्रा केवल 0.03 से 0.1% ही होती है।
- संयुक्त अवस्था में सल्फर मुख्यतया सल्फेटों के रूप में, जैसे-जिप्सम (CaSO4.2H2O), एपसम लवण (MgSO4.7H2O), बेराइट (BaSO4) तथा सल्फाइडों के रूप में, जैसे-गेलेना (PbS), यशद ब्लैंड (जिंक ब्लैंड) (ZnS), कॉपर पाइरॉइट (CuFeS2) में पाई जाती है।
- सल्फर की सूक्ष्म मात्रा ज्वालामुखी में हाइड्रोजन सल्फाइड के रूप में भी पाई जाती है।
- कार्बनिक पदार्थों; जैसे-अंडे, प्रोटीन, लहसुन, प्याज, सरसों, बाल तथा ऊन में भी सल्फर होती है।
प्रश्न 7.14.
वर्ग 16 के तत्वों के हाइड्राइडों के तापीय स्थायित्व के क्रम को लिखिए।
उत्तर:
वर्ग में नीचे जाने पर परमाणु आकार बढ़ने के कारण बन्ध वियोजन एन्थैल्पी कम होती जाती है अतः हाइड्राइडों का तापीय स्थायित्व कम होगा।
H2O > H2S > H2Se > H2Te > H2Po
हाइड्राइडों का तापीय स्थायित्व
![]()
प्रश्न 7.15.
H2O एक द्रव तथा H2S गैस क्यों है?
उत्तर:
ऑक्सीजन के छोटे आकार और उच्च विद्युत्त्त्टणात्मकता (3.0) के कारण O-H बन्ध अधिक ध्रुवीय होने से जल के अणु अन्तराअणुक हाइड्रोजन आबंध के द्वारा अधिक संगुणित होकर पास-पास आ जाते हैं। इसके परिणामस्वरूप यह द्रव अवस्था में रहता है, जबकि H2S के अणु दुर्बल वान्डरवाल बल द्वारा आकर्षित होते हैं अतः अणु दूरदूर होने के कारण यह गैस होती है।
प्रश्न 7.16.
निम्नलिखित में से कौनसा तत्व ऑक्सीजन के साथ सीधे अभिक्रिया नहीं करता?
Zn, Ti, Pt, Fe
उत्तर:
इन तत्वों में से Pt, ऑक्सीजन के साथ सीधे अभिक्रिया नहीं करता क्योंकि इसकी क्रियाशीलता बहुत कम होती है अतः यह उत्कृष्ट धातु (Noble metal) है।
प्रश्न 7.17.
निम्नलिखित अभिक्रियाओं को पूर्ण कीजिए-
(i) C2H4 + O2 →
(ii) 4Al + 3O2 →
उत्तर:
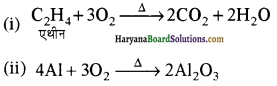
प्रश्न 7.18.
O3, एक प्रबल ऑक्सीकारक की तरह क्यों क्रिया करती है?
उत्तर:
O3 (ओजोन ) आसानी से वियोजित होकर नवजात ऑक्सीजन [O] देती है अतः यह प्रबल ऑक्सीकारक की भाँति कार्य करती है।
O3 → O2 + O ( नवजात ऑक्सीजन )
प्रश्न 7.19.
O3 का मात्रात्मक आकलन कैसे किया जाता है?
उत्तर:
जब ओजोन, बोरेट बफर (उभय प्रतिरोधी) (pH 9.2) युक्त उभय प्रतिरोधित पोटैशियम आयोडाइड (KI) विलयन के आधिक्य से अभिक्रिया करती है तो आयोडीन (I2) मुक्त होती है जिसका मानक सोडियम थायोसल्फेट (Na2S2O3) विलयन के साथ अनुमापन करके O3 गैस का मात्रात्मक आकलन किया जाता है।
प्रश्न 7.20.
तब क्या होता है जब सल्फर डाइऑक्साइड को Fe(III) लवण के जलीय विलयन में से प्रवाहित करते हैं?
उत्तर:
जब सल्फर डाइऑक्साइ्ड को Fe(III) लवण के जलीय विलयन में प्रवाहित करते हैं तो SO2 इसे Fe(II) में अपचयित कर देती है क्योंकि नम सल्फर डाइऑक्साइड (SO2) अपचायक की तरह व्यवहार करती है।
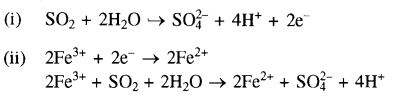
प्रश्न 7.21.
दो S-O आबंधों की प्रकृति पर टिप्पणी कीजिए जो SO2 अणु बनाते हैं। क्या SO2 अणु के ये दोनों S-O आबंध समतुल्य (समान) हैं?
उत्तर:
SO2 अणु कोणीय होता है तथा यह दो अनुनादी संरचनाओं (विहित रूपों) का अनुनाद संकर है अतः ये दोनों S-O बन्ध समान हैं तथा सहसंयोजी हैं।
प्रश्न 7.22.
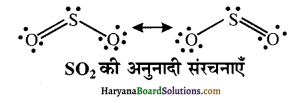
SO2 की उपस्थिति का पता कैसे लगाया जाता है?
उत्तर:
SO2 तीखी गंधयुक्त रंगहीन गैस है। SO2 गैस की उपस्थिति का पता निम्नलिखित परीक्षण से लगाया जाता है। यह अम्लीय पोटैशियम परमैंगनेट (VII) (KMnO4) के गुलाबी विलयन को रंगहीन कर देती है क्योंकि इससे KMnO4 का अपचयन हो जाता है।
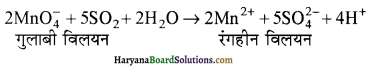
प्रश्न 7.23.
उन तीन क्षेत्रों का उल्लेख कीजिए जिनमें H2SO4 महत्वपूर्ण भूमिका निभाता है।
उत्तर:
H2SO4 निम्नलिखित क्षेत्रों में महत्त्वपूर्ण भूमिका निभाता है-
- पेट्रोलियम के शोधन में,
- अपमार्जक उद्योग में तथा
- उर्वरकों (अमोनियम सल्फेट, सुपर फास्फेट) के उत्पादन में।
प्रश्न 7.24.
संस्पर्श प्रक्रम (सम्पर्क विधि) द्वारा H2SO4 की मात्रा में वृद्धि करने के लिए आवश्यक परिस्थितियों को लिखिए।
उत्तर:
संस्पर्श प्रक्रम द्वारा H2SO4 के निर्माण की मुख्य अभिक्रिया SO2 गैस का V2O5 उत्प्रेरक की उपस्थिति में O2 द्वारा ऑक्सीकरण है।
![]()
यह अभिक्रिया ऊष्माक्षेपी तथा उत्क्रमणीय है एवं इसमें आयतन में कमी होती है। अतः कम ताप और उच्च दाब SO3 की उच्च लब्धि (yield) के लिए उपयुक्त परिस्थितियाँ हैं। परन्तु ताप बहुत कम नहीं होना चाहिए अन्यथा अभिक्रिया की गति धीमी हो जाएगी। अतः सल्फ्यूरिक अम्ल के उत्पादन में प्रयुक्त संयंत्र का दाबं 2 तथा ताप 720K रखा जाता है।
प्रश्न 7.25.
जल में H2SO4 के लिए \(K_{a_2} \ll K_{a_1}\) क्यों है?
उत्तर:
जलीय विलयन में H2SO4 का आयनन दो पदों में होता है-
(i) \(\mathrm{H}_2 \mathrm{SO}_4(\mathrm{aq})+\mathrm{H}_2 \mathrm{O}(l) \rightarrow \mathrm{H}_3 \mathrm{O}^{+}(\mathrm{aq})+\mathrm{HSO}_4^{-}(\mathrm{aq}) \text {; }\)
K1 = बहुत अधिक (\(K_{a_1}\) > 10)
(ii) \(\mathrm{HSO}_4^{-}(\mathrm{aq})+\mathrm{H}_2 \mathrm{O}(l) \rightarrow \mathrm{H}_3 \mathrm{O}^{+}(\mathrm{aq})+\mathrm{SO}_4^{2-}(\mathrm{aq})\)
K2 = 1.2 × 10-2
\(K_{a_1}\) का अधिक मान यह दर्शाता है कि H2SO4 अधिकतर H+ तथा \(\mathrm{HSO}_4^{-}\) में वियोजित हो जाता है।
\(\mathrm{K}_{\mathrm{a}_2}\) का मान \(\mathrm{K}_{\mathrm{a}_1}\) से बहुत कम होता है क्योंकि H2SO4 (उदासीन अणु) का प्रथम वियोजन आसानी से होता है जबकि \(\mathrm{HSO}_4^{-}\) का वियोजन (द्वितीय वियोजन) बहुत कम होता है क्योंक ऋणात्मक आयन में से प्रोटोन का निकलना मुश्किल होता है।
प्रश्न 7.26.
आबंध वियोजन एन्थैल्पी, इलेक्ट्रॉन लब्धि एन्थैल्पी तथा जलयोजन एन्थैल्पी जैसे प्राचलों (Parameters) को महत्व देते हुए F2 तथा Cl2 की ऑक्सीकारक क्षमता की तुलना कीजिए।
उत्तर:
वर्ग में नीचे जाने पर हैलोजनों के जलीय विलयन में उनकी ऑक्सीकारक क्षमता कम होती है जिसकी पुष्टि मानक इलेक्ट्रॉड विभव मानों से होती है जो कि आबंध वियोजन एन्थैल्पी, इलेक्ट्रॉन लब्धि एन्थैल्पी तथा जलयोजन एन्थैल्पी पर निर्भर करते हैं।
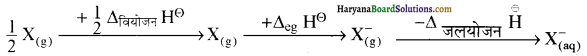
F2 के लिए बन्ध वियोजन एन्थैल्पी का मान Cl2 की तुलना में कम है तथा F– के छोटे आकार के कारण इसकी जलयोजन एन्थैल्पी भी Cl– से बहुत अधिक है अतः F का मानक इलेक्ट्रोड विभव (अपचयन विभव) Cl के मानक इलेक्ट्रोड विभव से अधिक है। इसी कारण F2 का ऑक्सीकारक गुण Cl2 से अधिक है।
प्रश्न 7.27.
दो उदाहरणों द्वारा फ्लुओरीन के असामान्य व्यवहार को दर्शाइए।
उत्तर:
फ्लुओरीन के असामान्य व्यवहार का कारण उसका छोटे आकार, उच्च विद्युतत्रणता, निम्न F-F बन्ध वियोजन एन्थैल्पी तथा संयोजकता कोश में d कक्षकों की अनुपस्थिति है।
फ्लुओरीन के असामान्य व्यवहार के उदाहरण निम्नलिखित हैं-
- फ्लुओरीन केवल एक ऑक्सो अम्ल बनाती है जबकि दूसर हैलोजन कई ऑक्सो अम्ल बनाते हैं।
- F2 की आबंध वियोजन एन्थैल्पी तथा इलेक्ट्रॉन लब्धि एन्थैल्पी के मान अपेक्षित मानों से बहुत कम होते हैं।
प्रश्न 7.28.
समुद्र कुछ हैलोजन का मुख्य स्तोत है। टिप्पणी कीजिए।
उत्तर:
समुद्र कुछ हैलोजनों का मुख्य स्रोत है क्योंकि समुद्री पानी में सोडियम, पोटैशियम, मैग्नीशियम तथा कैल्शियम के क्लोराइड, ब्रोमाइड तथा आयोडाइड होते हैं लेकिन मुख्यतः यह सोडियम क्लोराइड का विलयन (द्रव्यमान 2.5%) है। शुष्क हुए समुद्री निक्षेपों में सोडियम क्लोराइड तथा कारनेलाइट (KCl.MgCl2.6H2O) जैसे यौगिक उपस्थित होते हैं। कुछ समुद्री जीवों के तंत्र में आयोडीन होती है; बहुत से समुद्री पादपों में 0.5% आयोडीन तथा चिली साल्टपीटर में 0.2% तक सोडियम आयोडेट पाया जाता है।
प्रश्न 7.29.
Cl2 की विरंजक क्रिया का कारण बताइए।
उत्तर:
Cl2 एक प्रबल विरंजक है। विरंजन क्रिया नमी की उपस्थिति में ऑक्सीकरण के कारण होती है। नमी की उपस्थिति में Cl2 नवजात ऑक्सीजन [O] देती है जो रंगीन पदार्थ का ऑक्सीकरण करके उसे रंगहीन कर देती है। यह विरंजन स्थायी होता है।
Cl2 + H2O → 2HCl + [O]
रंगीन पदार्थ + [O] → रंगहीन पदार्थ
![]()
प्रश्न 7.30.
उन दो विषैली गैसों के नाम बताइए जो क्लोरीन गैस से बनाई जाती हैं।
उत्तर:
क्लोरीन गैस से बनाई जाने वाली विषैली गैसें फास्जीन (COCl2), अश्रु गैस (CCl3NO2) तथा मस्टर्ड गैस (Cl-CH2-CH2-S-CH2-CH2-Cl) हैं।
प्रश्न 7.31.
I2 से ICI अधिक क्रियाशील क्यों है?
उत्तर:
सामान्यतः अंतराहैलोजन यौगिक हैलोजन की अपेक्षा अधिक क्रियाशील होते हैं क्योंकि X-X आबंध की अपेक्षा X-X’ आबंध दुर्बल होता है। l-Cl बन्ध ध्रुवीय तथा l-l बन्ध अध्रुवीय है। अतः lCl, l2 से अधिक क्रियाशील है।
प्रश्न 7.32.
हीलियम को गोताखोरी के उपकरणों में उपयोग क्यों किया जाता है?
उत्तर:
आधुनिक गोताखोरी के उपकरणों में हीलियम, ऑक्सीजन के तनुकारी (Diluent) के रूप में प्रयुक्त की जाती है क्योंक रक्त में इसकी विलेयता बहुत कम होती है।
प्रश्न 7.33.
निम्नलिखित समीकरण को संतुलित कीजिए –
XeF6 + 2H2O → XeO2F2 + 4HF
जीनॉन डाइऑक्सीडाइफ्लुओराइड
प्रश्न 7.34.
रेडॉन के रसायन का अध्ययन करना कठिन क्यों था?
उत्तर:
रेडॉन (Rn) रेडियोसक्रिय तत्व है तथा इसकी अर्धायु बहुत कम (3.82 दिन) होती है अतः इसका विघटन हो जाता है। इसलिए रेडॉन के रसायन का अध्ययन कठिन हो जाता है।